2017年优先审评发力,一批创新药加速审批上市。2016 年 2 月 26 日,CFDA 发布《关于解决药品注册申请积压实行优先审评审批的意见》,正式确定了三类可优先审评审批药品的范围:创新药、儿童用药、临床亟需药、专利过期药和首仿药等受到重点扶持。截至2017年底,药审中心共将25批 423 件注册申请纳入优先审评程序,其中具有明显临床价值的新药占比最大,共191件,占45%,有33件具有明显临床价值的新药注册申请通过优先审评程序得以加快批准上市。
优先审评新药占比45%
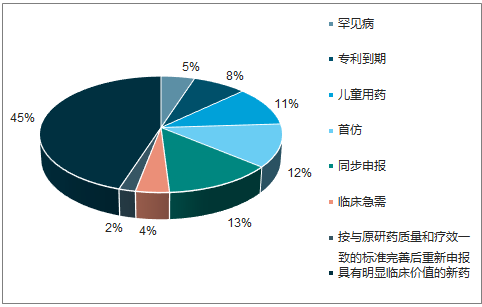
数据来源:公开资料整理
相关报告:智研咨询发布的《2018-2024年中国中药创新药物行业竞争态势及未来发展趋势报告》
2017年全球52个创新药首次上市,是继2016的“33个”低谷后的强势反弹。2017 年全球获批上市113个新药,其中 52个新药首次上市,7款为首创新药(first-in-class),包括 CAR-T 疗法,色氨酸羟化酶 1(TPH1)抑制剂telotristatethyl,抗白介素-4 受体α(IL-4Rα)单克隆抗体((MAb) dupilumab 和嘌呤核苷酸磷酸化酶(PNP)抑制剂 forodesine。具体细分来看,2017全球获批的生物药和新分子实体持平,新药上市申请中新分子实体占比仍超过一半。2017 全球获批的生物药和新分子实体相较 2016 年均有较大幅度的提升,两者数量相等,同时新药上市申请新分子化学实体占66%,仍然超过创新生物药。
2017全球获批创新生物药和新分子实体持平
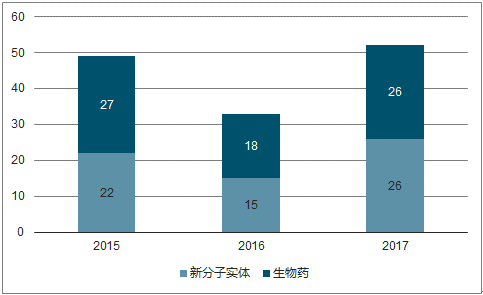
数据来源:公开资料整理
全球新药上市申请中新分子实体占比66%
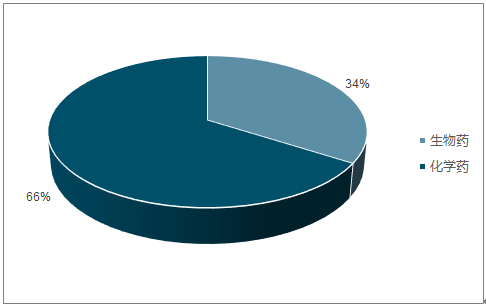
数据来源:公开资料整理
作为全球药物创新的领头羊,2017年美国 46个新药获批上市。2017年FDA药品审评与研究中心(CDER)批准了46个新药,达到近10 年新药批准的最高值,这些新药包括新药申请NDA中的新分子实体(NME)34个和生物制品许可申请(BLA)12个。
2017年美国46个新药获批上市,达近10年最高

数据来源:公开资料整理
2017我国1类创新药申报数量174个,超60个临床Ⅲ期1类药物即将迎来收获期。 2017 年我国1.1类化药申报数目为112 个,达十年之最;1 类生物药申报数量62个,是 2016 年的2倍多。根据数据,截至2018年5月有超 60个1类新药进入临床Ⅲ期。
2017年我国新分子实体申报112项
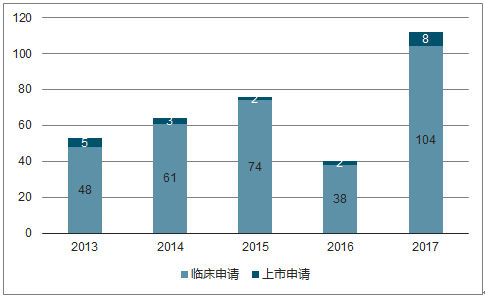
数据来源:公开资料整理
2017年我国1类生物药申报62项
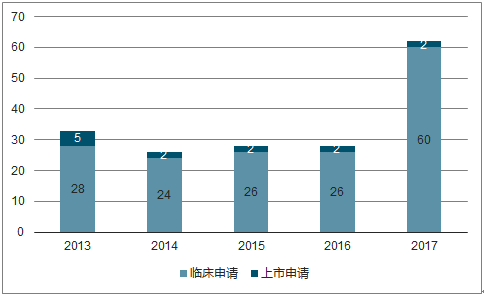
数据来源:公开资料整理
 智研咨询 - 精品报告
智研咨询 - 精品报告

2026-2032年中国小分子创新药行业市场竞争格局及发展前景研判报告
《2026-2032年中国小分子创新药行业市场竞争格局及发展前景研判报告》共九章,包含2021-2025年中国小分子创新药行业竞争格局分析,主要小分子创新药企业或品牌竞争分析,2026-2032年中国小分子创新药行业发展前景预测等内容。

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询























