乳腺癌是中国第四大癌种,晚期乳腺癌根据HER2和HR表达主要分为三条赛道:激素阳性(HR+,9.9万人)、HER+(3.5万人)、三阴乳腺癌TNBC(HR-且HER-,3.5万人)。
HR+赛道暂无国产新药。辉瑞进口CDK4/6抑制剂哌柏西利已上市,国产微芯生物组蛋白去乙酰化酶(HDAC)抑制剂西达本胺乳腺癌适应症NDA。
HER2受biosimilar冲击,吡咯替尼已上市。曲妥珠联合帕妥珠+化疗是NCCN推荐的HER2+、HR-乳腺癌首选治疗方案,另外恒瑞新药吡咯替尼已上市。
FDA加速批准PD-L1阿特珠单抗治疗TNBC,中国临床需求尚未满足。
FDA已批准3款治疗乳腺癌的CDK4/6抑制剂上市,辉瑞的哌柏西利2018年在中国获批上市,中国区核心专利2023年到期,目前齐鲁制药的仿制药已处于申请上市阶段。西达本胺是全球首个亚型选择性组蛋白去乙酰化酶(HDAC)抑制剂,联合依西美坦用于绝经后HR+晚期乳腺癌二线对比安慰剂疗效显著(mPFS:7.4月v.s3.8月)。
HER2+乳腺癌一线及新辅助治疗采用曲妥珠、帕妥珠,而拉帕替尼为主二线治疗中吡咯替尼疗效显著,头对头试验优于拉帕替尼,但面临即将上市的T-DM1等新机制药物的市场竞争。要二线治疗方案。
二线治疗竞争激烈,临床数据显示吡咯替尼疗效占优
试验分期 | 主要试验药物 | 实验设计(试验:对照) | 试验组PFS(月) | 对照组PFS(月) |
II | 吡咯替尼 | 吡咯替尼+卡培他滨 拉帕替尼+卡培他滨 | 18.1 | 7 |
III | 吡咯替尼 | 吡咯替尼+卡培他滨 安慰剂+卡培他滨 | 11.1 | 4.1 |
III | T-DM1 | T-DM1 拉帕替尼+卡培他滨 | 9.6 | 6.4 |
III | T-DM1 | T-DM1+帕妥珠单抗 曲妥珠单抗+紫杉类 | 15.2 | 13.7 |
III | T-DM1 | T-DM1+帕妥珠单抗 T-DM1+安慰剂 | 15.2 | 14.1 |
III | T-DM1 | T-DM1 无 | 暂无 | 暂无 |
数据来源:公开资料整理
吡咯替尼作为创新药目前治疗费用较高,有待进入医保放量。从试验布局看,联用曲妥珠治疗乳腺癌是吡咯替尼市场拓展的战略方向,但面临帕妥珠单抗等药物竞争,疗效有待验证。
吡咯替尼目前已完成/在研临床试验
治疗 场景 | 试验 分期 | 实验设计(试验:对照) | 试验状态 |
新辅助 | III | 吡咯替尼+曲妥珠+多西他赛 安慰剂+曲妥珠+多西他赛 | 在研 |
辅助/ 一线 | III | 吡咯替尼+曲妥珠+多西他赛 安慰剂+曲妥珠+多西他赛 | 在研 |
二线 | II | 吡咯替尼+卡培他滨 拉帕替尼+卡培他滨 | 已完成 |
III | 吡咯替尼+卡培他滨 安慰剂+卡培他滨 | 已完成 |
数据来源:公开资料整理
2019年3月,阿特珠单抗(PD-L1)联合紫杉醇治疗PD-L1阳性的TNBC获得FDA加速批准。目前中国尚未有相关产品上市。
阿特珠单抗治疗PD-L1疗效显著
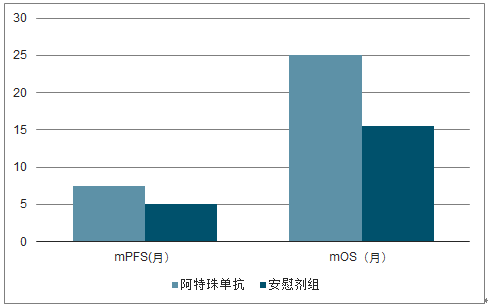
数据来源:公开资料整理
相关报告:智研咨询发布的《2019-2025年中国乳腺癌治疗药物市场前景分析及发展趋势预测报告》

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询


















![2026年中国合成生物行业发展全景分析:下游应用从医药健康、化工材料向农业食品、能源环保全面渗透,行业已展现出巨大的应用潜力[图]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![2026年中国骨密度仪行业产业链图谱、采购总量、采购金额、获批企业、竞争格局及未来竞争趋势分析:外资品牌占据主导地位[图]](http://img.chyxx.com/images/2022/0330/e060dd24be7392f76ddd0a84489963879d953ac6.png?x-oss-process=style/w320)
![研判2026!中国物联网行业概念、市场规模、企业竞争格局分析:中国物联网产业领跑全球,AI融合驱动“泛在智联”新纪元[图]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![研判2026!中国汽车行业分类、产销量、重点企业销量分析:一季度中国汽车行业现“内冷外热”分化,出口同比激增成核心增量引擎[图]](http://img.chyxx.com/images/2022/0330/ff5315f651f3e124d0f5a156ac51655e46e5433f.png?x-oss-process=style/w320)
![2026年中国彩钢板行业发展历程、供需情况、市场规模、竞争格局及趋势研判:彩钢板市场规模达1138.76亿元,钢结构与绿色建材政策驱动增长[图]](http://img.chyxx.com/images/2022/0330/4279f04d08c7260a105d321a303d34a91af3a3d5.png?x-oss-process=style/w320)
![2026年中国UV灯管行业产业链、发展现状、竞争格局、竞争趋势分析:外资垄断高端赛道,中低端市场竞争白热化[图]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)
