生物医药外包包括:研发外包(CRO)、生产外包(CMO)、销售外包(CSO)、管理外包(SMO)及其他外包服务,最主要的还是CRO与CMO。
与全球CRO市场以临床前研究为主不一样的是,目前国内CRO公司业务主要集中在新药早期临床前研发以及临床研究两大方面,其中临床前研究约占43%;临床试验研究约占57%。2018年我国临床前研究市场规模为268.3亿元;临床试验研究市场规模为360亿元。
2007-2018年中国CRO细分市场收入
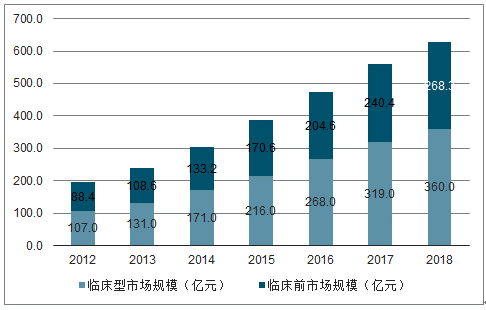
数据来源:公开资料整理
2018年中国CRO市场结构占比
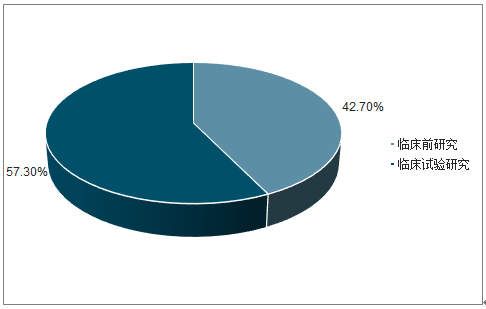
数据来源:公开资料整理
一、医药外包服务(CRO/CMO):政策催化行业高景气
从CDE公布的历年药品审评报告可以看出,从2015年起,我国药品注册申请审评审批(包括临床试验申请、进口再注册申请、补充申请、ANDA、NDA等)速度明显加快,从2015年前的年均5000件审评完结量大幅提升到1万件左右;CDE药品注册审评大幅提速,积累等待审评量从2015年高峰期20000万件下降到2017年末约4000件水平,2018年新增新药注册受理数量回升,年末积累等待评审数量小幅回升到4370件左右。评审速度翻倍,新药审批等待时间大幅缩减,都有利于CRO行业潜在客户需求提升。
CDE新药注册审评审批完结量和积累量(件)
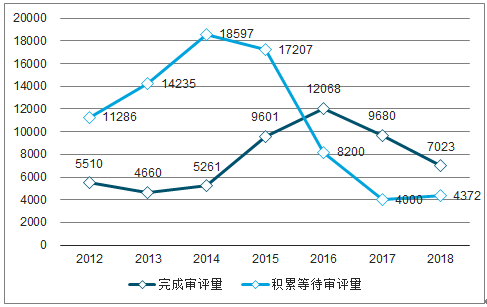
数据来源:公开资料整理
从2012年开始,国务院和药监部门就提出开展仿制药一致性评价,2016年3月,国务院办公厅正式对外公布《关于开展仿制药质量和疗效一致性评价的意见》,规定化学药品新注册分类实施前批准上市的仿制药,凡未按照与原研药品质量和疗效一致原则审批的,均须开展一致性评价。仿制药一致性评价包括药学等效(PE)和生物等效(BE)两部分,国家基药目录289个品种需要在2018年底完成,我国大部分药企不具备资源自行开展一致性评价的能力,大型药企有自行开展能力但是旗下拥有批文众多,时间就是金钱,谁先通过一致性评价,谁将抢占一致性评价后药品市场。
2017年一致性评价收入大幅提升到1.81亿元,同比大增190%,营收占比提升到10.7%;2018全年完成约100个一致性评价项目,营收超3亿元。
二、国际CRO向国内产业转移:低成本、庞大人口和丰富疾病谱
低成本、庞大人口和丰富疾病谱,促使国际CRO向国内产业转移。目前,新药研发难度不断提高,高投入、长周期、高淘汰率始终伴随新药研发全过程;另外,药企现有专利药将在未来几年内专利保护集中到期,专利悬崖导致仿制药冲击专利药原有市场,降价和市场被蚕食不可避免。国际药企为降本增效,有动力在持续高投入新药研发的基础上,寻求低成本的各类医药外包服务,国际新药研发CRO正在经历向包括中国在内的亚洲低成本地区转移浪潮,主要基于以下几点:低成本。具体体现在高素质低成本的专业人才获取和低成本的临床病例两方面。
高素质低成本的专业人才。每年我国大学高校毕业人数超过700万,硕博研究生招生人数超过60万,拥有大量后备专业人才储备;另外,海外有丰富从业经验的各类医药外包服务人才回流国内。我国人均收入水平远低于欧美发达国家,高素质低成本的专业人才获取,为人才与技术密集型的我国CRO行业带来竞争优势。
低成本的临床病例。国外对药物在人体进行试验管理相当严格,药物观察和注册周期都很长,对试药人有严格保护措施;另外,国内外平均收入差距巨大,我国受试人获得的经济补偿只有美国的1/10。据调查数据显示,将各类药物的临床试验数据平均来看,2010年在美国完成1例Ⅰ期临床试验所需的综合成本约为6000美元,Ⅱ期临床试验为7000美元,Ⅲ期临床试验为8000美元。在中国进行临床试验完成一例合格病例所需的成本通常不超过20000元,大大低于国外的试验成本。国内低廉的研究成本吸引海外订单转移。
庞大的病患人群和丰富的疾病谱。我国人口众多,在疾病种类的多样性和病例数量方面拥有其他国家所不具备的条件,足够数量临床试验病例的召集和临床终点的完成,相比欧美发达国家都有优势,尤其是在一些罕见病或需要长时间临床终点的癌症等疾病方面,可入列临床病例数大大提高,提高了临床试验研究的可靠性和统计学意义。
国内外临床试验成本比较(单位:美元)
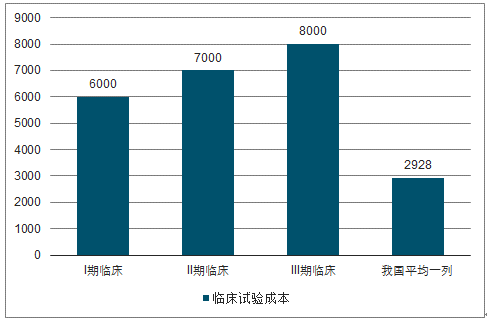
数据来源:公开资料整理
医药外包服务(CRO/CMO)行业上市公司主要有药明康德、泰格医药、康龙化成、博济医药、昭衍新药、凯莱英和百花村,百花村由于计提资产减值,导致2017-2018年连续两年扣非净利润重大亏损。近年来,医药外包服务行业受鼓励药械创新和仿制药一致性评价政策影响,营收连年实现快速增长,2018年,行业主要公司营收均实现20%以上的高增长;扣非后核心净利润方面,均实现24%以上高速增长,利润增速高于营收增速,头部企业2019年估值水平在45倍左右,成长性和估值相对匹配。
医药外包服务CRO/CMO仍将快速增长,标的上选择行业头部公司,如药明康德、泰格医药、康龙化成。药明康德是一家覆盖新药研发、生产全流程的CRO/CMO企业,优势在CRO上游新药分子开发和筛选以及CMO领域,近年来也逐步拓展临床CRO业务,以实现CRO、CMO全覆盖;泰格医药主要集中在临床CRO;康龙化成优势在上游新药分子开发和筛选,在国内新药分子发现领域营收仅次于药明康德,近年来逐渐向临床CRO、CMC等全产业链拓展。
2012年中国CMO市场容量为22亿美元,同比增长16%,而2018年其增长将超过2012年一倍多,达到58亿美元,5年的CAGR为17.62%。由于政策所限,目前大部分国内CMO只能开发国际市场,主要客户是国际制药巨头,随着国内市场的逐步开启,国内CMO增速有望继续突破。
2012-2018年中国CMO市场规模趋势
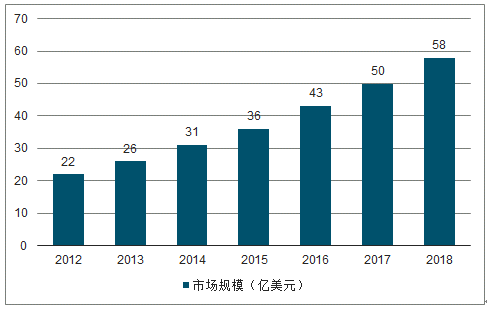
数据来源:公开资料整理
而在医药外包方面,中国医药服务外包市场潜力无限。特别近几年,中国加速推行医药体制改革,国家已经明确把医药产业作为一个新兴产业进行推动,并加大投资力度。中国已经成为全球最具吸引力的医药投资市场,越来越多的外资企业来到中国,挖掘市场商机和寻找合作伙伴。
目前中国生物医药外包服务企业近千家,药物研究开发生产外包服务市场规模达超过千亿规模,随着我国医药行业以及服务外包行业利好政策不断,我国医药外包行业将会继续保持较高速度增长,未来5年药物研究开发生产外包服务市场规模将保持10%-15%的增速,预计2024年我国药物研究开发生产外包服务市场规模将达2000亿元以上。
2019-2024年中国药物研究开发生产外包服务市场规模及预测
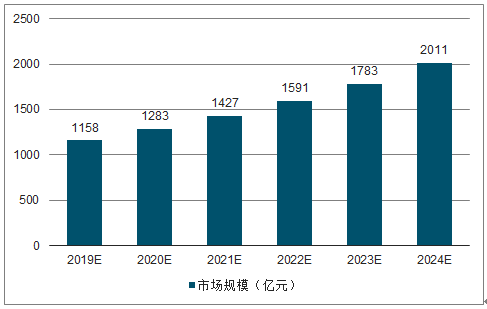
数据来源:公开资料整理
相关报告:智研咨询发布的《2019-2025年中国CRO医药研发外包行业运营态势及投资前景预测报告》
 智研咨询 - 精品报告
智研咨询 - 精品报告

2026-2032年中国医药外包(CXO)行业市场运营态势及投资机会研判报告
《2026-2032年中国医药外包(CXO)行业市场运营态势及投资机会研判报告》共十一章,包含中国医药外包(CXO)行业重点企业布局案例研究,中国医药外包(CXO)行业市场前景预测及发展趋势预判,中国医药外包(CXO)行业投资战略规划策略及建议等内容。

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询


















![2026年中国医药外包(CXO)行业政策、运行现状、细分市场、竞争格局及未来发展趋势研判:创新药融资与BD交易双升,CXO行业景气度持续向上[图]](http://img.chyxx.com/images/2022/0408/54b870b64f647f1fc10474b02796382c9242dcfa.png?x-oss-process=style/w320)

![智研研判!医药制造外包(CMO/CDMO)行业现状及趋势分析:国产企业加速拓展高附加值业务,行业规模不断扩容[图]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)


