对于医药行业来说,技术研发水平间接代表着行业发展水平。无论是药品还是制药设备,都在疾病治疗过程中起着重要的辅助作用,如果医药技术研发水平不够先进,医疗水平的进步就会受到影响。
如果医药技术研发水平不够先进,医疗水平的进步就会受到影响。因此,医疗技术的持续进步,将带动医药产业走上新的台阶。
一、中国医药品进出口量分析
智研咨询发布的《2020-2026年中国医药生物行业竞争现状及投资前景规划分析报告》数据显示:2019年1-3季度中国医药品进口量逐渐增长,2019年12月中国医药品进口量为1.5万吨,同比增长15.4%。
2019年1-12月中国医药品进口量及同比增长走势分析
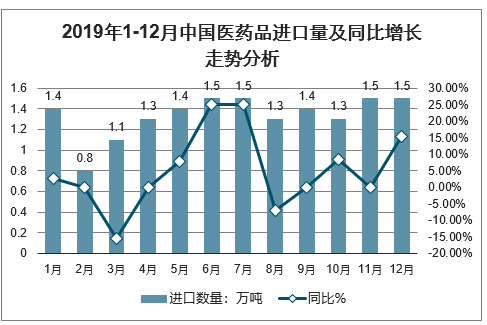
数据来源:公开资料整理
从金额方面来看,2019年12月中国医药品进口金额为3413百万美元,同比增长22.8%。
2019年1-12月中国医药品进口金额及同比增长走势分析
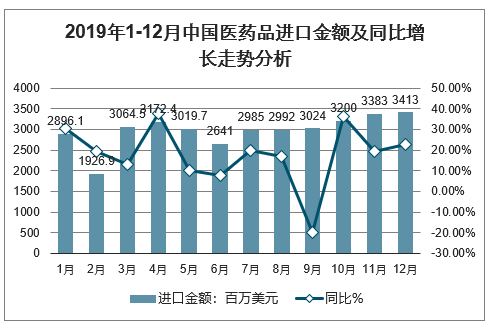
数据来源:公开资料整理
2019年1-12月中国医药品进口数量及金额增长率情况
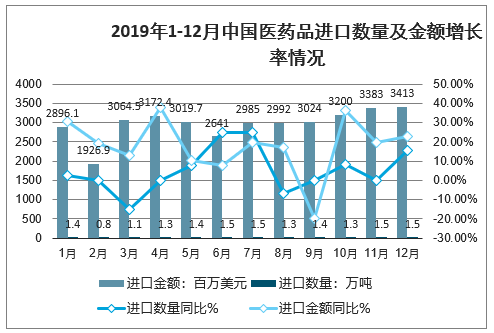
数据来源:公开资料整理
一、药品研发创新情况分析
随着鼓励药品研发创新的政策不断出台落地,国内药品研发迎来历史上最好的黄金时代,国内以恒瑞医药、复星医药、中国生物制药等为首的大型制药企业抓住行业机遇,持续加大研发投入,加快推进产品管线的构建及上市进程。而作为创新的新兴力量,百济神州、信达生物、歌礼制药等biotech在资本助力下也全力加速创新管线推进。随着市场对这些创新药企业的预期现金流改善及成长性加快的判断加强,创新药成为未来几年医药板块的最大主题。
从2013-2019H1的国内大型制药企业研发投入占比来看,以恒瑞医药为代表的创新药龙头企业研发占比已经达到15%左右,接近跨国药企的研发投入水平。国内大型制药企业的研发投入增速也在不断的创新高,恒瑞医药的研发投入已稳定保持在50%以上增长
目前国内制药企业的研发多是FAST-FOLLOW的策略,可以减少新药研发风险的同时又可以缩短新药研发的时间。而FAST-FOLLOW的创新模式对新药研发的进度要求高,同类药物率先上市、先进医保能够在市场份额中占据极大的优势。
2019年11月国家药品审评中心新出台了《突破性治疗药物工作程序(征求意见稿)》,明确提出了“新的临床试验数据不再显示比现有治疗手段具有明显临床优势”、“已有相同适应症的药物获批上市,成为新的治疗手段,而该药物无法证明较新上市药物具有明显临床优势”两种情形终止突破性治疗药物认定。该项制度的提出对于fast-follow能力极强的恒瑞医药等龙头企业是极大的利好,也反映了监管部门对于国内制药企业Best-in-class/First-in-class研发策略的引导,这也是我国创新药三步走从崛起到跨越阶段重要的战略指导,引导国内企业迈向全球制药先进行列
与全球First-in-Class越来越小的差距也使得国内创新药产品在欧美规范市场更具竞争力,越来越多的企业选择将自己的创新药中美同时临床及申报。相比于欧美市场,国内的药品市场规模有限,要想成为国际化的制药企业就必须走向国际化的市场。并且国内的创新药专利保护、创新药医保覆盖等制度仍待改善,想要在创新的道路上继续向前,欧美市场也是必然的选择。
国内还没有创新药产品在欧美法规市场成功商业化的案例,国内也没有企业能够在海外建立自己的学术推广团队。但是随着大量创新药海外注册申报及临床,国内药企与欧美企业授权合作协议越来越多,创新产品海外收入将为DCF模型现金流的重要来源,尤其是在中国第一个自主1类新药泽布替尼以“突破性疗法”获FDA批准后
随着新药研发时间及金钱成本不断提高,和销售市场及专利到期后对原研药的市场冲击,全球制药企业为了缩短研发周期、控制成本、降低研发风险等,逐步将资源集中在疾病机理研究、新药靶点发现等研发早期研究,而将后续研发中晚期及开发阶段涉及的药物筛选、临床前研究、临床研究、合同生产等委托给医药研发服务企业。根据新药研发领域中客户服务阶段的不同,医药研发服务一般分为合同研发服务(CRO)、合同生产业务/合同生产研发业务(CMO/CDMO),分别对应新药研发领域中的临床前研究及临床研究、定制化生产及研发服务等产业链中的不同环节。
从产业链逻辑来看,CRO行业主要包括临床前CRO(药物发现、临床前研究)、临床CRO(I-III期临床、注册申报及上市后临床等);从时间跨度来看,新药研发一般需要10年以上的研究,其中药物发现需要2-3年、临床前研究1-3.5年、I-III期临床5-7年,注册申报上市0.6-2年;从研发费用分布来看,药物筛选占5%、药物学研究10%、药物安全性评价15%、临床I期占5%、临床II期占15%、临床III期占50%
新药研发过程中各阶段费用占比情况
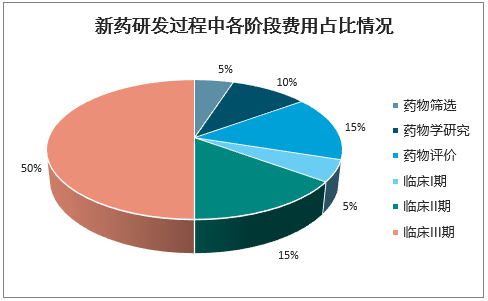
数据来源:公开资料整理
从全球来看,跨国巨头包括QuintilesIMS、Covance、Parexel、Charlesriver等,其中QuintilesIMS主要业务布局在临床CRO研究、Covance实现从药物发现到临床CRO的全产业链布局、Charlesriver以药物发现及药物安全性评价见长。国内行业内标杆性企业有药明康德(化药CRO全产业链布局,尤其以药物发现见长)、昭衍新药(药物安全性评价的细分市场龙头、积极沿产业链延伸)、泰格医药(国内临床CRO龙头、积极进行全球网络化布局)、药明生物(生物药从药物发现到CDMO行业领先者)、博腾股份、凯莱英、和全药业(国内CDMO行业领先者)
二、全球研发支出呈现稳健增长,外包比例呈现提升趋势、产能呈现转移趋势
回顾全球研发外包趋势:全球研发支出呈现稳健增长,研发外包比例呈现上升趋势
2016年全球医药市场规模和全球研发支出规模分别达到1.15万亿美元和1454亿美元,预期其分别在未来5年保持5%和2%的复合增长;相应的受益于大型跨国药企外包倾向增加以及小biotech呈现繁荣发展等带来的外包比例呈现上升趋势,全球CRO市场规模从2012年的323亿美元上升到2017年的533亿美元(5年年均复合增长率为10.54%),预期未来5年仍然能保持8%左右的复合增长、至2021年达到735亿美元。
2012-2021年全球医药市场规模及增长走势预测
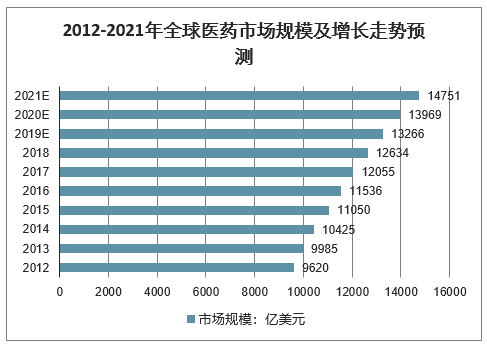
数据来源:公开资料整理
2012-2021年全球医药研发外包比例走势预测
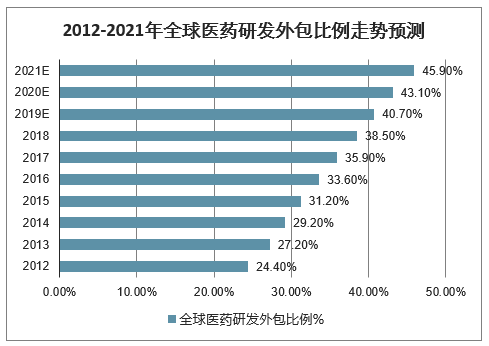
数据来源:公开资料整理
从CRO全球市场份额分布情况来看,由于不同地区CRO产业发展时长不同,产业地域分布差异明显。主要以欧美国家为主,合计占比超80%。全球前50位的CRO企业大部分位于欧美发达国家。不过随着CRO巨头的全球扩张以及亚洲生物医药的迅速崛起,CRO产业逐渐向亚洲转移。
2015-2021年全球各区域市场规模及增长走势预测
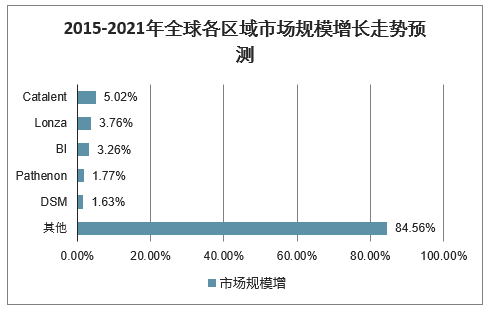
数据来源:公开资料整理
全球来看靶向免疫疗法呈现明显上升趋势,跨国药企研发支出呈现稳健增长
对创新靶点作用机制的探索、小biotech数量增多以及研发的加速,驱动整体靶向治疗药物的数量不断增加,2018年肿瘤药研发后期管线包含849个分子药物,自2008年以来增长了77%、相对2017年同比增长19.4%;结构上来看,2018年处于研发后期的抗肿瘤药物中,91%为小分子靶向制剂和大分子靶向生物制品,其中靶向生物制剂增加了近30%、靶向小分子药物增加了14%,呈现明显增长。
探索新一代肿瘤生物疗法:自2013年以来,新一代肿瘤生物疗法(细胞、基因和核苷酸疗法)的研发数量增加了一倍多,2017-2018年增长了32%、目前占研发后期管线仅为不到10%;肿瘤NGB管线候选药物中,36%为癌症疫苗、25%的为CAR-T疗法。
持续探索免疫肿瘤治疗机制:目前在研的450种免疫肿瘤疗法中,III期和预注册管线仅包含9种免疫肿瘤治疗机制,而早期研发管线包含62种机制。Anti-PD-1/anti-PD-L1、B淋巴细胞CD19抗原抑制剂(CAR-T治疗的靶点)和B淋巴细胞CD20抗原抑制剂(下一代CAR-T靶点)在III期和预注册管线中占比50%以上,在I期和II期管线中占比27%。
肿瘤药研发管线后期项目呈现快速增长,以及对新一代生物疗法和免疫治疗机制的探索等,全球前10和前30的跨国药企研发支出呈现稳健增长,即全球前10大跨国药企研发支出从2015年的640亿美元提升到2018年的779亿美元,期间保持6.78%复合增长,高于全球制药企业研发投入复合增速2%;前30名全球研发投入2015-2018年复合增长率为4.7%,高于全球行业增长。
政策+全球第二大市场+研发成本低多重因素共振加速跨国药企的产业化转移
中国自2009年以来一直进行新一轮医改,尤其是2015年以来对药品的审评审批、临床数据要求加快加严,特别是2017年修订了药品管理法和注册法等,进一步完善国内鼓励创新,加速审评审批。2018年中国正式加入国际人用药品注册技术协调会(ICH),未来审评审批标准将与欧美等国家对齐,同时随着国内医药市场占全球比重的提升,未来将有越来越多的跨国药企将中国作为第一批次上市的市场,将会优选开展包括中国在内全球多中心临床,以实现在中国的优先上市。
2012-2021年中国医药市场全球占比走势预测
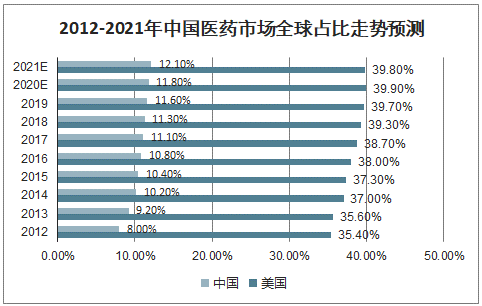
数据来源:公开资料整理
根据上海医药临床研究中心研究报告,国内临床试验成本一般仅相当于西方发达国家成本的30%~60%。目前,在国内医药政策环境逐渐好转以及我国加入ICH的双重背景下,国内具有成本优势和人口优势,预期未来跨国药企将进一步加大研发部门的转移,重大利好本土优质CRO企业。
三、2020年医药行业发展方向分析
在“4+7”带量采购、分级诊疗、新医保目录出台等医药行业政策频出的大背景下,未来市场发展又将会有哪些趋势
创新药发展被看好
近2年,可以看到CDE受理的新药申请明显在增加,2018年受理化药创新药申请167件,相比2015年增加了80件。申报的数量变多,获批的产品也相应增加。在2018年国产的9个一类新药获批,涉及恒瑞医药、正大天晴、歌礼药业等国内优秀企业。也可以看出中国的创新药也逐步进入了收获期,随着相关企业药品研发顺利推进,未来将有越来越多的创新药获批上市。而受益于国内医药创新政策的催化、一致性评价的执行,国内药企正在越来越重视创新药发展,预计未来在创新药领域还将维持高强度的研发投入。
目前,从国产的PD-1单抗正逐步开始销售,大适应症和联用也将逐步登上舞台;其次生物类似药也将集中上市等情况看来,创新药发展趋势一片大好。业内认为,虽然创新药竞争有一定加剧,但在支付能力提升、放量加速的情况下,龙头企业快速跟随,有望实现多产品布局;且基本上和外资站在同一水平线竞争,有望占据较大市场份额。创新药依然是未来备受青睐的大趋势,建议布局产品管线丰富的创新药龙头标的。
医疗器械领域发展潜力大
在我国,医疗器械是一个朝阳行业。有数据显示,中国医疗器械市场规模近五年来一直保持稳步增长。已由2014年的2556亿元增长至2018年的5304亿元,年均增速保持在20%左右,营业收入及净利润均保持高速增长态势,正步入医疗器械行业发展黄金期,预计到2022年中国医疗器械市场规模将超过9000亿元。截至2019年4月,全国共有医疗器械类企业约1.88万家,其中以广东、江苏和北京为典型省市,拥有医疗器械企业数量分别为3743家、2558家和1852家。
未来随着国家政策的扶持、不断扩大的市场需求、中国人口老龄化加速以及医疗器械行业的技术发展和产业升级,医疗设备将有望继续保持高速增长的良好态势,并实现从中低端市场向高端市场进口替代的愿景。总体来说,器械行业因为其基数低空间大,是一个可以长期享受高成长性的行业。但是由于医药受政策的影响比较大,所以必须在把握政策的基础上充分了解各个子行业和公司的基本面,因地制宜做价值投资。
CRO行业市场增长快速
有分析数据显示,2015年至2021年,全球CRO市场规模将从318.5亿美元增长到645.8亿美元,预计年复合增长率为12.8%,并且将较长一段时间内保持较快的增长势头。目前,国外主要的CRO企业包括昆泰、科文斯、百瑞精鼎、SyneosHealth、PPD及PRAHealthSciences等。而这些企业营业收入规模普遍超过20亿美元,规模较大的昆泰营业收入甚至超过100亿美元。
实际上,当前全球CRO产业有逐渐向中国转移的趋势,尤其在是临床前研究方面。加上中国的医药行业的需求增长快于全球,并且在政策驱动下创新药正在成为众多企业转型的重要方向的大环境下,我国CRO市场也将保持高速增长。有预测,国内CRO行业规模从2012年的33.3亿美元,上升至2021年的283.1亿美元。当下中国本土CRO企业中,药明康德、康龙化成、泰格医药、睿智化学、昭衍新药等规模居前。
原料药需求将快速增长
过去在原料药市场中,发达国家以生产专利药为主要的盈利增长点,此种模式在未来的发展中仍会持续。不过要注意到,在未来20年内,全球药品专利将大规模到期,专利新药上市的速度减缓、品种下降;而且各个国家已经过了医疗支出野蛮增长的阶段,很多国家开始控制医疗及医保支出,降低药品成本,这将大力推进仿制药市场的发展,同时带动仿制药在全球的药品市场中的份额不断提升,推动全球仿制原料药需求的快速增长。而我国作为原料药进出口大国,在这种情况下会迎来非常好的发展机遇。

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询


















![趋势研判!2026年中国无人配送车行业政策、产业链、成本、市场规模、竞争格局及发展趋势:末端物流市场需求持续旺盛,派送场景不断开发,前景良好[图]](http://img.chyxx.com/images/2022/0408/54b870b64f647f1fc10474b02796382c9242dcfa.png?x-oss-process=style/w320)
![研判2026!中国海运行业货运量、运价、重点企业运力分析:中国海洋货运量稳健增长凸显核心引擎地位,港口能效升级护航贸易流通[图]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)
![研判2026!中国高压避雷器行业相关政策汇总、产业链、供需现状、竞争格局及未来发展趋势分析:供需两端均呈现高景气态势[图]](http://img.chyxx.com/images/2022/0330/4279f04d08c7260a105d321a303d34a91af3a3d5.png?x-oss-process=style/w320)
![研判2026!中国智慧城市轨道交通行业政策、产业链、市场规模、竞争格局及发展前景:智慧城市轨道交通市场规模达698.36亿元,技术融合驱动行业快速发展[图]](http://img.chyxx.com/images/2022/0330/920e1a3ff3bb6b7f469fbaa1e9ad45bc470a7578.png?x-oss-process=style/w320)
![趋势研判!2026年中国软件外包行业发展环境、产业链、市场规模、代表企业及未来趋势:受益于数字化转型需求增长,软件外包市场规模达6165.98亿元[图]](http://img.chyxx.com/images/2022/0330/83e55e0fd01cd7eb3b56b758f35281ec8d2514ab.png?x-oss-process=style/w320)
![2026年中国人工智能基础层行业产业链、发展现状、竞争格局、发展趋势研判:行业市场规模持续上涨,全栈自主可控进程持续深化[图]](http://img.chyxx.com/images/2022/0330/d1363a7ee3953fc25ed09e0b79158acce9dc7c22.png?x-oss-process=style/w320)
