2019年是“4+7带量采购”出台后的第一年,据《医药经济报》报道:首批带量采购的执行超预期。11个试点城市从3月开始陆续启动带量采购,平均药品降幅52%,最高降幅96%,截至6月完成约定采购总量的70%。
带量采购药品降幅较大
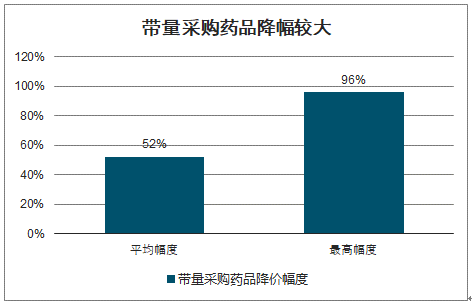
数据来源:公开资料整理
智研咨询发布的《2020-2026年中国创新药行业市场现状调研及投资机会预测报告》数据显示:在仿制药大幅降价的大背景下,利润空间压缩,促使企业转型。而之前布局创新药的企业产品正在逐步落地,进入回报期。而已经有创新药产品或相关业务布局的公司,预计将有较好的竞争力和增长潜力。
2017年10月8日,国务院办公厅发表《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,以改善中国医药市场的监管制度,旨在加快药物在中国的开发及批核过程,并鼓励药物及医疗器械业内的创新。
医药产业政策支持创新医药发展
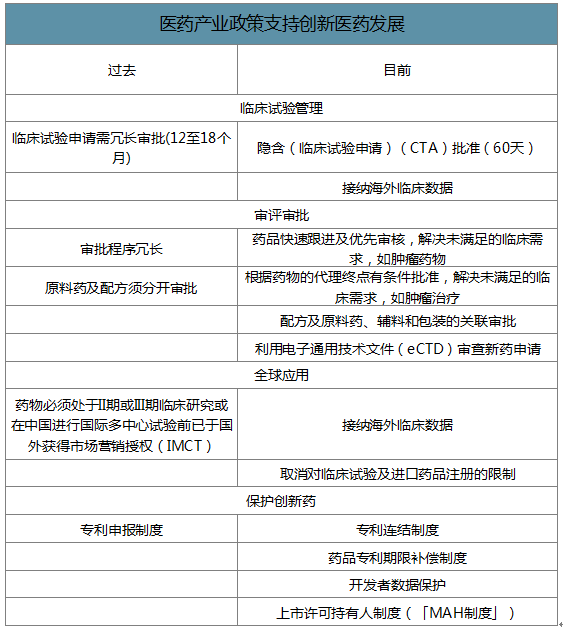
数据来源:公开资料整理
中国药品审批流程的转变

数据来源:公开资料整理
2019年,美国FDA的药物评估与研究中心(CDER)批准了48款创新药,其中包括9款生物类似药,5款罕见病药物,生物制品评估与研究中心(CBER)批准了诺华公司的基因疗法Zolgensma和首款登革热疫苗及多款伴随诊断产品。。我们认为,有5款新药成为2019年FDA批准药物的亮点。分别是:①全身性基因疗法Zolgensma;②RNAi疗法Givlaari;③不限癌种基于生物标志物的肿瘤靶向药Rozlytrek;④首个获美国FDA批准的中国原研抗癌药泽布替尼;⑤新一代HER2-ADC药物Enhertu。
2010-2019年美国FDA批准的新药数量
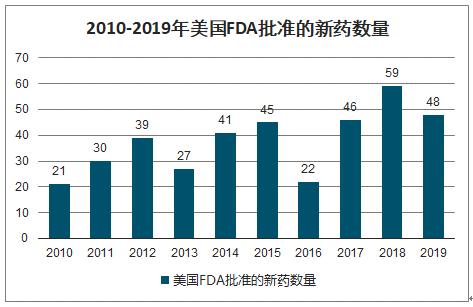
数据来源:公开资料整理
2019年,我国NMPA批准5个国产重磅新药,3个国产生物类似药,2个国产疫苗,6个进口重磅新药。国产重磅新药包括包括翰森制药的聚乙二醇洛塞那肽、氟马替尼,恒瑞医药的卡瑞利珠单抗、瑞马唑仑,百济神州的替雷利珠单抗。国产生物类似药包括2个阿达木单抗类似药和1个贝伐珠单抗生物类似药。
2019年NMPA批准的重磅品种

数据来源:公开资料整理
2019年获批创新医疗器械名单
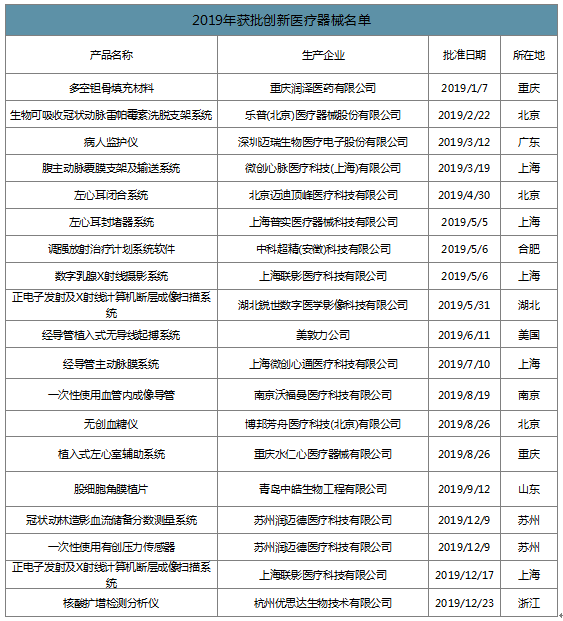
数据来源:公开资料整理
龙头公司中,乐普医疗、迈瑞医疗、联影医疗及微创医疗子公司均有产品获批,市场竞争力有望进一步增强;此外部分企业有望通过创新产品放量抵御集采对业绩的影响。
2019年获批产品所属上市公司名单
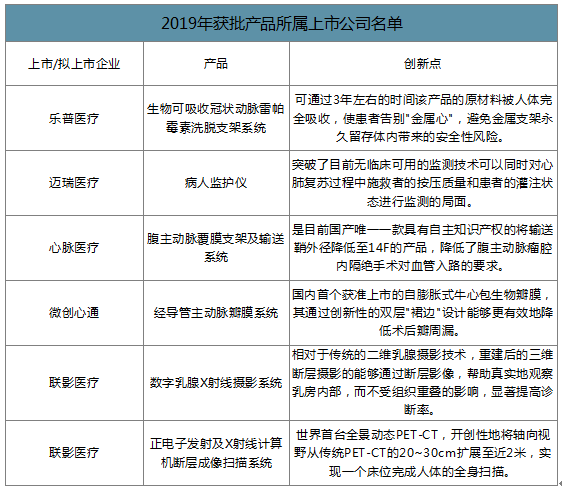
数据来源:公开资料整理
中国创新药市场空间测算
2018年中国创新药(以化药、生物药为主)销售额占所有药物比例约为2.5%,占非中药比例为4.17%,远低于美国和日本的水平。我们预计到2024年,中国创新药销售额占非中药的比例有望达到10%,2029年有望达到30%。创新药销售额有望达到7000亿元以上,年复合增速近30%。
中国各类药品销售额预测(单位:亿元)
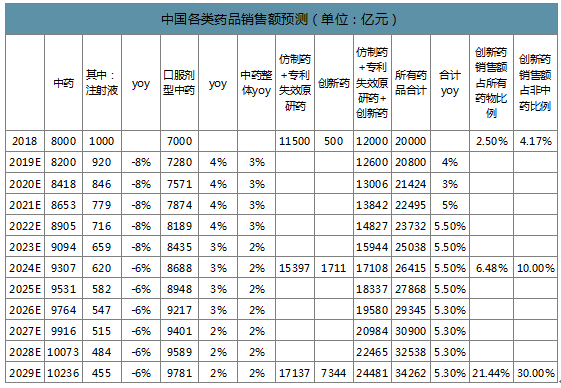
数据来源:公开资料整理

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询


















![趋势研判!2026年中国无人配送车行业政策、产业链、成本、市场规模、竞争格局及发展趋势:末端物流市场需求持续旺盛,派送场景不断开发,前景良好[图]](http://img.chyxx.com/images/2022/0408/54b870b64f647f1fc10474b02796382c9242dcfa.png?x-oss-process=style/w320)
![研判2026!中国海运行业货运量、运价、重点企业运力分析:中国海洋货运量稳健增长凸显核心引擎地位,港口能效升级护航贸易流通[图]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)
![研判2026!中国高压避雷器行业相关政策汇总、产业链、供需现状、竞争格局及未来发展趋势分析:供需两端均呈现高景气态势[图]](http://img.chyxx.com/images/2022/0330/4279f04d08c7260a105d321a303d34a91af3a3d5.png?x-oss-process=style/w320)
![研判2026!中国智慧城市轨道交通行业政策、产业链、市场规模、竞争格局及发展前景:智慧城市轨道交通市场规模达698.36亿元,技术融合驱动行业快速发展[图]](http://img.chyxx.com/images/2022/0330/920e1a3ff3bb6b7f469fbaa1e9ad45bc470a7578.png?x-oss-process=style/w320)
![趋势研判!2026年中国软件外包行业发展环境、产业链、市场规模、代表企业及未来趋势:受益于数字化转型需求增长,软件外包市场规模达6165.98亿元[图]](http://img.chyxx.com/images/2022/0330/83e55e0fd01cd7eb3b56b758f35281ec8d2514ab.png?x-oss-process=style/w320)
![2026年中国人工智能基础层行业产业链、发展现状、竞争格局、发展趋势研判:行业市场规模持续上涨,全栈自主可控进程持续深化[图]](http://img.chyxx.com/images/2022/0330/d1363a7ee3953fc25ed09e0b79158acce9dc7c22.png?x-oss-process=style/w320)
