宫颈癌是致死率仅次于卵巢癌的女性生殖道恶性肿瘤,我国妇女患宫颈癌的比例为15/10万,是仅次于智利的全球第二大宫颈癌高发国家。全球每年新发病例接近60万人,死亡约30万人。目前国内患者约40万人,每年新增14万人,居女性生殖道肿瘤首位。我国的宫颈癌死亡率为11.34%,在西部地区,宫颈癌居女性癌症死亡率之首。人乳头状瘤病毒(HPV)与宫颈癌之间具有高相关性。1995年国际癌症研究协会(IARC)认定HPV感染是导致宫颈癌的主要原因,临床证明,几乎所有(99.7%)的宫颈癌都是HPV感染所引起,HPV感染不仅仅导致宫颈癌,85-90%的肛门癌、70-75%的阴道癌、30%的外阴癌也与HPV感染密切相关。
HPV感染导致宫颈癌机理示意图

数据来源:公开资料整理
全球HPV16/18感染率情况
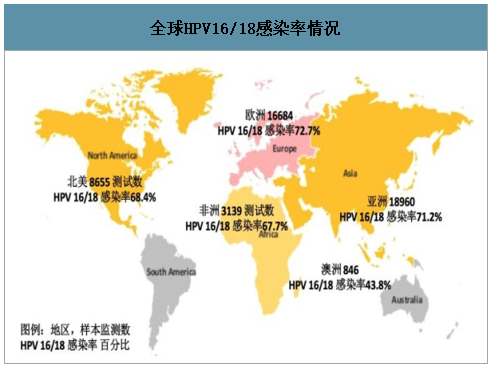
数据来源:公开资料整理
智研咨询发布的《2020-2026年中国HPV疫苗行业竞争格局及经营模式分析报告》数据显示:宫颈癌是致死率仅次于卵巢癌的女性生殖道恶性肿瘤,我国妇女患宫颈癌的比例15/10万。全球每年新发病例接近60万,死亡约30万。我国患者约40万,每年新增14万,居女性生殖道肿瘤首位。我国的宫颈癌死亡率高达11.34%。人乳头状瘤病毒(HPV)与宫颈癌之间具有高相关性。1995年国际癌症研究协会(IARC)认定HPV感染是导致宫颈癌的主要原因,临床证明,几乎所有(99.7%)的宫颈癌都是HPV感染所引起,HPV感染不仅仅导致宫颈癌,84%的肛门癌、77%的阴道癌、40%的外阴癌与HPV感染密切相关。
HPV感染非常普遍,有性生活的妇女一生中感染过一种HPV的可能性高达40%-80%。但是超过80%的HPV感染8个月内会自然清除,感染了HPV并不一定会发展成宫颈癌。HPV有100多种亚型,分为低危型和高危型,只有高危型HPV的持续感染,才会进展为恶性病变。HPV16和18是最主要的高危型HPV,70%的宫颈癌都是由这两型HPV导致的,31、33、45、52与58等其他高危亚型可导致另外20%左右的宫颈癌。另外,6、11低危亚型主要与肛门癌与生殖器疣相关。因此,只要预防高危型HPV的持续感染,就能很大程度上预防宫颈癌。HPV疫苗是全球第一个预防肿瘤的疫苗,预防效果显著且安全。2价(16/18型)与4价(6/11/16/18型),9价(6/11/16/18/31/33/45/52/58型)HPV疫苗分别对70%、92%左右的宫颈癌有显著预防效果,另外4价与9价HPV疫苗由于覆盖6、11两个低危亚型,可以预防男性和女性的肛门癌以及生殖器疣。目前有79个国家将HPV疫苗列为国家免疫规划项目。
国外获批上市的HPV疫苗对比
国外获批上市的HPV疫苗对比 | |||
商品名 | Cervarix | Gardasil | Gardasil9 |
首次上市时间 | 2007年9月 | 2006年6月 | 2014年12月 |
国内上市时间 | 2016年7月 | 2017年5月 | 2018年4月 |
生产商 | 葛兰素史克 | 默沙东 | 默沙东 |
覆盖亚型 | 16/18 | 6/11/16/18 | 6/11/16/18/31/33/45/52/58 |
宫颈癌覆盖率 | 70% | 70% | 92% |
国内获批接种人群 | 9-45岁女性 | 20-45岁女性 | 16-26岁女性 |
国内中标价格 | 580元/支 | 798元/支 | 1298元/支 |
数据来源:公开资料整理
自HPV疫苗上市以来,众多国际临床试验对HPV疫苗的有效性及安全性进行了系统评估,并普遍认为HPV疫苗安全有效。其中,一项九价HPV疫苗与四价HPV疫苗的非劣效试验表明,四价和九价HPV疫苗的血清阳转率均接近100%,抗体应答水平是自然感染的数倍。HPV疫苗对未感染个体的保护率更高,但依旧能够为既往感染者的其他未感染亚型提供保护。
16-26岁女性接种四价或九价HPV疫苗后的血清阳性率和几何平均效价
16-26岁女性接种四价或九价HPV疫苗后的血清阳性率和几何平均效价 | ||||||
检测指标 | 九价HPV | 四价HPV | ||||
受试者数量 | 血清阳性率(%) | 几何平均效价(mMU/mL) | 受试者数量 | 血清阳性率(%) | 几何平均效价(mMU/mL) | |
抗HPV6 | 3,993 | 99.8 | 893 | 3,975 | 99.8 | 875 |
抗HPV11 | 3,995 | 100 | 666 | 3,982 | 99.9 | 830 |
抗HPV16 | 4,032 | 100 | 3,131 | 4,062 | 100 | 3,157 |
抗HPV18 | 4,539 | 99.8 | 805 | 4,541 | 99.7 | 679 |
数据来源:公开资料整理
截止2018年1月26日,全球共有79个国家将HPV疫苗纳入国家免疫规划,相较于2017年增加11个国家,多为经济发达的国家与地区。考虑到HPV疫苗较高的卫生经济学价值,我们预计,未来将会有更多的国家或地区将其纳入国家免疫规划。
HPV疫苗纳入国家免疫规划情况(截至18年1月26日)
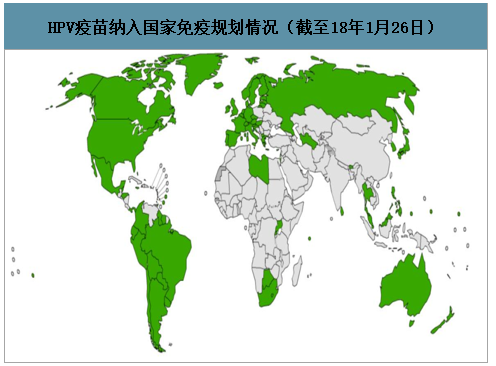
数据来源:公开资料整理
美国是全球最早将HPV纳入国家免疫规划的国家,其于2007年正式将HPV疫苗纳入国家免疫规划,2010年将推荐人群由11-12岁女性拓展至所有11-12岁青少年,并一直致力于18-26岁成年人群的HPV疫苗补种。由于美国将HPV疫苗纳入国家免疫规划且由多种商业医疗保险覆盖,因此HPV疫苗接种率较高。2017年美国13-17岁青少年中,女性和男性至少接种1剂HPV疫苗的比例分别为68.6%和62.6%,19-26岁成年人群中,女性和男性至少接种1剂HPV疫苗的比例分别为51.5%和21.2%,上升趋势明显。
全球已上市的HPV疫苗主要有葛兰素史克的2价疫苗Cervarix以及默沙东的4价与9价疫苗Gardasil、Gardasil9,近年均在国内上市。由于国内外临床开展情况略有不同,所获批接种年龄区间、性别人群以及常规接种程序有所不同。GSK的二价HPV疫苗Cervarix受默沙东四价和九价HPV疫苗Gardasil冲击影响,2016年10月开始退出美国市场。而默沙东的Gardasil最近几年持续保持增长,特别是2018年受益于其男性适应症拓展和中国市场带动,销售额达到31.51亿美元,实现了36.5%大幅增长。
全球4/9价HPV疫苗销售额
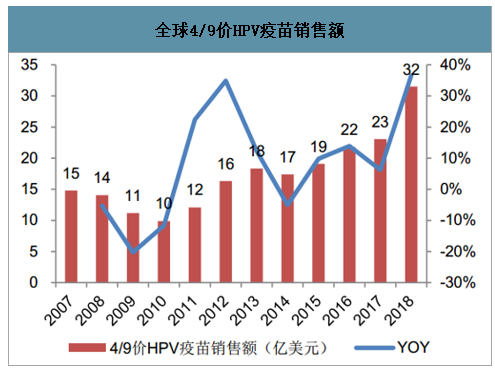
数据来源:公开资料整理
全球2价HPV疫苗销售额

数据来源:公开资料整理
1)1-3月:整体批签发量同比增长41%,单月无批签发,4价苗份额大幅提升
目前我国已上市HPV疫苗产品有主要有3种,分别是9价HPV(默沙东)、4价HPV(默沙东)、2价HPV(葛兰素史克),厦门万泰国产HPV疫苗近期获批;HPV疫苗整体批签发量呈现上升趋势,批签发数量由2017年的145.5万支增长到2019年的1111.4万支,CAGR达到97%。2020年1-3月实现批签发223.4万支,同比增长78%,HPV疫苗仍处于快速放量阶段,终端供不应求,国产2价HPV获批有望带动增速提高;
9价HPV:主要应用于16-26岁人群,由默沙东生产。批签发量呈现上升趋势,2020年1-3月实现批签发41.4万支,维持快速放量;4价HPV:主要应用于20-45岁人群,由默沙东生产。批签发量呈现上升趋势,批签发数量由2017年的34.8万支增长到2019年的554.3万支,CAGR为152%。2020年1-3月实现批签发182万支,同比增长45%,维持快速放量。市场份额;2价HPV:主要应用于9-45岁人群,由葛兰素史克生产。批签发量呈现上升趋势,批签发数量由2017年的110.7万支增长到2019年的200.8万支,CAGR为22%。2020年1-3月累计无批签发;
宫颈癌疫苗2011年以来批签发量
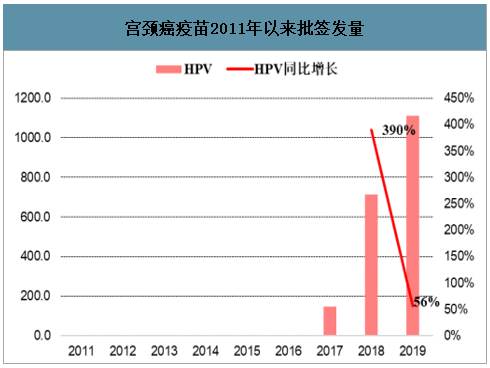
数据来源:公开资料整理
宫颈癌疫苗近年1-3月累计批签发量
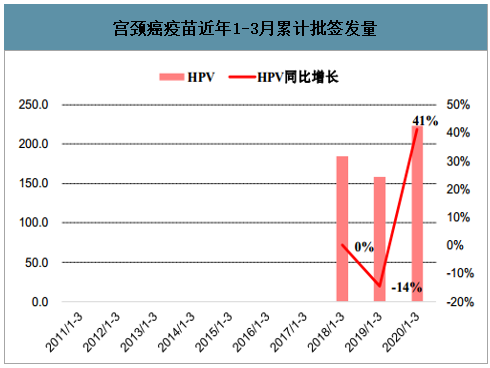
数据来源:公开资料整理
宫颈癌疫苗竞争格局
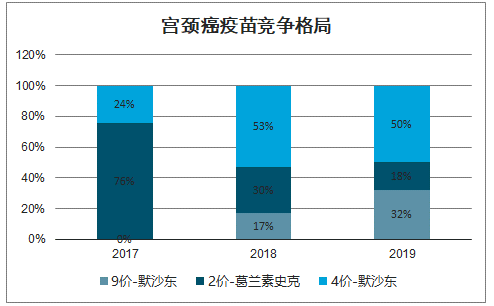
数据来源:公开资料整理
宫颈癌疫苗2020年1-3月累计批签发竞争格局
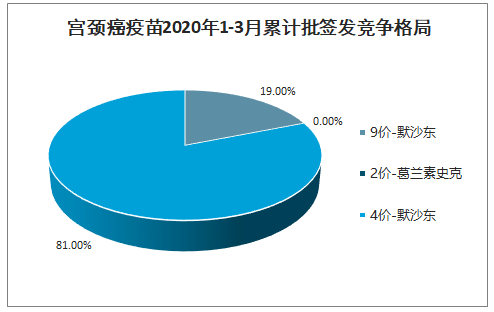
数据来源:公开资料整理
国内企业仅有万泰生物的2价HPV已获批上市,沃森生物的2价HPV疫苗即将申报生产。国内其他企业在研产品均以2价HPV为主,4价和9价HPV疫苗都还在临床试验阶段。智飞生物代理的4价和9价HPV疫苗在未来几年均为市场独家品种。
我国HPV疫苗研发进度
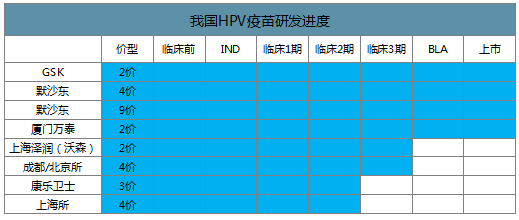
数据来源:公开资料整理
2)国内HPV疫苗存量市场空间广阔
HPV疫苗存量市场巨大,每年增量显著。我们测算HPV疫苗存量市场高达852亿元,假设5年完成消化,每年对应市场规模170亿元,每年增量市场规模44亿元,每年增量+存量市场空间合计214亿元,其中4价和9价市场空间高达179亿元。
HPV疫苗存量市场空间测算
16-26岁女性接种四价或九价HPV疫苗后的血清阳性率和几何平均效价 | ||||||
检测指标 | 九价HPV | 四价HPV | ||||
受试者数量 | 血清阳性率(%) | 几何平均效价(mMU/mL) | 受试者数量 | 血清阳性率(%) | 几何平均效价(mMU/mL) | |
抗HPV6 | 3,993 | 99.8 | 893 | 3,975 | 99.8 | 875 |
抗HPV11 | 3,995 | 100 | 666 | 3,982 | 99.9 | 830 |
抗HPV16 | 4,032 | 100 | 3,131 | 4,062 | 100 | 3,157 |
抗HPV18 | 4,539 | 99.8 | 805 | 4,541 | 99.7 | 679 |
数据来源:公开资料整理
HPV疫苗增量市场空间测算
HPV疫苗增量市场空间测算 | |||
人数(万人) | 750 | ||
渗透率 | 20% | ||
苗种 | HPV2 | HPV4 | HPV9 |
份额 | 20% | 30% | 50% |
价格(元/人) | 1200 | 2394 | 3894 |
市场空间(亿元) | 4 | 11 | 29 |
增量市场合计(亿元) | 44 | ||
数据来源:公开资料整理
3)高价HPV疫苗市场竞争格局良好
目前我国尚没有国产HPV疫苗上市,但国内企业的HPV疫苗研发热情高涨,国内进入临床申报及以后阶段的HPV疫苗研发项目多达24项。按疫苗价位划分,在研疫苗包括单价、二价、三价、四价、六价、九价、11价、14价及治疗性HPV疫苗。从研发进度来看,进入上市申报阶段的只有万泰沧海的二价HPV疫苗,预计有望2019年底2020年初获批上市;进入III期临床的有泽润生物(沃森生物子公司)的二价HPV疫苗及成都所的四价HPV疫苗;进入II期临床的有万泰沧海的二价HPV疫苗(6/11型)、康乐卫士的三价HPV疫苗、上海所的四价HPV疫苗及万泰沧海的九价HPV疫苗。
我国HPV疫苗研发进度情况
我国HPV疫苗研发进度情况 | |||||
分类 | 药品名称 | 受理号 | 企业名称 | 办理状态 | 状态开始日 |
2价HPV疫苗 | 单价HPV疫苗重组16型人乳头瘤病毒疫苗(大肠杆菌) | CXSL0600071 | 迪沙麦特 | 获批临床 | 2008年10月 |
重组人乳头瘤病毒16/18型双价疫苗(大肠杆菌) | CXSS1700036 | 万泰沧海 | 申请上市 | 2018年3月 | |
重组(大肠杆菌)人乳头瘤病毒6/11型双价疫苗 | CXSL0900046 | 万泰沧海 | II期临床 | 2016年3月 | |
重组人乳头瘤病毒16/18型二价疫苗(汉逊酵母) | CXSL1500069 | 瑞科生物 | I期临床 | 2019年1月 | |
重组人乳头瘤病毒6/11型二价疫苗(汉逊酵母) | CXSL1600042 | 瑞科生物 | 获批临床 | 2018年6月 | |
重组(大肠杆菌)人乳头瘤病毒16/18型双价疫苗 | CXSL0700015 | 厦门大学 | 获批临床 | 2010年3月 | |
重组人乳头瘤病毒双价(16/18型)疫苗(酵母) | CXSL0900008 | 泽润生物 | 获批临床 | 2011年6月 | |
重组(毕赤酵母)人乳头瘤病毒双价(16/18型)疫苗 | CXSL1500086 | 健康元 | 获批临床 | 2017年3月 | |
3价HPV疫苗 | 重组三价人乳头瘤病毒(16/18/58型)疫苗(大肠杆菌) | CXSL1500033 | 康乐卫士 | II期临床 | 2018年4月 |
4价HPV疫苗 | 四价重组人乳头瘤病毒疫苗(6/11/16/18型)(汉逊酵母) | CXSL1300106 | 成都所 | III期临床 | 2018年1月 |
重组四价人乳头瘤病毒(16/18/52/58型)病毒样颗粒疫苗(毕赤酵母) | CXSL1400135 | 上海所 | II期临床 | 2019年3月 | |
四价重组人乳头瘤病毒(6/11/16/18型)疫苗(汉逊酵母) | CXSL1400144 | 博唯生物 | I期临床 | 2016年12月 | |
四价重组(大肠杆菌)16/18/52/58型人乳头瘤病毒类病毒颗粒疫苗 | CXSL1700115 | 双鹭药业 | 申报临床 | 2018年3月 | |
6价HPV疫苗 | 六价重组人乳头瘤病毒疫苗(6/11/16/18/52/58型)(汉逊酵母) | CXSL1400044 | 成都所 | 申报临床 | 2014年7月 |
9价HPV疫苗 | 重组人乳头瘤病毒6/11/16/18/31/33/45/52/58型九价疫苗(大肠埃希菌) | CXSL1500061 | 万泰沧海 | II期临床 | 2019年5月 |
重组人乳头瘤病毒(6/11/16/18/31/33/45/52/58型)九价疫苗(汉逊酵母) | CXSL1600087 | 博唯生物 | I期临床 | 2018年9月 | |
重组人乳头瘤病毒6/11/16/18/31/33/45/52/58型九价疫苗(汉逊酵母) | CXSL1700214 | 瑞科生物 | I期临床 | 2019年1月 | |
重组人乳头瘤病毒九价病毒样颗粒疫苗(6/11/16/18/31/33/45/52/58型L1蛋白)(毕赤酵母) | CXSL1600090 | 泽润生物 | I期临床 | 2019年3月 | |
重组九价人乳头瘤病毒(6/11/16/18/31/33/45/52/58型)疫苗(大肠埃希菌) | CXSL1700219 | 康乐卫士 | 获批临床 | 2018年10月 | |
11价HPV疫苗 | 11价重组人乳头瘤病毒疫苗(汉逊酵母) | CXSL1800033 | 中生生物 | 申报临床 | 2018年4月 |
14价HPV疫苗 | 重组十四价人乳头瘤病毒疫苗(6/11/16/18/31/33/35/39/45/51/52/56/58/59型)(昆虫细胞) | CXSL1800003 | 诺宁生物 | 申报临床 | 2018年1月 |
治疗性 | 治疗用人乳头瘤病毒16型重组蛋白疫苗 | CXSL1200006 | 普康生物 | 获批临床 | 2015年1月 |
治疗用重组人乳头瘤病毒16型E7融合蛋白疫苗 | CXSL1200076 | 泽润安珂 | 终止研究 | 2019年8月 | |
治疗用人乳头瘤病毒16型重组腺病毒载体疫苗 | CXSL1300046 | 普康生物 | 获批临床 | 2017年11月 | |
数据来源:公开资料整理
 智研咨询 - 精品报告
智研咨询 - 精品报告

2026-2032年中国HPV疫苗行业市场供需态势及发展前景研判报告
《2026-2032年中国HPV疫苗行业市场供需态势及发展前景研判报告》共十章,包含2021-2025年HPV疫苗行业投资现状分析,2026-2032年HPV疫苗行业投资机会与风险防范,研究结论及投资建议等内容。

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询



















![2022年中国宫颈癌(HPV)疫苗行业运行现状及竞争格局分析,智飞生物九价HPV疫苗批签发量为9298758支[图]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)

