2004年以来,我国逐步完善批签发制度,2005年《疫苗流通和预防接种管理条例》颁布,作为国家监管疫苗的框架性文件,为我国疫苗行业的规范发展贡献了重要作用;2016年3月“山东疫苗事件”引发了社会强烈反响,2016年4月,国务院颁布实施修订后的《疫苗流通和预防接种管理条例》,其中提出了取消批发环节,由生产企业直接向县级疾控预防控制机构配送二类疫苗,即实施流通环节的一票制。2018“长生生物事件”再次引发公众对于疫苗安全的质疑,促成了疫苗法的出台,2019年7月,《中国人民共和国疫苗管理法》颁布,12月起开始实施,从立法的角度严格监管疫苗行业,疫苗行业迎来了前所未有的强监管时代。
我国疫苗监管相关政策

资料来源:智研咨询整理
2016年山东疫苗事件爆发,二类疫苗经历了大调整。2016年4月《疫苗流通和预防接种管理条例》修改后,删除了“关于药品批发企业经批准可以经营疫苗”取消其经营资质;同时将疫苗采购全部纳入省级公共资源交易平台,由县级疾控机构向疫苗生产企业、疫苗进口单位直接购买后供应给行政区域的接种单位。即流通形式由之前经销制变为“一票制”,生产企业需要变经销为直销,而流通小经销商则需要转经销为专业的推广服务商。
新的《生物制品批签发管理办法》于2017年12月29日公布,自2018年2月1日起施行。相较于2004年《办法》,新《办法》共八章,共计49条,比现行《办法》增加了12条。主要修改内容包括:一是进一步细化了批签发工作流程。二是进一步明确了批签发相关单位职责。三是进一步强化了批签发申请人的主体责任。四是进一步明确了批签发工作时限要求。五是进一步强化了批签发机构管理。六是进一步增强了批签发工作的透明度。国家药监局2019年11月公布了《生物制品批签发管理办法(修订草案征求意见稿)》,《办法》未进行大幅度调整;根据新制修订的《药品管理法》和《疫苗管理法》重点条款要求,逐项进行对照落实,对相关内容进行补充完善。同全球其他疫苗生产国相比,我国疫苗批签发具有企业数量多、疫苗品种多、签发批次多、受众人群多等特点,批签发任务十分繁重,2017年,申请签发的疫苗有50个品种,达到4404批,其中4388批(约计7.12亿人份)符合规定,16批(约计80.68万人份)不符合规定,不通过率为0.36%。
从我国目前疫苗的整体结构看,存在较为明显的优化空间,目前我国以疫苗批号企业主体(不考虑母子公司、关联企业的情况)超过40家,其中只有1个品种批号的企业多达22家,1-2个品种合计达到32家,超过5个品种的企业只有10家,剔除中生集团下属的6大所,超过5个品种批号的企业只有4家。因此未来行业优势劣汰,国内优质规范龙头企业国企及骨干型民企以及创新型疫苗企业有望胜出,未来稀缺性进一步凸显。
我国疫苗企业大多只有一个品种,结构待优化
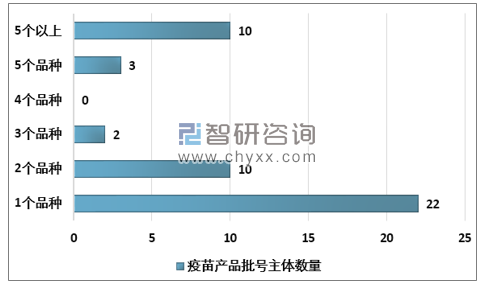
资料来源:智研咨询整理
智研咨询发布的《2020-2026年中国疫苗行业市场全面调研及竞争格局预测报告》显示:中国疫苗市场近年来发展迅速,国内疫苗市场总规模由2014年233亿元增长至2019年373亿元,预计到2030年达到1161亿元,年复合增长率达到10.9%,体现出疫苗行业的强劲增长势头。新冠疫情的全民教育,有助于居民健康接种意识的提升,推动行业的持续扩容。
2014-2019年中国疫苗市场规模
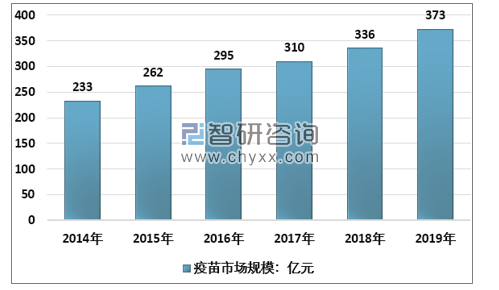
资料来源:智研咨询整理
从我国目前疫苗的消费品种结构和全球十大疫苗品种相比有很大的差异,海外主流的疫苗大品种如13价肺炎疫苗、HPV疫苗、带状疱疹疫苗等在我国量还相对较小,另外其他品种如百白破-乙肝-灭活机会联合疫苗等在国内还未有品种上市,未来我国疫苗市场高价值大品种疫苗有很大的发展空间。而随着国内企业的持续研发积累,国产大疫苗品种如13价肺炎疫苗、HPV疫苗等逐步上市,开启国产疫苗大品种新时代。
从我国和全球疫苗消费品种看我国还有很大的大品种增长空间
2019年 | 国内十大 | 批签发(万剂) | 全球十大 | 销售额(亿 美元) |
1 | 吸附无细胞百白破联合疫苗 | 7442.78 | Prevnar13/Prevenar13(13价肺炎结合疫苗) | 58.47 |
2 | 乙肝疫苗 | 6237.71 | Gardasil(四价HPV疫苗)/Gardasil9(九价HPV疫苗) | 37.37 |
3 | 人血白蛋白 | 5426.88 | Shingrix(带状疱疹疫苗) | 24.00 |
4 | 冻干人用狂犬病疫苗 | 4807.28 | ProQuad/MMRII/Varivax(麻腮风水痘疫苗) | 22.75 |
5 | 脊髓灰质炎疫苗 | 4522.77 | Polio/Pertussis/HibVaccines(包括百白破/脊髓灰质炎/Hib/乙肝疫苗) | 21.82 |
6 | A群C群脑膜炎球菌多糖疫苗 | 4392.23 | InfluenzaVaccines(包括三价和四价) | 21.20 |
7 | 乙型脑炎减毒活疫苗 | 4256.63 | Hepatitis(肝炎疫苗) | 11.59 |
8 | 麻腮风联合减毒活疫苗 | 2442.93 | Infanrix(百白破),Pediarix(百白破乙肝脊灰疫苗) | 9.72 |
9 | 水痘减毒活疫苗 | 2102.49 | Pneumovax23(23价肺炎多糖疫苗) | 9.26 |
10 | 肠道病毒71型灭活疫苗 | 1885.05 | Bexsero(B型脑膜炎疫苗) | 9.00 |
资料来源:智研咨询整理
13价肺炎疫苗:国内目前仅有辉瑞一家上市,2019年批签发量475.5万剂,仅够119万新生儿童使用,沃森产品国内首家上市后将打破进口依赖。13价增量市场空间可超70亿元,若考虑5岁以下存量儿童,市场规模有望进一步到100亿元。
2011-2019年我国肺炎疫苗年度批签发数据(万支)
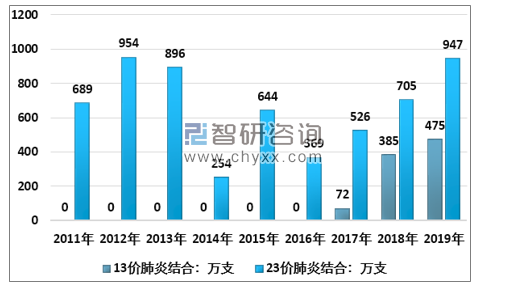
资料来源:中检院
HPV疫苗:默沙东的九价和四价HPV疫苗、GSK二价苗在售,厦门万泰二价HPV2019年底获批上市。MSD的四价HPV2019年全年批签发532万剂,同比+40%;九价HPV2019年批签发达到332万剂,同比增速173%;GSK2019年批签发201万剂,同比下滑5%。HPV疫苗市场空间可达1000亿元级别,市场潜力可观。
2017-2019年我国HPV疫苗批签发量(万支)
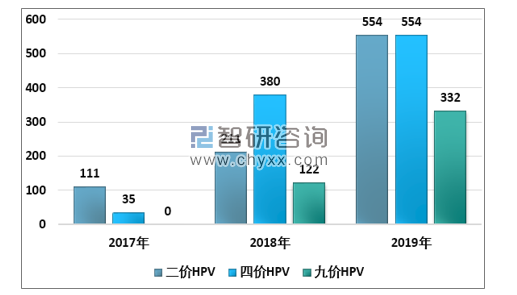
资料来源:中检院
多联苗:1)智飞生物的AC-Hib疫苗销售额在10亿元级别,公司再注册于2020年2月最终未通过,公司正加紧开发AC-Hib疫苗冻干剂型,后续有望上市接替旧有水剂。2)DTap/Hib四联苗为康泰生物独家产品,2014年以来批签发逐年增加,2018年借助赛诺菲巴斯德五联苗短暂退出市场的契机,公司加快渠道布局,补足市场缺口,全年批签发515万件,同比+261%,2019年阶段性去库存,共批签发426万件,同比-17%,批签发货值超10亿元。3)Dtap-IPV/Hib五联苗是全球疫苗大品种,根据赛诺菲巴斯德年报,其2019联苗系列销售额达到19.46亿欧元,体现出强劲的终端需求,未来国内市场可拓展空间大。
2011-2019年我国多联苗批签发量(万支)
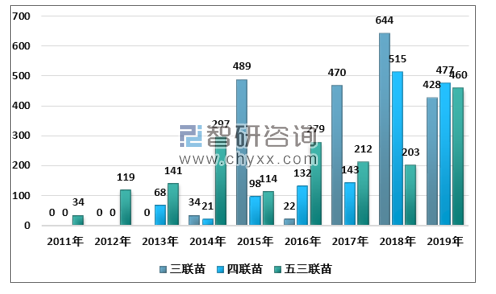
资料来源:中检院
流感疫苗:2019年流感规模较大,两种疫苗总批签发量3078万剂,同比大幅增加91%,其中四价流感疫苗批签发971万件,同比+90%,四价苗占整体比例为31.5%,我国流感疫苗渗透率低,若整体接种率提升至10%,则市场潜力可超100亿元。
2011-2019年我国流感疫苗批签发量(万支)
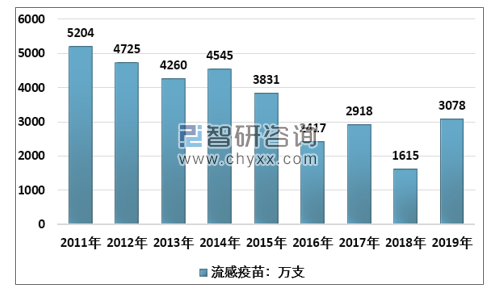
资料来源:中检院
人用狂犬病疫苗:2019年批签发5566万件,批签发货值达到36亿元,随着宠物的持续增长,带来的抓伤咬伤事件将继续增长,人用狂犬疫苗市场有望实现持续增长。
2011-2019年我国狂犬疫苗批签发量(万支)
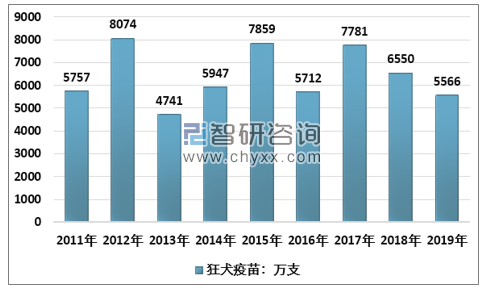
资料来源:中检院
麻腮风疫苗/水痘疫苗:麻腮风全年共计2443万剂,预计后续作为免疫规划重要品种,批签发有望迎来明显增长。水痘减毒活疫苗:自2014年以来逐年增长,2019年批签发2102万件,增幅较2018年有所下降,主要是长春生物痘苗退出市场。目前我国主要是MMR+V的方式存在,长远看假设麻腮风水痘联苗接种率50%,按照两针法,则销量潜力达到1000万剂,市场空间可达25亿元。
2011-2019年我国麻风腮疫苗批签发量(万支)
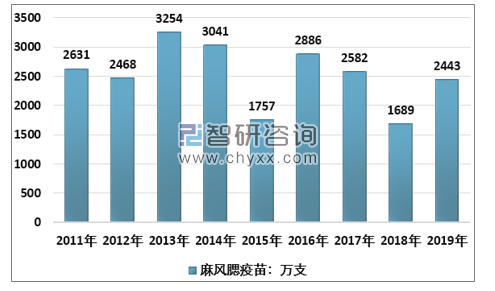
资料来源:中检院
2011-2019年我国水痘疫苗批签发量(万支)
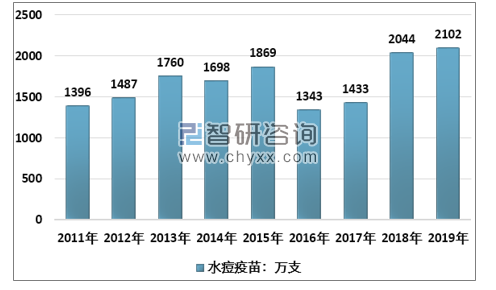
资料来源:中检院
五价轮状病毒疫苗:全球疫苗大品种,2018年在大陆上市,批签发持续增长,2019年批签发470万件,同比+485%。假设最终渗透率达到25%,则对应年峰值销售额可达到31.5亿元。
2011-2019年我国轮状病毒疫苗批签发量(万支)

资料来源:中检院
传统企业的技术路径大多是灭活、减毒和重组技术,应用相对成熟,近年来兴起的病毒载体、核酸疫苗等新技术平台为疫苗创新创造了新的方向,不同的技术路径各有特点,在新冠疫情下,疫苗研发备受市场关注,挑战与机遇并存,针对新冠肺炎的疫苗研发,传统路径和新疫苗路径均在同步展开,企业迎来了良好的新技术布局时点,当前时点是行业新技术储备的机会,有利于奠定长期发展。
不同疫苗技术路径各有特点
类型 | 原理 | 优点 | 缺点 |
灭活疫苗 | 将病原体灭活,使其传染因子被破坏而仍保留免疫原性 | 安全性好;运输稳定,甚至不需要冷藏 | 免疫反应持续时间较短,需多次免疫 |
减毒疫苗 | 病原体经过处理后,发生变异,毒性减弱或丧失,但仍保留免疫原性 | 产量高;免疫力持久 | 保存和运输条件要求高;安全性略差,存在毒性逆转风险 |
重组基因工程疫苗/亚单位疫苗 | 提取病原体免疫活性片段,刺激机体产生抗体 | 安全性好;稳定性好 | 免疫原性较低,通常需要佐剂配合使用 |
病毒载体疫苗 | 将抗原基因以无害的微生物作为载体进入体内诱导免疫应答 | 可有效诱导机体产生高效价的中和抗体,可诱导细胞免疫 | 机体易对宿主病毒产生免疫反应 |
核酸疫苗 | 将含有编码的蛋白基因序列的质粒载体导入体内,诱导免疫应答 | 制备简单;成本低;免疫力持久 | 可能诱导免疫反应;细胞内传递效果差;DNA疫苗存在染色体整合治癌风险,mRNA稳定性差 |
资料来源:智研咨询整理
我国消费潜力大,大疫苗品种具备良好的放量潜力:疫苗作为预防性的产品,药物经济学价值高,尤其是其使用人群具有特殊性(儿童、女性、老年人等),需求相对刚性,加之目前人们对于健康预防保健意识的持续提升,对消费类产品有更高的支出意愿,为高价值疫苗大品种销售放量奠定更为坚实的基础。
《疫苗法》第九十八条提出国家鼓励疫苗生产企业按照国际采购要求生产、出口疫苗。出口的疫苗应当符合进口国(地区)的标准或者合同要求。
我国已有四款疫苗通过WHO预认证,后续预计将有更多产品走出国门:截止目前,成都生物制品研究所生产的乙型脑炎减毒活疫苗、北京北生研生物公司生产的口服Ⅰ型Ⅲ型脊髓灰质炎疫苗、华兰生物公司生产的流感疫苗、北京科兴生物公司生产的甲型肝炎灭活疫苗等先后通过了世界卫生组织预认证,并被纳入联合国儿童基金会、全球疫苗免疫联盟采购计划,标志着中国疫苗走向世界,随着政策的鼓励,预计后续更多的国产疫苗有望走出国门,造福世界。
 智研咨询 - 精品报告
智研咨询 - 精品报告

2026-2032年中国多联多价疫苗行业市场现状调查及未来前景研判报告
《2026-2032年中国多联多价疫苗行业市场现状调查及未来前景研判报告》共九章,包含2021-2025年中国多联多价疫苗行业竞争格局分析,主要多联多价疫苗企业或品牌竞争分析,2026-2032年中国多联多价疫苗行业发展前景预测等内容。

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询



















![研判2025!中国疫苗行业产业链图谱、产业现状、重点企业及未来前景展望:产业规模日益扩容,本土企业国际化步伐加快[图]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)



