西达本胺,抗癌新药,中国自主知识产权,已经量产,广泛用于临床治疗。西达本胺是全球首个获准上市的亚型选择性组蛋白去乙酰化酶口服抑制剂,也是中国首个授权美国等发达国家专利使用的原创新药。
西达本胺是苯酰胺类 HDAC 亚型选择性抑制剂,能调控肿瘤异常表观遗传。通过抑制相关 HDAC 亚型以增加染色质组蛋白的乙酰化水平,进而引发染色质重塑,并由此导致针对肿瘤发生的多条信号传递通路基因表达的改变,也就是表观遗传改变。另外,西达本胺直接抑制肿瘤细胞周期,诱其凋亡;对调节机体抗肿瘤细胞免疫的活性;还有通过表观遗传调控机制,诱导肿瘤干细胞分化、逆转肿瘤细胞的上皮间充质表型转化(EMT)等功能,进而起到在抑制肿瘤转移、复发、耐药性等的作用。目前其适应症是外周 T细胞淋巴瘤,未来适应症可能延伸至非小细胞肺癌、乳腺癌和弥漫性大 B 细胞淋巴癌的治疗,目前正处于临床研究的不同阶段。
一、现状
西达本胺的销售收入从 2016 年 5,576 万元增长至 2018 年的 1.37 亿元,2018 年同比增长 47.52%;销量从 2016 年 13.05 万片增长至 2018 年的 44.64 万片,2018 年同比增长 71.76%。目前西达本胺的单价为7349.93 元/盒,进入医保后价格有所下降。
2016-2018年西达本胺销售额及增速
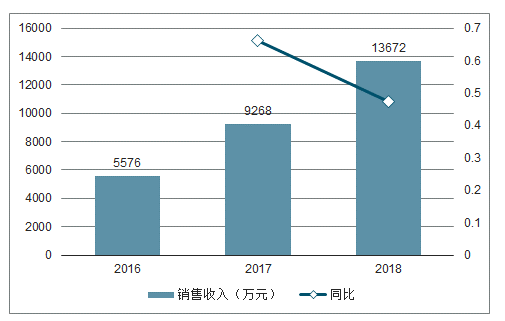
数据来源:公开资料整理
2016-2018年西达本胺销量
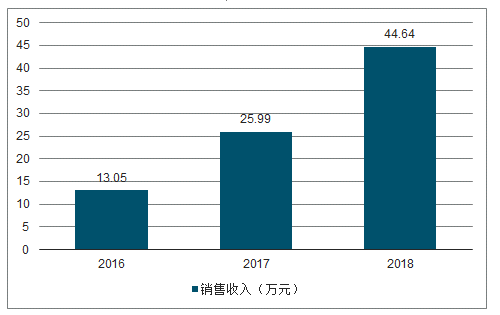
数据来源:公开资料整理
2016-2018年西达本胺的单价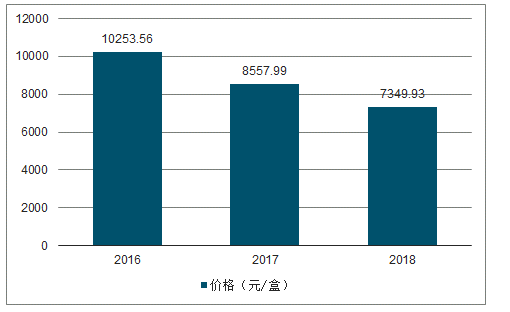
数据来源:公开资料整理
我国外周 T 细胞淋巴瘤每年新发患者约为 1.31-1.57 万人,按照临床统计的西达本胺1.85 万元/月的治疗费用测算,西达本胺对于外周 T 细胞淋巴瘤的销售空间达 29.08 亿-34.85 亿。2018 年西达本胺实现销售 1.37 亿元,渗透率约为 3.93%-4.71%。随着西达本胺片学术推广和医保报销等多层面的推动,产品有望加速渗透。
西达本胺
适应症 | 计算依据和说明 | 理论需求 人数 | 平均治 疗时间 | 治疗费用 | 市场空间 | 2018 年西 达本胺销 售额 | 渗透率 |
西达本胺 | 2014 年我国经年龄标准化后 淋巴瘤的发病率为 4.18/10 万 人。根据临床统计显示,淋巴 瘤中大部分为非霍奇金淋巴 瘤,约占 90%,而外周 T 细 胞淋巴瘤发病例数约占非霍奇 金淋巴瘤的 25%~30%,因此, 我国每年新增外周 T 细胞淋 巴瘤发病人数大约为1.31-1.57 万人。 | 1.31 万人 -1.57万人 | 4.4 个月 | 1.85 万元/ 月 | 29.08 亿 -34.85 亿 | 1.37 亿 | 3.93%-4.71% |
数据来源:公开资料整理
二、发展前景分析
1、非小细胞肺癌适应症处于临床三期
按照《中国晚期原发性肺癌诊治专家共识(2016 年版)》,非小细胞肺癌肺癌的治疗方案主要:EGFR 敏感突变:推荐 EGFR-TKIs(埃克替尼一线治疗,厄洛替尼和吉非替尼二线/三线治疗);LK 阳性:推荐克唑替尼作为一线治疗;EGFR 敏感突变,ALK 阴性:体力状况评分(ECOG PS)0-1 分,建议含铂两药方案全身治疗(不适合铂类药物患者,建议非铂类两药联合化疗),并考虑联合血管生成抑制剂治疗;ECOG PS 评分=2,建议单药化疗;ECOG PS 评分≥3,建议采用最佳支持治疗;EGFR 敏感突变阴性/ALK 阴性:建议优先考虑化疗(联合西达本胺的治疗方案处于临床三期);从临床结果分析,按照目前已公布的一期临床结果,西达本胺与紫杉醇和卡帕联用一般可耐受,推荐剂量为 20mg(用法用量:3 周一个疗程,每周两次服用 20mg 西达本胺,4 个疗程后疾病缓解或稳定后维持西达本胺单药治疗)。
从患者群体层面分析,西达本胺主要针对表皮生长因子受体(EGFR)基因突变阴性或无法检测的非小细胞肺癌患者,我国肺癌新发病例 73.30 万人。
其中,非小细胞肺癌患者占比 80%,对应 58.64 万人。非小细胞肺癌患者当中,EGFR 阴性比例 52%,西达本胺对应目标患者人群约 30.49 万人。从治疗费用层面分析,西达本胺(外周 T 细胞淋巴瘤)目前 9240 元/5mg*24 片的中标价,按照 3 周一个疗程,每周两次服用 20mg 西达本胺的用法用量,每个疗程的治疗费用约为 9240 元,每年治疗费用约为 16.02 万元。
从销售空间层面分析,西达本胺对应表皮生长因子受体(EGFR)基因突变阴性或无法检测的非小细胞肺癌患者(约 30.49 万人),按照每年 16.02 万元治疗费用,该品种在非小细胞肺癌上的销售空间为 488.49亿元。假设西达本胺在非小细胞肺癌上的渗透率为 4.5%,对应 21.98 亿元销售峰值。
2、乳腺癌适应症处于临床三期
西达本胺拓展适应症用于激素受体阳性晚期乳腺癌治疗,目前研发进度处于临床三期。临床设计方案为西达本胺联合内分泌治疗药物依西美坦进行治疗。西达本胺一方面具有亚型选择性 HDAC 抑制剂的特有表观遗传调控特征,另一方面通过调控乳腺癌细胞激素受体依赖和1非依赖通路,达到治疗乳腺癌的作用。
按照中国抗癌协会乳腺癌诊治指南与规范,乳腺癌主要分 Luminal A 样、Luminal B 样(HER-2 阴性)、Luminal B 样 (HER-2 阳性)、ERBB2+型、Basal-like 型等亚型。
乳腺癌的治疗方案
乳腺癌亚型 | 标志物 | 治疗类型 | 各分子亚型发病比例 |
Luminal A 样 | Luminal A 样 ER/PR 阳性且 PR 高表达 HER-2 阴性 Ki-67 低表达 | 大多数患者仅需内分泌治疗 | 65%-70% |
Luminal B 样 (HER-2 阴性) | Luminal B 样(HER-2 阴性) ER/PR 阳性 HER-2 阴性 且 Ki-67 高表达或 PR 低表达 | 全部患者均需内分泌治疗,大多数 患者要加用化疗 | - |
Luminal B 样 (HER-2 阳性) | Luminal B 样(HER-2 阳性) ER/PR 阳性 HER-2 阳性(蛋白过表达或基因扩增) 任何状态的 Ki-67 | 化疗+抗 HER-2 治疗+内分泌治疗 | - |
ERBB2+型 | HER-2 阳性 HER-2 阳性(蛋白过表达或基因扩增) ER 阴性和 PR 阴性 | 化疗+抗 HER-2 治疗 | - |
Basal-like 型 | 三阴性(非特殊型浸润性导管癌) ER 阴性 PR 阴性 HER-2 阴性 | 化疗 | - |
数据来源:公开资料整理
从临床试验结果分析,三期临床采用“西达本胺(每周两次,每次 30mg)+依西美坦(每天 1 次,每次 25mg)”VS“安慰剂(每周 2 次)+依西美坦(每天 1 次,每次 25mg)”进行对照,西达本胺组中位无进展生存期 7.4 个月明显优于安慰组的 3.8 个月。三期临床结果表明,西达本胺联合依西美坦可成为雌激素受体阳性晚期乳腺癌患者的治疗新选择。
西达本胺对于治疗雌激素受体(ER)阳性晚期乳腺癌的三期临床试验
试验设计 | 临床试验设计的具体内容 |
试验目的 | 评估西达本胺联合依西美坦在治疗绝经后激素受体阳性晚期乳腺癌患者中的疗效和安全性; |
试验方法 | 随机、双盲、安慰剂对照的 3 期试验,通过一个交互网络系统采用动态随机方案,选取 365 例符 合条件的患者,按照 2:1 的比例随机分配至接受西达本胺(口服,每周两次,每次 30mg 剂量共 6 片)联合依西美坦(口服,每天 1 次 25 毫克)治疗,或者安慰剂(口服,每周 2 次,与西达本 胺外观类似的片剂共 6 片)联合依西美坦(口服,每天 1 次 25mg)治疗。 |
试验结果 | 244 例接受西达本胺联合依西美坦,121 例接受安慰剂联合依西美坦。基于研究者评估的中位无进 展生存期在西达本胺组为 7.4 个月(95%CI 5.5-9.2),而安慰剂组为 3.8 个月(95%CI 3.7-5.5), 西达本胺组更优(HR 0.75,95%CI 0.58-0.98,P=0.034)。两组治疗中最常见的 3 或 4 级不良反 应均为中性粒细胞减少【西达本胺组 244 例患者中有 124 例(51%),安慰剂组 121 例患者中 有 3 例(2%)】、血小板减少【(西达本胺组 67 例(27%),安慰剂组 3 例(2%))、以及 白细胞减少【(西达本胺组 46 例(19%),安慰剂组 3 例(2%))。严重不良事件在西达本胺 组 244 例患者中有 51 例(21%),在安慰剂组 121 例患者中有 7 例(6%)。没有与治疗药物 相关的死亡发生; |
试验结论 | 亚型选择性 HDAC 抑制剂联合内分泌治疗可以提高在既往内分泌治疗进展后的激素受体阳性晚 期乳腺癌患者的无进展生存期,西达本胺联合依西美坦可以为这些患者提供一种新的治疗选择。 |
数据来源:公开资料整理
从患者群体层面分析,2014 年我国女性乳腺癌发病率为 41.82 人/10 万,中国女性乳腺癌新发病例约27.9 万,按照每年 2%增速增长,2019 年对应 30.80 万人。雌激素受体阳性乳腺癌占比约为 70%,早期患者约 40%概率发展为晚期乳腺癌,则雌激素受体阳性晚期乳腺癌患者人数约为 8.62 万人。从治疗费用层面分析,西达本胺目前中标价格为 9240 元/5mg*24 片,按照临床设计方案(口服西达本胺,每周两次,每次 30mg),治疗费用约为 24.02 万元/年。从市场空间层面分析,西达本胺对应的患者群体为雌激素受体阳性晚期乳腺癌患者,人数约为 8.62 万人,按照 24.02 万元治疗总费用估算,对应 207.22 亿元的市场空间。假设在雌激素受体阳性晚期乳腺癌上的渗透率为 5%,对应 10.36 亿元销售峰值。
3、弥漫性大 B细胞淋巴癌适应症处于临床二期
目前对于弥漫性大 B 细胞淋巴癌的一线治疗选择为蒽环类为基础的 CHOP 化疗+利妥昔单抗。目前,西达本胺对于弥漫性大 B 细胞淋巴癌适应症的研发处于临床二期。
从临床试验分析,西达本胺对于弥漫性大 B 细胞淋巴癌适应症的研发处于临床二期,研究目的主要评估西达本胺联合利妥昔单抗治疗复发或难治(难治的弥漫大 B 细胞淋巴瘤是指经过 2 个标准的含有或者不含有利妥昔单抗的 CHOP 方案化疗,治疗无效或者进展)的弥漫大 B 细胞淋巴瘤的疗效。
从患者群体层面分析,根据国家癌症中心发布的数据,2014 年我国经年龄标准化后淋巴瘤的发病率为 4.18/10 万人。根据临床统计显示,淋巴瘤中约 90%为非霍奇金淋巴瘤,而弥漫性大 B 细胞淋巴癌发病例数约占非霍奇金淋巴瘤的 32.5%。因此,我国每年新增弥漫性大 B 细胞淋巴癌发病人数大约 1.71 万人从药品定价层面分析,西达本胺目前中标价为 9240 元/5mg*24 片,按照 20mg/次,每周 2 次的用法用量保守估计(目前中国临床试验注册中心尚未公布临床治疗方案,我们进行保守假设),治疗费用约为 16.02万元/年。
从销售空间层面分析,西达本胺对应弥漫性大 B 细胞淋巴癌患者群体,人数约为 1.71 万人,按照 16.02万元治疗总费用估算,对应 27.42 亿元的市场空间。假设在雌激素受体阳性晚期乳腺癌上的渗透率为 20%,对应 5.48 亿元销售峰值。
与相对其他二线药物相比西达本胺具有以下优势:(1)使用西达本胺的 PTCL 患者的总生存期更长;(2)西达本胺为口服制剂,依从性好;(3)费用低,西大苯胺 1.85 万元/月的治疗费用低于普拉曲沙、罗米地辛和贝利司他等药物。我国外周 T 细胞淋巴瘤每年新发患者约为 1.31-1.57 万人,按照西达本胺 1.85万元/月的治疗费用测算,西达本胺对于外周 T 细胞淋巴瘤的销售空间达 29.08 亿-34.85 亿。2018 年西达本胺实现销售 1.37 亿元,渗透率约为 3.93%-4.71%。随着西达本胺片学术推广和医保报销等多层面的推动,产品有望加速渗透。
相关报告:智研咨询发布的《2020-2026年中国西达本胺行业竞争格局分析及战略咨询研究报告》

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询


















![2026年中国合成生物行业发展全景分析:下游应用从医药健康、化工材料向农业食品、能源环保全面渗透,行业已展现出巨大的应用潜力[图]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![2026年中国骨密度仪行业产业链图谱、采购总量、采购金额、获批企业、竞争格局及未来竞争趋势分析:外资品牌占据主导地位[图]](http://img.chyxx.com/images/2022/0330/e060dd24be7392f76ddd0a84489963879d953ac6.png?x-oss-process=style/w320)
![研判2026!中国物联网行业概念、市场规模、企业竞争格局分析:中国物联网产业领跑全球,AI融合驱动“泛在智联”新纪元[图]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![研判2026!中国汽车行业分类、产销量、重点企业销量分析:一季度中国汽车行业现“内冷外热”分化,出口同比激增成核心增量引擎[图]](http://img.chyxx.com/images/2022/0330/ff5315f651f3e124d0f5a156ac51655e46e5433f.png?x-oss-process=style/w320)
![2026年中国彩钢板行业发展历程、供需情况、市场规模、竞争格局及趋势研判:彩钢板市场规模达1138.76亿元,钢结构与绿色建材政策驱动增长[图]](http://img.chyxx.com/images/2022/0330/4279f04d08c7260a105d321a303d34a91af3a3d5.png?x-oss-process=style/w320)
![2026年中国UV灯管行业产业链、发展现状、竞争格局、竞争趋势分析:外资垄断高端赛道,中低端市场竞争白热化[图]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)
