医药研发外包服务:Contract Research Organization(CRO),合同研究组织,就是承担新药研究开发某一部分工作的专门研究机构或公司。
作为制药企业可借用的一种外部资源,CRO公司可以在短时间内迅速组织起一支具有高度专业化和具有丰富经验的研究队伍,缩短新药研发周期,降低新药研发费用,从而帮助制药企业在新药研发过程中实现“高质量的研究和低成本的投入”。
CRO公司是社会分工更加专业化和风险平均化的产物,CRO企业能够以较低成本且高效地完成某些药物研发工作,是医药研发产业链中不可缺少的环节。
CRO行业在不到四十年的时间内发展壮大,成为医药公司不可或缺的合作伙伴。
目前CRO行业的服务范围基本覆盖了新药研究与开发的各个阶段和领域,主要包括化学结构分析、化合物活性筛选、药理学、药代学(吸收、分布、代谢、排泄)、毒理学、药物配方、药物基因组学、药物安全性评价、I至IV期临床试验的设计、研究者和试验单位的选择、监查、稽查、数据管理、统计分析以及注册申报等工作。
按照研究阶段划分,CRO企业分为临床前CRO和临床试验CRO两大主要类别,目前临床前CRO主要从事化合物研究服务和临床前研究服务,其中化合物研究服务包括调研、先导化合物和活性药物中间体的合成及工艺开发;临床前研究服务服务包括药代动力学、药理毒理学、动物模型等。临床试验CRO主要以临床研究服务为主,包括I至IV期临床试验技术服务、临床试验数据管理和统计分析、注册申报以及上市后药物安全监测等。
智研咨询发布的《2019-2025年中国CRO市场供需预测及未来发展前景研究报告》指出:我国CRO产业2017年规模559亿,同比增速20%。我国CRO产业规模情况如下图所示:
2007-2017年中国CRO产业规模情况

资料来源:智研咨询整理
国内现有CRO企业众多,北京、上海、江苏是主要集聚区。从目前还处于存续状态的CRO企业的成立时间上看,2004-2014年是CRO发展的高峰时期,主要受益于GCP、GLP等行业政策发布,以及药品市场快速扩容的影响,新成立企业数量平均每年在30个以上,随着行业监管政策趋紧,行业进入调整期,近几年来新成立企业数量放缓。
按照地域分布来看,CRO企业主要分布在北京、上海、江苏等地,这三个地区的一个共同特征是:产业园区发展相对成熟、医药企业相对集中、创新创业产业发展活跃、人才以及教育资源较为丰富等。
国内CRO企业区域分布
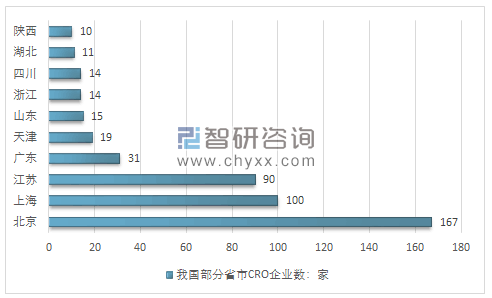
资料来源:智研咨询整理
中国生物医药外包市场竞争激烈
1、以昆泰、科文斯、PPD等大型跨国企业和药明康德得益于强大的资金实力、庞大的业务规模、丰富的项目经验,占据着我国CRO行业的顶尖位置。这些CRO公司承担了大量的跨国药企在我国的新药研发工作,但其占国内医药企业的外包服务市场份额较低。
2、其次是本土大型CRO企业,以泰格医药、博济医药等为代表,熟悉国内市场,可提供大部分临床前和临床试验研究服务,但在资金实力、业务规模、国际多中心试验开展上与大型跨国CRO企业尚有差距。不过,近年来我国本土企业开始通过兼并重组等方式积极拓展国外市场。
3、数目最多的也是准入门槛最低的是中小型本土CRO,良莠不齐,很多以提供注册申报等低技术密集型的工作为主,盈利能力较差,容易陷入无序竞争,但运作规范的CRO企业将在激烈竞争中生存壮大。
随着康龙化成的成功上市,A股再添加一家CRO上市公司。随着CRO公司的接连上市,行业将在资本的助推下获得快速发展,但对企业自身而言却也同样将面对激烈的竞争压力。
2017年中国医药外包产业企业集中度情况
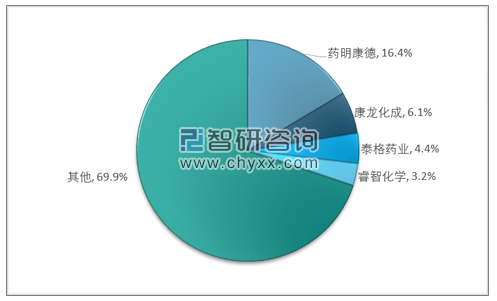
资料来源:智研咨询整理
参考国外创新药市场和药物外包行业的发展历史,二者的快速发展休戚相关。政策推动下,中国正开始进入创新药大时代中,创新药的发展将推动医药研发和生产外包服务的快速发展,预计未来5-10年都是黄金发展期。
相比于欧美等市场发展历史,CRO行业近20年才在中国得到发展,其潜力相对于欧美国家更大。
1996年,MDS Pharma Service投资设立了中国第一家真正意义上的CRO,从事临床研究服务业务,中国CRO行业开始萌芽。2000年药明康德成立,随后尚华医药、博济医药、泰格医药等目前国内主要CRO公司成立,中国CRO行业开始正真开始起步。
一、医保控费和一致性评价催生CRO行业快速发展
随着人口老龄化进程的加剧,医保费用透支仍旧是我国面临的重大社会问题,解决这一问题的最关键因素就是医保控费,要控费就必须降低昂贵的原研药的使用额度,因此国产药代替进口药将成为大势所趋,但进口替代的前提则是国内仿制药质量能够保证。因此,CFDA推出了仿制药一致性评价,随着一致性评价的逐渐推进,国内仿制药企业有望加速实现进口替代。
一致性评价的仿制药替代原研药的思路是:只有质量和原研药一样的仿制药才可以CFDA提出“通过一致性评价”,这些国产仿制药在临床上将得到优先使用的特权,这样可以直接降低百姓的用药负担,减少医保支出,提高医保基金的使用效率。同时能间接促使国产药企注重仿制药品的质量和疗效,有利于淘汰落后产能,提高国产药企的竞争力,可以打破市场份额被原研药企垄断的桎梏。
文件要求2018年底前须完成目录中品种的仿制药一致性评价,289个品种共涉及19715个批准文号,涉及企业数量为2028家,其中7家企业批文数量超过100个,47家企业所持批文数量为50-100个,529家企业批文数量在10-50之间。如果企业做一致性评价申报能够一次性成功也至少要耗时22个月。而至2018年年底,已经仅剩30个月不到的时间了,企业的时间很不充裕。此次开展的一致性评价执行力度大、时间紧、任务重,企业势必将主动放弃一部分品种,而选择体量较大、成功率较高、具有竞争优势或性价比较高的品种开展一致性评价。但国内只有少数大型药企能够自行承担仿制药一致性评价,大多数药企没有充足的时间和资源自行开展,只能选择外包给CRO企业,因此CRO企业将迎来订单项目的快速增长期。
二、业务范围不断延伸,打造一体化服务
医药研发外包服务业务已由最初的药物发现、临床前研究、、药物安全性评价等有限服务发展到几十项内容,甚至包括数据管理与分析、信息学、政策法规咨询、产品注册、生产和包装、推广、市场、产品发布和销售支持以及各类相关的商业咨询等诸多领域,而且每年都有新的服务内容增加。
目前,国际CRO巨头们的业务范围基本都已经覆盖了药物发现到上市过程中的全部流程。未来巨头将进一步加强现有服务内容,并且继续拓展业务范围。合同生产(CMO)和合同销售(CSO)正在逐步融入CRO制造商的服务内容中。昆泰作为临床研究服务的巨头,已经逐渐将其业务内容拓展到商业、咨询等业务,未来昆泰将进一步加强商业服务模块。药明康德作为临床前研究服务的巨头,近些年其业务范固基本已经覆盖了医药研发过程中的所有流程,期合同生产业务也正在加紧布局。2016年3月,药明生物在其无锡CGMP工厂为战略合作伙伴Prima制造商生产的创新肿瘤免疫候选药物IMP321(LAG-3Ig融合蛋白),被正式用于比利时11b期临床试验,首位患者成功入组并被给药。
三、服务方式:从从药企辅助者走向战略伙伴
制药制造商与CRO合作方式已经逐渐从单个项目合作走向战略结盟,并且未来的合作关系将进一步加强,实现利益共同分享和风险共同承担。
与其他传统合作模式相比,战略联盟的方式主要有这几方面优势:
1、利用每个项目中透明且可重复的过程提高服务质量;
2、实现风险共担,减少药企的的风险;
3、可以通过长期的合作方式,培养CRO与客户之间的信任度;
4、通过长期稳定的合作团队确保持续的合作质量;
5、通过避免反复招标以减少药品进入市场的时间;
6、是多种药物要发同时进行;
7、可以提高研发工作的连贯性和准时性。

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询



















![趋势研判!2026年全球车辆铰接系统行业产业链、市场规模、竞争格局及发展趋势:市场规模将突破20亿元,本土企业迅速崛起,“一超多强”格局正在重塑[图]](http://img.chyxx.com/images/2022/0330/dd2a6e2dd1963d26c8672c625ba6166e69bd4120.png?x-oss-process=style/w320)
![2026年全球智能泳池设备行业政策、产业链、市场规模、竞争格局及发展趋势研判:市场规模呈现持续增长态势,有望突破40亿美元[图]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)
![研判2026!中国透明质酸钠行业性质、生产工艺、产业链、市场规模及发展趋势分析:从传统保湿到前沿再生,技术创新重塑透明质酸钠应用版图[图]](http://img.chyxx.com/images/2022/0330/d1363a7ee3953fc25ed09e0b79158acce9dc7c22.png?x-oss-process=style/w320)
![趋势研判!2026年中国冶金煤行业政策、供需情况、市场规模、重点企业及发展趋势:冶金煤供不应求结构性短缺特征明显,市场规模增速有所放缓[图]](http://img.chyxx.com/images/2022/0408/54b870b64f647f1fc10474b02796382c9242dcfa.png?x-oss-process=style/w320)
![研判2026!中国商业航天行业相关政策、发射情况、企业布局及融资情况分析:从“补充”到“主导”,多款新型号首飞在即[图]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)
