一、CRO提高研发效率,正在全球范围蓬勃发展
1、CRO是药品研发分工专业化的产物
CRO(ContractResearchOrganization)即合同研究组织,是指通过合同形式为医药企业在药物研发过程中提供专业化外包服务的组织或机构。CRO企业接受药企的委托,执行新药研究中的部分工作。
新药研发是一个复杂的、长期的活动。为了获得活性化合物、证实新药的疗效及保证其安全性需要经过包括早期药物发现阶段(活性成分发现与筛选)、临床前研究阶段(药学研究+药物评价)、临床研究阶段(I、II、III期临床)、审批上市(审批上市、IV期临床及药物后期监测)在内等诸多流程。因此,药物研发不仅是一项高投入、高回报,同时又是高风险的业务,新药研发不仅耗资大、耗时长,且失败率也非常高。
CRO可提高研发效率、降低成本,是专业化分工的产物。在新药研发变得更复杂、费时,成本和风险不断增长的同时,外部监管也更加严格,为了提高效率,研发外包服务需求不断增长。新药研发过程中有很多重复性的工作,如前期研究中的合成提纯、中期的临床管理、后期的材料申报审批等,都可以直接外包以节省成本。总的来说,CRO具有三方面意义:
1)降低成本与风险分担。新药可为药企带来巨大利润,但新药的研发投入和风险也很高,一个项目的失败往往伴随巨大的经济损失和裁员。一般而言,CRO人员成本比大型药企低20-30%,研发外包在降低新药研发的成本的同时,可以提高药企研发的灵活性,降低风险;
2)降低研发难度。新药研发是一个复杂的系统工程,外包以及多方合作可以将研发过程分解,降低研发的复杂性,能够在一定程度上减小研发难度;
3)缩短研发周期。新药研发从药物发现到获批上市一般要耗时10-15年,其中,药物发现与临床前研究耗时在3-6年,临床的时间跨度基本在6-7年,监管机构审批时间在0.5-2年。药企把研发的过程分解并将部分流程外包,从而使得更多、更专业的专家一起加入到新药研发中,缩短新药的研发周期。一般来说,由CRO承担的项目与药企自身承担的项目所需时间相比,大约可以节省1/3-1/4的时间。
CRO有效降低研发成本
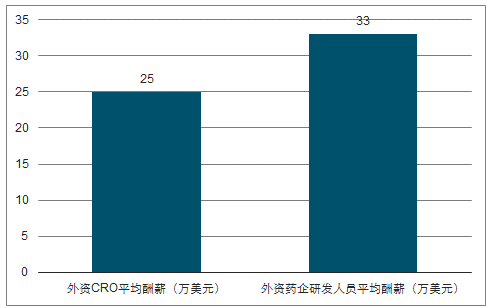
数据来源:公开资料整理
CRO有效缩短30%研发周期
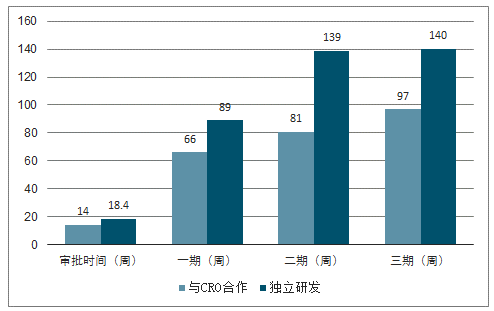
数据来源:公开资料整理
CRO业务可以分为临床前、临床两类。目前CRO相关服务范畴已经涵盖了药物研发的整个过程,成为医药研发产业链中不可缺少的环节,可粗略划分为两类:
1)临床前CRO:主要从事化合物研究服务和临床前研究服务,其中化合物研究服务包括调研、先导化合物和活性药物中间体的合成及工艺开发,临床前研究服务服务包括药代动力学、药理毒理学、药效学等。
2)临床CRO:主要以临床研究服务为主,包括I至IV期临床试验技术服务、临床试验数据管理和统计分析、注册申报以及上市后药物安全监测等。
CRO已涵盖药物研发的整个过程,包含临床前和临床CRO

数据来源:公开资料整理
二、全球研发成本不断增加,医药服务外包向中国转移
1)新药研发周期长,研发投入大,回报率低
药物研发过程复杂化,药企面临巨大压力:新药研发具有高技术、高风险、高投入和长周期的特征,最初的10000+个候选化合物经历临床前研究、临床试验、药品注册申请与审批等研发过程最终只有1个创新药物能够批准上市,整个研发周期更是长达数十年,投入资金高达几十亿美金,这对医药企业的研发实力、质量水平以及资金实力无疑提出了巨大的挑战。
新药研发周期长、难度高、投入大
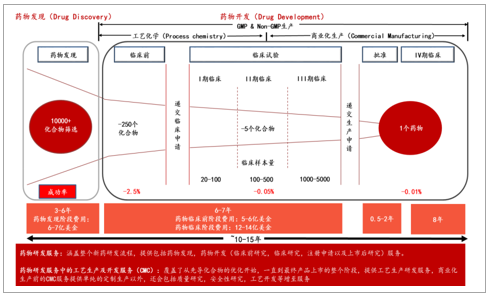
数据来源:公开资料整理
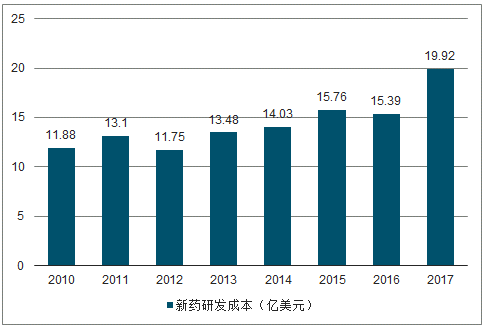
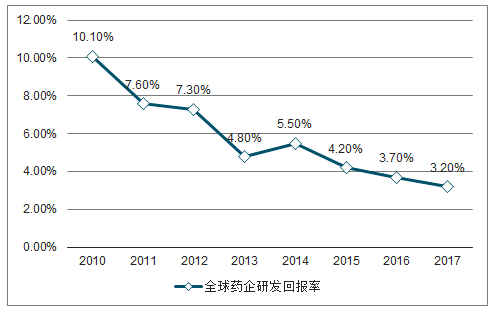
医药研发投入大但回报率低:2017年全球医药研发投入高达1650亿美元,同比增长3.9%,研发投入占收入比例为18.9%。预测到2024年全球研发投入将达到2040亿美元,2018-2024年研发费用年复合增长率为3.1%。虽然新药研发费用不断的增加,但是研发回报率却在不断的下降。单个新药的研发成本从2010年的11.88亿美元上升到2017年的19.92亿美元;而研发回报率却从2010年的10.1%下降到2017年的3.2%。
2010-2024年全球医药研发投入情况
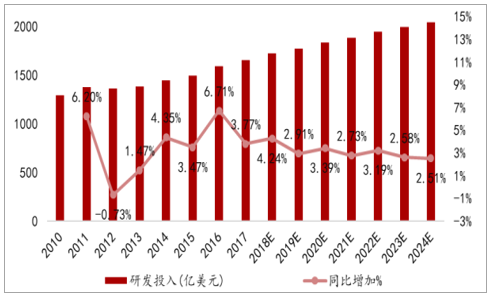
数据来源:公开资料整理
单个新药研发成本逐年上升(亿美元)
数据来源:公开资料整理
全球药企研发回报率逐年下降
数据来源:公开资料整理
2)受益于全球CRO产能转移,中国研发外包高速增长
由于新药研发复杂程度的提升,导致研发费用不断的上涨和研发成功率不断降低,药企为了缩短研发周期和降低研发的风险,从而将一些非核心的研发外包给CRO企业。CRO企业集合专业人才和知识、先进的设备,能够帮助制药企业加速项目研发进程、控制风险、优化资源及降低成本,因此越来越多的药企开始寻求与CRO企业合作将药品研发外包,CRO可以帮助药企节省大约20%研发时间。
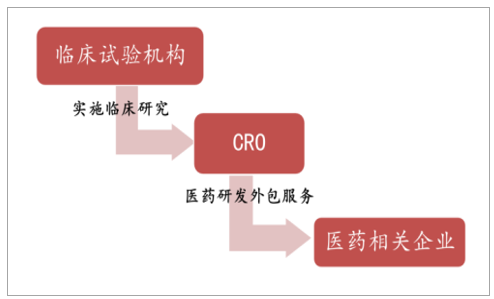
CRO已成药物研发环节重要的一环
数据来源:公开资料整理
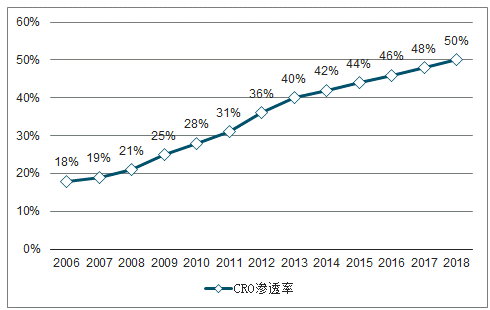
CRO渗透率逐年提升
数据来源:公开资料整理
CRO可以帮助药企节约20%研发时间
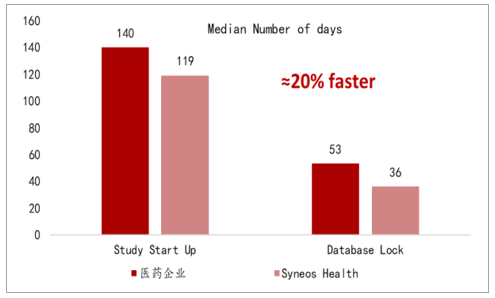
数据来源:公开资料整理
到2021年全球CRO市场将达到646亿美元,2016年到2021年CAGR=12.8%。而亚太市场由于人口红利和成本等多方面优势,离岸外包服务发展得天独厚,预计2021年亚太地区CRO市场将达到123亿美元,2016年到2021年CAGR=20.3%,其中中国CRO市场复合年增长率更是高达28.3%。
全球CRO市场规模预测
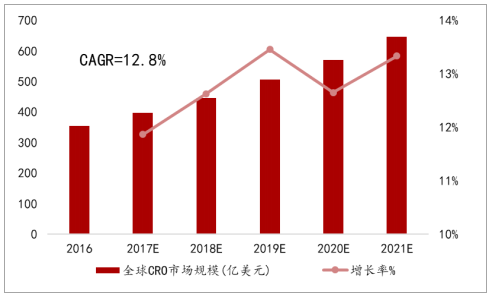
数据来源:公开资料整理
亚太区CRO市场规模预测
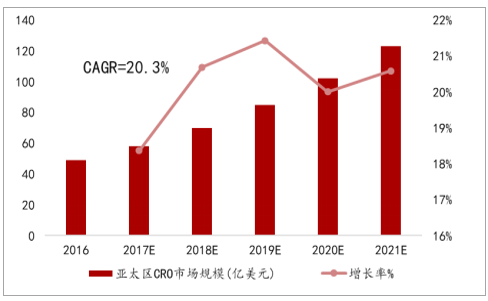
数据来源:公开资料整理
三、我国CRO产业在承接外资需求中发展壮大
1、我国CRO产业在外资药企外包需求中建立
我国CRO产业在承接外资需求中建立,内资药企外包需求近年爆发。国内CRO产业自成立之初,主体都是承接外资药企外包需求。近年来,内资药企的外包需求正爆发式增长。具体而言,国内CRO产业的发展可以简略划分为三个阶段:
1)外资药企离岸外包期:1996-2008年。在承接外资临床前外包需求中,国内CRO产业蓬勃发展。我国境内第一家CRO是由MDS于1996年设立的分支机构,主要做临床业务。随着2000年美股科技股泡沫破裂,药企巨头中的大量海归回到中国,建立了第一批内资CRO公司。依托于国内大学扩招带来的人口红利,内资CRO公司凭借成本优势,大量承接外资药企临床前外包需求。临床方面,在这一过程中,外资CRO纷纷通过并购、自建等方式在我国境内建立起了分支机构,主要为了服务于海外已上市药品在我国的上市需求。这段时间,虽然我国在2003年建立了GLP、GCP制度,但要求十分宽松。国内药企研发基本是仿制药,并且国内药企普遍享受各地政府补贴,补贴往往专款专用,普遍用于购买仪器,所以这段时间内资药企对CRO的需求很小。
2)外资药企开拓市场期:2009-2015年。内资需求占比逐步提升,但外资需求仍是主体。金融危机后,外资药企纷纷开源节流:削减早期研发投入,将有限的资源投入到处于临床阶段等即将商业化的项目中,并积极开拓新市场。09年我国临床前CRO市场受到外资需求波动的冲击,当年增速急剧下滑,但此后众多Biotech公司成立,这些公司更加依赖CRO,驱动临床前CRO行业继续高速增长。临床CRO行业则受益于外资药企积极开拓国内市场,09年之后增速反而有所提升。竞争格局方面,不同于08年之前的百花齐放,09年之后国内临床前和临床CRO都出现了一定的分化,走出了药明康德、康龙化成、睿智化学、泰格医药等优势企业。
3)内资药企发展期:2016年之后。自15年起,一系列的药改政策促进了国内药企的研发投入,内资需求增速超过了外资需求,但外资需求仍占主体。在此前竞争中走出来的头部CRO公司,积累了大量的创新药研发经验,成为了国内创新药研发外包的首选。头部CRO的地位逐步强化。
我国CRO产业历经三个阶段
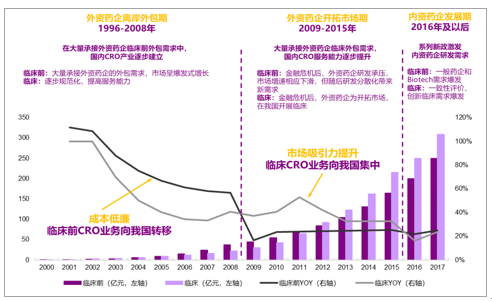
数据来源:公开资料整理
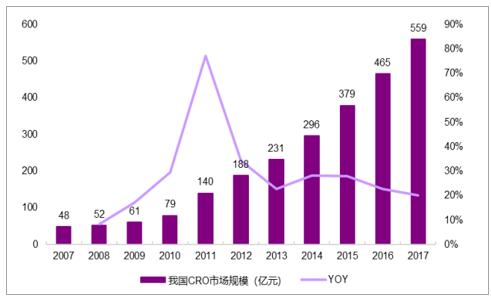
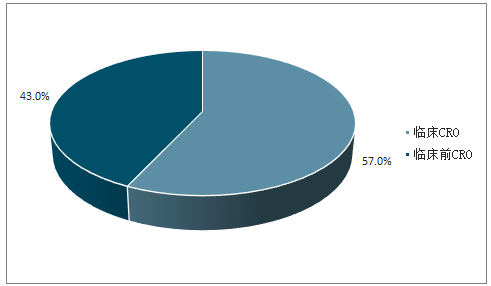
我国CRO产业17年规模559亿,同比增速20%。我国CRO产业持续高速增长,2017年达到559亿,增速超20%。其中,临床CRO市场占比约57%。
17年我国CRO规模559亿,同比增速超20%
数据来源:公开资料整理
17年我国临床CRO占比57%,低于全球平均
数据来源:公开资料整理
四、我国CRO产业正迎来黄金发展期
1、研发分散化,预计全球CRO行业超10%较快增长
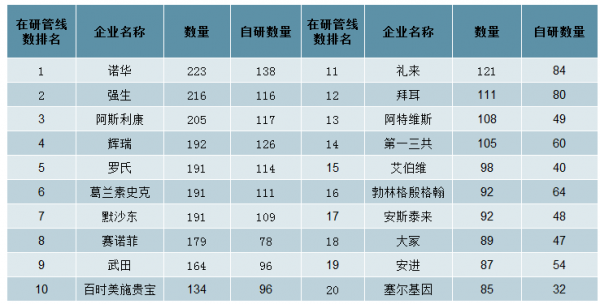
Biotech成为药品研发新兴力量。90年代开始,随着研发资金要求和难度不断提高,大型药企在更多地和CRO合作的同时,研发投向也更倾向于研发后期,研发管线的建立更多地依赖收购。尤其在08年金融危机中,许多大药企选择裁撤早期研发阶段的人员,这些人员大大促进了Biotech公司的发展。截至18年中,大药企的在研管线中,约有一半是通过并购获得。目前,拥有创新药研发管线的全球4000多家药企中,拥有管线数量在3个以下的小型药企占比超过50%。
全球大药企的在研管线约有一半是通过并购获得(截至18年6月底)
数据来源:公开资料整理
全球拥有在研创新药的小企业占比过半

数据来源:公开资料整理
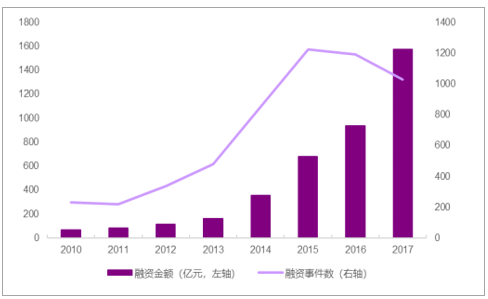
17年全球医药行业VC/PE融资1571亿
数据来源:公开资料整理
全球CRO行业18-21年仍将保持每年超10%较高速增长,预计2021年达到645.8亿美元。
全球在研创新药数量11-17年CAGR约7.4%
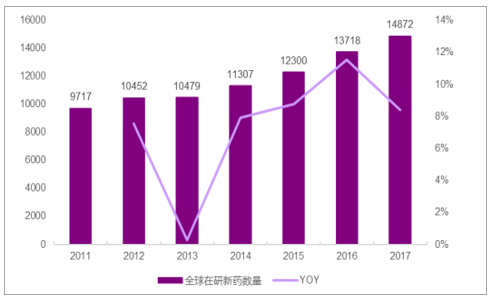
数据来源:公开资料整理
预计17-21年全球CRO行业CAGR为11%
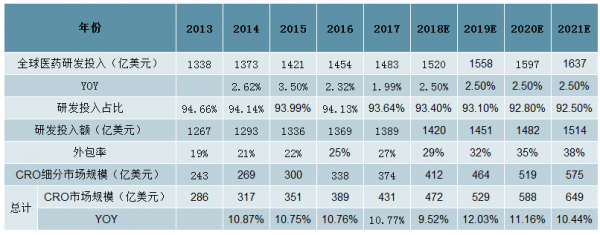
数据来源:公开资料整理
2、外资需求:我国仍是外包首选,需求将结构升级
我国CRO产业起源于外资药企的外包需求,下游长期以外资需求为主。目前,我国对外资药企外包需求依然具有吸引力。
1)临床前:我国成本、人力优势仍在,预计需求稳定增长
我国此前凭借着低成本、人力资源丰富的优势,吸引了大量的外资药企临床前外包需求。时至今日,我国的这两方面优势依然显著,同时相关产业已经较为成熟:1)低成本:2015年之前,我国人工成本仅为欧美发达国家的40%,16年之后,国内人力成本持续提升,报价也有所提升,目前报价大约在60%;2)人力资源丰富:自98年大约扩招以来,我国每年大学毕业生人数持续攀高,18年已超过800万人。3)相关产业成熟:经过近20年的发展,我国已经涌现出了一批优秀的CRO公司,这些公司完全可以承接符合发达国家GLP、GCP要求的项目,并有能力能承担全流程外包业务,目前已普遍与外资药企合作。另外,作为CRO行业的上游,我国化工行业可供应品类齐全,总体实力在发展中国家中优势明显。
虽然人工成本相比于印度、东南亚等国家不具优势,但临床前阶段的研发投入只占药品研发全周期总投入的30%。相对而言,技术服务能力是更重要的考量因素。
综合来看,我国依然对外资药企临床前外包需求极具吸引力,我们认为外资药企对我国的临床前外包需求将继续维持稳定增长。
2)临床:市场吸引力持续提升,外资需求将结构升级
在患者多样和临床成本优势的基础上,国内药品市场吸引力也在不断提升,吸引外资药企积极在我国开展临床。09年之后,外资药企为了拓展新市场,纷纷在中国开展临床试验。目前,随着针对海外药品的审批、医保新政逐步落地,我国药品市场对外资的吸引力进一步提升:
1)低成本:15年之前,我国人工成本和临床费用仅为欧美发达国家的40%,15年7月22日启动临床数据核查之后,国内临床费用有所提高,目前大约达到了海外70-80%的成本;
2)患者人群多样:中国有近14亿人口,各种疾病的患者人数众多,招募临床试验受试者较容易,可以加快新药研发进度,最大限度延长专利药垄断市场的时间;
3)市场吸引力持续提升:我国已经是仅次于美国的全球第二大医药市场。近年来落地的优先审评、医保谈判等政策,大大压缩了外资创新药国内审批、医保接入周期。目前,创新药医保谈判已经进行了3批,共覆盖56个品种,其中40个以上都是外资药企所有。最新批次的17个品种中有11个是17年之后上市。除此之外,进口抗癌药零关税等政策都将加大国内市场的吸引力。更重要的是,带量采购政策将压缩仿制药的体量,大大利好创新药的支付。外资药企积极拓展中国区业务,为我国CRO产业带来巨大需求:a)更多已在国外上市的重磅新药进入中国;b)在中国进行新药全球多中心临床试验,谋求在研新药在中国同步上市;c)研发具有“中国特色”的产品,如研发针对胃癌、肝癌、乙肝等中国高发病的药物。
本批次医保谈判是首次由医保局主导
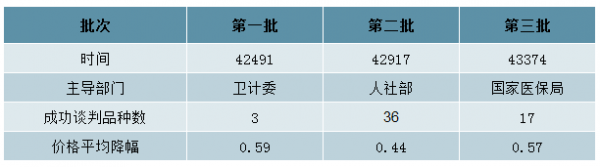
数据来源:公开资料整理
国际多中心、海外临床数据药审新政,促进外资临床外包需求结构升级。我国于17年6月正式加入ICH(国际人用药品注册技术协调会),预示着我国药品质量监管体系将逐步和国际接轨。在这一过程中,外资药企在国内开展的临床试验的结构将有所升级,具体体现在两个方面:
1)创新药国际多中心临床将迎来爆发:17年10月,CFDA发布了《国家食品药品监督管理总局关于调整进口药品注册管理有关事项的决定》,取消了原先要求申请国际多中心临床的要务必须已进入2期的限制,使得海外创新药可以在临床1期就可以进入我国进行临床试验;同时将“三报三批”简化为“两报两批”,简化审批流程。此举将促进外资药企更多地将我国和其他地区打包,以实现在各地区的快速上市。我们认为国内的国际多中心临床需求将增加。
2)海外已上市药品国内临床需求将有所回落:17年10月,CFDA发布了《接受境外临床试验数据的技术要求(征求意见稿)》。随即,外资药企开始对国内的海外数据认可政策观望,其在国内申请临床数量明显回落。18年7月,经过近1年的征求意见,正式文件发布,对海外临床数据的认可正式落地。正式文件中要求对于药品的有效性、安全性的评价,需要分析中国亚组与总体人群的一致性。由于绝大多数的海外临床试验当初在设计的时候都没有考虑到这一要求,我们认为海外已上市药品国内临床需求在未来几年内可能受冲击有限。我们观察到,外资药企每月在国内临床申请受理数已回升到正常水平。当然,随着越来越多的药企直接在国内开展国际多中心临床,远期海外已上市药品的国内临床需求将萎缩。
国际多中心、海外临床数据药审新政要点

数据来源:公开资料整理
我国每年开展的国际多中心临床数逐年提高(个)
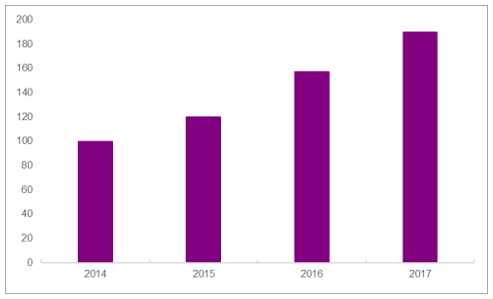
数据来源:公开资料整理
外资药企每月国内临床申请受理数已回升(个)
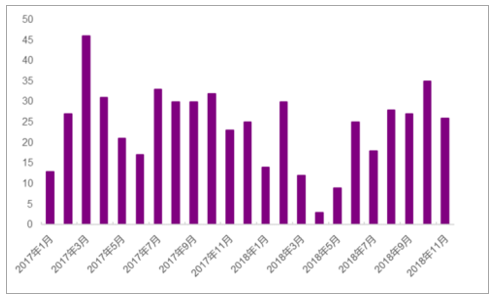
数据来源:公开资料整理
综上,我们认为外资药企在我国开展临床试验的需求将继续维持较高增长,同时内部结构将升级。国际多中心的临床需求占比将提升,而海外已上市多年的药品在国内的临床需求占比将下降,这给我国CRO公司带来了机遇和挑战。
3、内资需求:制药产业大破大立,研发外包需求迫切
1)我国制药产业大破大立,转型创新迫在眉睫
超级医保局开启我国制药产业大破大立时代,系列新政促进研发投入。自15年起,涵盖药品“研发-生产-流通-招标/采购-支付”全生命周期的改革新政陆续出台,几乎重构了我国制药行业的监管体系。这些新政指向了一个共同的目标:促进药企研发投入,加快医药产业升级。尤其是集“采购权、支付权、定价权”于一身的超级医保局成立,开始试点一致性评价仿制药的带量采购模式,预示着我国原有仿制药模式将终结。在新体系下,药品的临床价值成为更加核心的要素,原先审评审批、招采、医保目录调整周期长等行政壁垒带来的不合理红利被迅速压缩;原先大多数药企依赖的抢仿模式回报率大幅下滑,原有的仿制药“高定价、高费用、高毛利”的创新药营销模式开始终结。未来,企业只有不断推陈出新,持续加大研发投入,不断研发出真正具临床价值的新品才能生存。可以说,我国制药产业正迎来大破大立,转型创新迫在眉睫。
15年起,涉及药品全生命周期的各环节政策相继落地
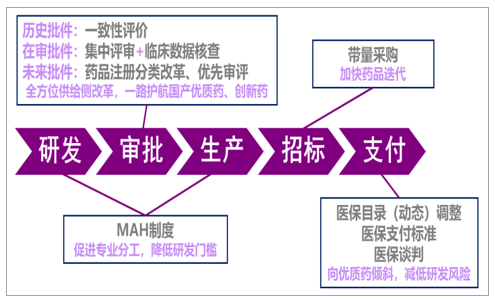
数据来源:公开资料整理
预计我国规模以上医药制造企业未来3年研发投入保持接近20%较高增长。由于国家统计局公布的规模以上医药制造企业统计数据样本可能变动,所以我们选用其公布的主营业务收入可比增速、研发投入强度这两个相对数字来计算我国规模以上医药制药企业研发投入情况。我国规模以上医药制造企业研发投入在17年明显加强,达到534亿,同比增长28%。我们预计,我国规模以上医药制造企业未来3年研发投入仍保持接近20%较高增长。
预计我国规模以上医药制造企业未来3年研发投入仍保持近20%较高增长
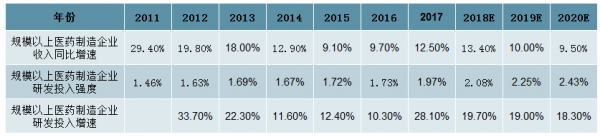
数据来源:公开资料整理
我国制药企业当前处境类似于全球大药企20世纪90年代的情况,CRO外包率有望快速提升。1984年,美国国会通过了《Hatch-Waxman法案》,简化了仿制药的研发审批流程。随后仿制药大量上市,自20世纪90年代,原研药企收入明显承压,研发效率成为更重要的考量因素,研发外包率开始显著提升,开启了全球CRO产业的高速发展期。在带量采购等政策下,我国药企面临的政策环境类似,我们预计,我国药企对CRO的依赖度有望提升。
研发投入结构升级,头部CRO更加受益。在研发投入高增长的同时,内部结构将不断升级,创新药投入占比将持续提升,头部CRO更加受益:1)临床前:我国CRO产业呈现分层竞争格局,头部公司主要承接高毛利的创新药业务,对全球创新药趋势更加敏感。而一般的CRO公司仅能依靠成本优势承接技术含量较低的仿制药业务。在我国制药产业大破大立的背景下,显然头部临床前CRO公司将是力图转型创新的内资药企的首选合作对象,相对更加受益;2)临床:头部临床CRO公司凭借外资创新药业务的积累,在内资创新大潮中同样更加受益。我国创新药临床获批数量上升趋势明显,15、16年受益于审评效率提高而呈现爆发式增长,17年继续维持高位。一般完整的创新药临床试验周期在3年以上,头部临床CRO公司将充分受益于15-17年的创新药临床申请的大量获批。
我国15-17年创新药临床申请大量获批

数据来源:公开资料整理
单提价对冲肿瘤领域患者短缺风险。出于学术性的考虑,医院倾向于承接创新药临床项目。所以总体而言,创新药的临床基地比较充足。但肿瘤领域的创新药数量较多,可能面临患者招募瓶颈。肿瘤领域临床CRO服务的报价已经提高到了单位志愿者10万元,可以一定程度对冲了患者短缺风险。
2)一致性评价:预计贡献累计510亿CRO市场空间
药品质量标准不一,一致性评价势在必行。所谓药物一致性评价,就是仿制药必须和原研药“管理一致性、中间过程一致性、质量标准一致性等全过程一致”的高标准要求。中国药品审评审批法规几经修订,目前流通中药品批文估计超过18万个,“地标转国标”的品种、郑筱萸时期品种、2007年药审标准收紧后品种同时存在。部分产品疗效存疑、存在安全隐患;不少产品获得几乎永久“独家”资质;安全无效药品大行其道,侵蚀宝贵医保资源;外企原研药享受价格超国民待遇。为提升药品质量,促进行业优胜劣汰,可以说一致性评价势在必行。
全部07年前化药口服固体制剂均需通过一致性评价。借鉴美国、日本等国仿制药一致性再评价经验,2016年3月国务院正式印发《关于开展仿制药质量和疗效一致性评价的意见》:全部化学药品均需通过仿制药一致性再评价,07年之前审批的2012版基药目录中口服固体制剂要求2018年底前完成,其他品种分期分批逐步推进。
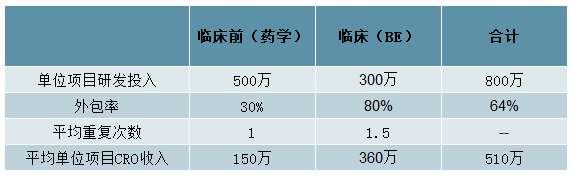
一致性评价的核心环节是药学研究和BE两部分。药学研究和BE是一致性评价中的最核心环节,主要的花费都在这两个环节。一般一个批件药学部分外包报价500w(包过,单次300w),BE部分300w(医院费用150w)。药学部分大多由药企自己完成,外包率约30%;BE部分要对接临床机构,外包率高达80%。折算下来,平均一个做一致性评价的批件,可以为临床前CRO市场带来150w收入,为临床CRO市场带来360w收入。
一致性评价流程
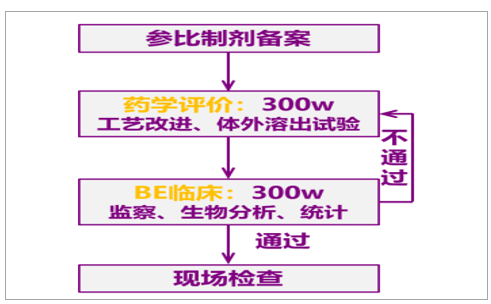
数据来源:公开资料整理
平均一个做一致性评价的批件,可以为CRO市场带来510w收入
数据来源:公开资料整理
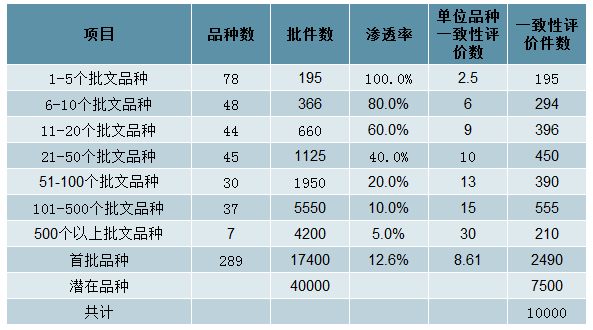
预计一致性评价贡献510亿CRO市场空间。07年10月之前获批的化药口服固体制剂均需做一致性评价,共计60000个批件。其中,基药目录中的289个品种为首批,涉及1.7万个批准文号、1800家企业。我们估算:
1)首批批件2500个:5个批文以下品种全做,5个以上品种平均做一致性评价件数假设如表15。迫切需要做一次性评价2490件。
2)潜在批件7500个:暂不考虑中成药、注射剂,首批品种以外的化药口服固体制剂批文约4万件,假设潜在需要做一致性评价的非基药口服固体制剂是迫切品种的3倍,约7500件。
综上,一致性评价需求约有1万个批文,总体为CRO企业带来510亿营收空间。其中临床前150亿,临床360亿。
一致性评价贡献510亿CRO累计市场空间
数据来源:公开资料整理
临床机构放开,破除BE产能瓶颈。此前,由于仿制药的临床并不具备太多的学术价值,并且报价较低,医院没有足够的动力承接BE试验。2015年的“722”临床数据核查后,BE试验的报价迅速攀升,达到了单位志愿者3万元。随着经济性的提高,临床中心在全国各地陆续建设。目前,BE临床基地已不再是瓶颈。
3)多因素催生一级市场医药大潮,带来每年近百亿外包需求
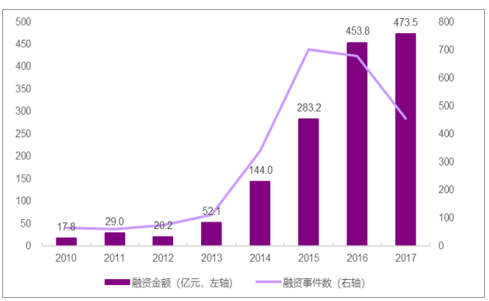
多因素催生一级市场医药大潮。近年来,一级市场医药的行情火热。17年,我国医药行业在一级市场共发生455起投资事件,合计474亿元。我们认为是多方面因素共振的结果:
1)医药促进创新政策:如前所述,15年起,涉及药品全生命周期的各环节政策相继落地。这些新政指向了一个共同的目标:促进药企研发投入,加快医药产业升级;
2)外资药企裁员提供充足人才:外资药企裁员并不鲜见,往往在原研药专利到期、在研项目失败后会进行相关人员调整。但在08年金融危机之后,外资药品逐步减少早期研发人员,转而更多的通过收购来储备项目。这些早期阶段研发人员就成为了Biotech公司重要的人才来源;
3)退出渠道拓宽:港交所放开对Biotech公司IPO限制等;
4)集中审评带来临床批件爆发:面对在申请批件积压问题,CFDA于15年开展集中审评,即打破原有受理号排队顺序,直接将同类型药品放在一起比较,这样大大加快了审评效率,带来了临床批件数量大爆发。临床批件作为一个阶段性的成果,促进了相关Biotech的融资。
17年我国医药行业VC/PE融资474亿
数据来源:公开资料整理
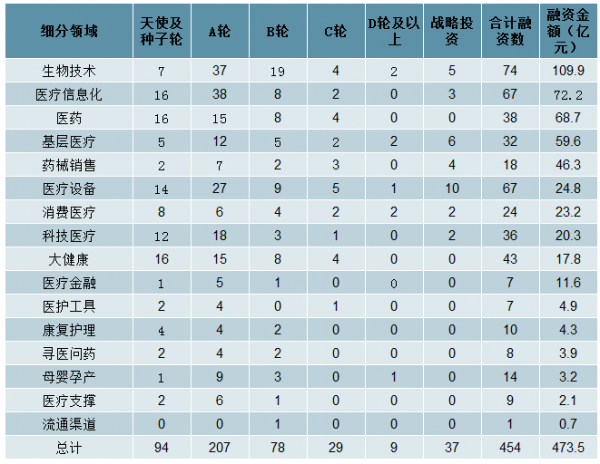
2017年我国医药行业VC/PE融资事件细分领域、阶段分布
数据来源:公开资料整理
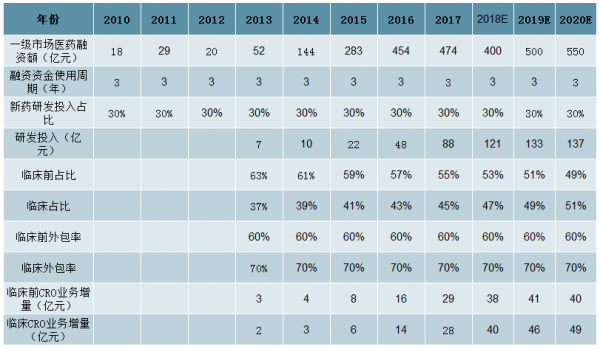
根据17年一级市场融资医药企业的细分行业分布,我们大致推算每年的总融资额大约有30%被投入到新品种的研发中。根据454个融资事件中有接近一半是A轮融资,我们假设融资资金使用3年。测算得出,18-20年一级市场融资对CRO行业增厚近百亿收入。
18-20年一级市场融资对CRO行业增厚近百亿收入
数据来源:公开资料整理
4)预计国内CRO行业18-20年仍将保持近20%增长
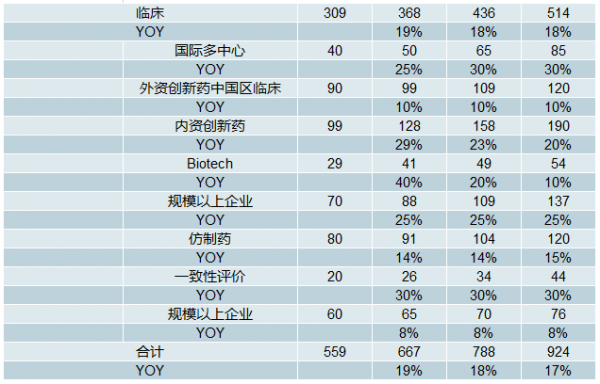
预计我国CRO行业18-20年增速仍接近20%。根据药审数据、开展临床情况、相关公司财务数据等,我们对CRO行业各细分子板块的规模、增速进行了预测,如表18所示。预计我国CRO行业18-20年增速仍接近20%,创新药外包需求占比将持续提升。
预计18-20年CRO行业保持接近20%增长

数据来源:公开资料整理
相关报告:智研咨询发布的《2019-2025年中国CMO行业市场潜力现状及投资战略研究报告》

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询



















![趋势研判!2026年全球车辆铰接系统行业产业链、市场规模、竞争格局及发展趋势:市场规模将突破20亿元,本土企业迅速崛起,“一超多强”格局正在重塑[图]](http://img.chyxx.com/images/2022/0330/dd2a6e2dd1963d26c8672c625ba6166e69bd4120.png?x-oss-process=style/w320)
![2026年全球智能泳池设备行业政策、产业链、市场规模、竞争格局及发展趋势研判:市场规模呈现持续增长态势,有望突破40亿美元[图]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)
![研判2026!中国透明质酸钠行业性质、生产工艺、产业链、市场规模及发展趋势分析:从传统保湿到前沿再生,技术创新重塑透明质酸钠应用版图[图]](http://img.chyxx.com/images/2022/0330/d1363a7ee3953fc25ed09e0b79158acce9dc7c22.png?x-oss-process=style/w320)
![趋势研判!2026年中国冶金煤行业政策、供需情况、市场规模、重点企业及发展趋势:冶金煤供不应求结构性短缺特征明显,市场规模增速有所放缓[图]](http://img.chyxx.com/images/2022/0408/54b870b64f647f1fc10474b02796382c9242dcfa.png?x-oss-process=style/w320)
![研判2026!中国商业航天行业相关政策、发射情况、企业布局及融资情况分析:从“补充”到“主导”,多款新型号首飞在即[图]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)
