2018年6月北京北生研生物制品有限公司批签发4739425瓶,其中麻疹风疹联合减毒活疫苗批签发2250640瓶,Sabin株脊髓灰质炎灭活疫苗(Vero细胞)批签发990615瓶,口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞)批签发913590瓶,口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞)批签发584580瓶。
2018年6月北京北生研生物制品有限公司批签发产品情况
生产企业 | 产品名称 | 规格 | 批号 | 签发量 | 签发结论 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201802028 | 83100瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201802029 | 83550瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201802030 | 82020瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803031 | 83670瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803032 | 83040瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803033 | 82800瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803034 | 83580瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803038 | 83790瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803037 | 80460瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803036 | 83790瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803035 | 83790瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻疹风疹联合减毒活疫苗 | 复溶后每瓶0.5ml,每1次人用剂量为0.5ml,含麻疹和风疹活病毒均应不低于3.2LgCCID50 | 201801001 | 125570瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻疹风疹联合减毒活疫苗 | 复溶后每瓶0.5ml,每1次人用剂量为0.5ml,含麻疹和风疹活病毒均应不低于3.2LgCCID50 | 201801002 | 124870瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻疹风疹联合减毒活疫苗 | 复溶后每瓶0.5ml,每1次人用剂量为0.5ml,含麻疹和风疹活病毒均应不低于3.2LgCCID50 | 201801003 | 125000瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻疹风疹联合减毒活疫苗 | 复溶后每瓶0.5ml,每1次人用剂量为0.5ml,含麻疹和风疹活病毒均应不低于3.2LgCCID50 | 201801004 | 124590瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻疹风疹联合减毒活疫苗 | 复溶后每瓶0.5ml,每1次人用剂量为0.5ml,含麻疹和风疹活病毒均应不低于3.2LgCCID50 | 201801005 | 124990瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801003 | 125210瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801004 | 123580瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801006 | 125060瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801007 | 125060瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801008 | 125770瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801009 | 124780瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804040 | 99204瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804041 | 99444瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804045 | 99504瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804044 | 99084瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804043 | 98424瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804046 | 99405瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804047 | 99165瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804048 | 99495瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804049 | 98715瓶 | 予以签发 |
北京北生研生物制品有限公司 | Sabin株脊髓灰质炎灭活疫苗(Vero细胞) | 每瓶0.5ml,每1次人用剂量为0.5ml。含脊髓灰质炎病毒抗原量Ⅰ型15DU、Ⅱ型45DU、Ⅲ型45DU。 | 201804050 | 98175瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801010 | 125120瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801011 | 125450瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801012 | 126000瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801013 | 124010瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801014 | 125120瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801016 | 125040瓶 | 予以签发 |
北京北生研生物制品有限公司 | 麻腮风联合减毒活疫苗 | 复溶后每瓶0.5ml。每一次人用剂量为0.5ml,含麻疹和风疹病毒均应不低于3.0LgCCID50,含腮腺炎活病毒应不低于3.7LgCCID50 | 201801015 | 125420瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803039 | 83250瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803040 | 83250瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803041 | 83700瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803042 | 83550瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803043 | 83490瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803044 | 83520瓶 | 予以签发 |
北京北生研生物制品有限公司 | 口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) | 每瓶1.0ml(10人份)。每1次人用剂量为2滴(相当于0.1ml),含脊髓灰质炎活病毒总量应不低于6.12 lgCCID50,其中Ⅰ型应不低于6.0 lgCCID50,Ⅲ型应不低于5.5 lgCCID50。 | 201803045 | 83820瓶 | 予以签发 |
数据来源:中国食品药品检定研究院,智研咨询整理
2018年6月北京北生研生物制品有限公司批签发企业占比图
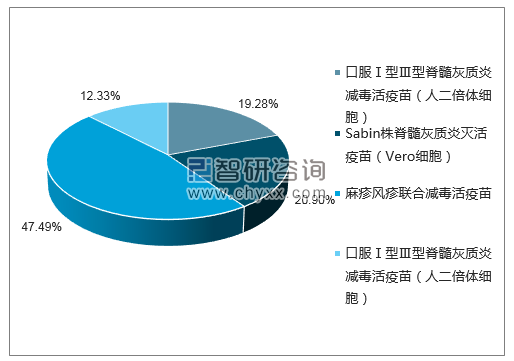
数据来源:中国食品药品检定研究院,智研咨询整理

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询
























