人乳头状瘤病毒(HPV)是一种通过性传播、皮肤亲密接触后男女均可感染的病毒。HPV主要感染于人体的皮肤与黏膜,感染后会引起人体皮肤黏膜的鳞状上皮增生,表现为寻常疣、生殖器疣等症状。根据HPV亚型致病危险性不同,可将HPV分为低危型和高危型两大类:
HPV分为低危型和高危型两大类

资料来源:智研咨询整理
低危型HPV包括HPV-6、HPV-11、HPV-34、HPV-40等常见型别,低危型HPV感染常引起生殖器疣、口腔喉部瘤等疾病。
高危型HPV包括HPV-16、HPV-18、HPV-31、HPV-33等常见型别。高危型HPV持续感染是多种癌症的主要诱因之一,其中宫颈癌最为常见,70%以上的宫颈癌是由HVP-16和HPV-18两种高危型HPV引起。
HPV疫苗是用于预防HPV感染的生物制品。HPV疫苗属于二类疫苗,需要公众自己承担接种费用。基于宫颈癌较高的发病率,且几乎所有宫颈癌是由HPV感染所致,人们习惯把HPV疫苗称为“宫颈癌疫苗”。
根据产生的作用,可将HPV疫苗分为预防性疫苗和治疗性疫苗。预防性HPV疫苗能够诱导机体产生免疫应答,在反应过程中形成中和性的抗体,当人体感染HPV前就可以与病毒抗原相结合,从而达到预防的目的。根据预防范围的不同,预防性HPV疫苗分为双价人乳头瘤病毒吸附疫苗、四价人乳头瘤病毒疫苗、九价人乳头瘤病毒疫苗三类。
预防性HPV疫苗三大类简介
分类 | 简介 |
2价HPV疫苗 | 针对预防HPV16、HPV18两种亚型HPV感染引起的疾病。该疫苗是英国GSK公司于2007年9月首次研发上市 |
4价HPV疫苗 | 针对预防HPV6、HPV11、HPV16、HPV18四种亚型HPV感染引起的疾病。该疫苗是美国默沙东公司于2006年6月首次研发上市 |
9价HPV疫苗 | 针对预防HPV6、HPV11、HPV16、HPV18、HPV31、HPV33、HPV45、HPV52、HPV58九种亚型HPV感染引起的疾病。该疫苗是美国默沙东公司于2014年12月首次研发上市 |
资料来源:智研咨询整理
目前全球商品化应用的预防性HPV疫苗对比
商品名 | Cervarix | Gardasil | Gardasil 9 |
生产商 | 葛兰素史克 | 默沙东 | 默沙东 |
覆盖亚型 | 16/18 | 6/11/16/18 | 6/11/16/18/31/33/45/52/58 |
首次上市时间 | 2007 年9 月 | 2006 年6 月 | 2014 年12 月 |
国内上市时间 | 2016 年7 月 | 2017 年5 月 | 2018 年4 月 |
宫颈癌覆盖率 | 70% | 70% | 92% |
国内获批接种人群 | 9-45 岁女性 | 20-45 岁女性 | 16-26 岁女性 |
国内中标价格 | 580 元/支 | 798 元/支 | 1298 元/支 |
资料来源:智研咨询整理
治疗性HPV疫苗能够引起特异性免疫应答,通过不同途径将抗原传递给免疫系统,激发机体的免疫反应,从而清除HPV病毒。
其中预防性HPV疫苗接种对象为健康群体,治疗性HPV疫苗接种对象为已经发生宫颈癌或癌前病变的患者,目前我国HPV疫苗市场只要是指预防性HPV疫苗。
预防性HPV疫苗与治疗性HPV疫苗对比
分类 | 预防性HPV疫苗 | 治疗性HPV疫苗 |
接种对象 | 健康群体 | 已经发生了宫颈癌及癌前病变的患者 |
研发进展 | 已经上市 | 研发中 |
目的 | 预防感染 | 治疗或防止病情恶化 |
作用机制 | 产生中和抗体 | 诱导细胞介导的免疫反应 |
资料来源:智研咨询整理
我国市场4 价和9 价HPV 疫苗占据主导地位。2017年我国HPV疫苗批签发量为145.52万支,2019年HPV疫苗批签发量增长至1087.54万支。
2017-2019年我国HPV疫苗批签发量走势图
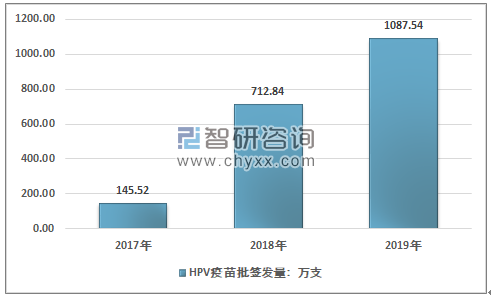
资料来源:中检所、智研咨询整理
2017-2019年我国不同类型HPV疫苗批签发量走势图
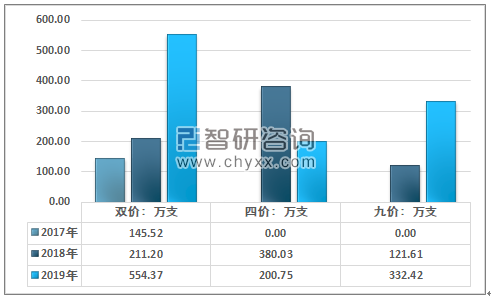
资料来源:中检所、智研咨询整理
2017年我国HPV疫苗批签发量分企业统计:支
产品名称 | 生产厂商 | 批号 | 批量 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA326AA | 274740 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA338AA | 16560 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA338AB | 253860 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA337AA | 269490 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA336AA | 292500 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | N021713 | 151664 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | N023263 | 196352 |
资料来源:中检所、智研咨询整理
2018年我国HPV疫苗批签发量分企业统计:支
产品名称 | 生产厂商 | 批号 | 批量 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R022753 | 327810 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R024259 | 35750 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R027667 | 40019 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R020226 | 306520 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R025022 | 100550 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R025064 | 100496 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R006560 | 90547 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R002424 | 8953 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R015079 | 99685 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R017837 | 99750 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R002424 | 6022 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | N033638 | 99634 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | N032635 | 121683 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | N028427 | 190689 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | N029274 | 196715 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | N026988 | 192390 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | N034531 | 226180 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | N034228 | 200925 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R002383 | 236742 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R001716 | 237750 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R005659 | 226998 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R004655 | 231702 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R006069 | 231590 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R005172 | 231814 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R013105 | 236662 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R013664 | 222438 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R014789 | 31590 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R014110 | 229927 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R010746 | 230278 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R011424 | 224566 |
资料来源:中检所、智研咨询整理
2019年我国HPV疫苗批签发量分企业统计:支
产品名称 | 生产厂商 | 批号 | 批量 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R036916 | 271556 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R036942 | 177910 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S006466 | 238848 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S004620 | 245566 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S005677 | 245478 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S017943 | 239728 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S009381 | 238481 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S014844 | 214342 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S014392 | 214402 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S014330 | 29878 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S017469 | 239850 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S025330 | 243238 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S024736 | 243348 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S019165 | 240774 |
九价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S020090 | 240774 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA390AB | 321150 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA390AA | 30960 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA391AA | 336910 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA392AA | 343950 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA387AB | 334560 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA394AB | 311010 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA386AA | 181740 |
双价人乳头瘤病毒吸附疫苗 | 葛兰素史克 | AHPVA386BA | 147190 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S027486 | 229706 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S027071 | 236340 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S028611 | 228258 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R025501 | 63830 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R025871 | 235510 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R025021 | 235581 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R024166 | 192252 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R028276 | 181280 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R029467 | 211280 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R029844 | 133440 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S016467 | 220234 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S020821 | 212064 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S013474 | 205120 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S013782 | 232824 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S015724 | 232448 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S016130 | 219786 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S005643 | 251312 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S003218 | 239504 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S008293 | 254768 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S007592 | 100400 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R035486 | 234016 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R036231 | 161551 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R031583 | 168550 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R031883 | 168800 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R034941 | 236193 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | R036122 | 9680 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S026464 | 236592 |
四价人乳头瘤病毒疫苗(酿酒酵母) | 默沙东 | S025725 | 212400 |
资料来源:中检所、智研咨询整理
智研咨询发布的《2020-2026年中国HPV疫苗行业市场前景规划及发展规划分析报告》显示: 2019年我国九价人乳头瘤病毒疫苗(酿酒酵母) 批签发量为332.42万支,占国内批签发总量的30.57%;双价人乳头瘤病毒吸附疫苗批签发量为200.75万支,占国内批签发总量的18.46%;四价人乳头瘤病毒疫苗(酿酒酵母) 批签发量为554.37万支,占国内批签发总量的50.98%。
2019年我国HPV疫苗批签发格局——按类型,万支,%
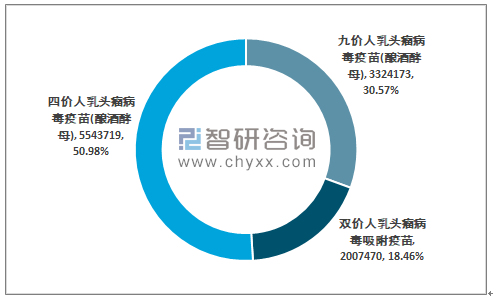
资料来源:中检所、智研咨询整理
就生产厂商而言,2019年葛兰素史克的双价疫苗批签发总量为200.75万支,占比为18.46%;默沙东的四价疫苗及九价疫苗累计批签发量为886.79万支,占比为81.54%。
2019年我国HPV疫苗批签发格局——按生产商,万支,%
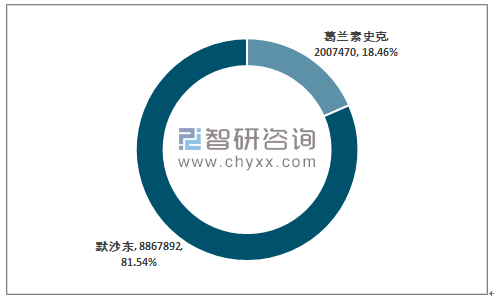
资料来源:中检所、智研咨询整理
目前我国国内企业仅有厦门万泰沧海生物技术有限公司的2 价HPV 疫苗——双价人乳头瘤病毒疫苗(大肠杆菌)已获批上市, 产品商品名为商品名馨可宁(Cecolin)。
首支国产HPV疫苗批文信息
批准文号 | 国药准字S20190047 |
产品名称 | 双价人乳头瘤病毒疫苗(大肠杆菌) |
商品名 | 馨可宁(Cecolin) |
剂型 | 注射剂 |
规格 | 每瓶0.5ml(西林瓶),含重组人乳头瘤病毒16型L1蛋白40μg,重组人乳头瘤病毒18型L1蛋白20μg。 |
生产单位 | 厦门万泰沧海生物技术有限公司 |
生产地址 | 福建省厦门市海沧区山边洪东路52号 |
产品类别 | 生物制品 |
批准日期 | 2019-12-30 |
药品本位码 | 86909593000025 |
资料来源:智研咨询整理
我国HPV 疫苗临床试验信息
试验状态 | 药物名称 | 适应症 |
进行中 尚未招募 | 重组(大肠杆菌)人乳头瘤病毒6/11型双价疫苗(剂量60ug,配比1:1) | 人乳头瘤病毒HPV6和HPV11感染及因此引发的尖锐湿疣等疾病 |
进行中 尚未招募 | 重组人乳头瘤病毒16/18型二价疫苗(汉逊酵母) | 适用于健康女性用于HPV-16和/或18型感染及相关病变的预防 |
进行中 尚未招募 | 重组九价人乳头瘤病毒(6/11/16/18/31/33/45/52/58型)疫苗(大肠埃希菌) | 适用于预防因人乳头瘤病毒(HPV)6、11、16、18、31、33、45、52、58型所致的持续感染,及由感染所致的CIN、VIN、VaIN、AIN、宫颈癌、阴道癌、外阴癌、肛门癌和生殖器疣(尖锐湿疣)等疾病 |
进行中 尚未招募 | 重组人乳头瘤病毒(6/11/16/18/31/33/45/52/58型)九价疫苗(汉逊酵母) | 接种本疫苗后,可刺激机体产生抗HPV 6型、11型、16型、18型、31型、33型、45型、52型和58型病毒的免疫力,从而预防上述型别的HPV病毒感染,进而预防由上述病毒感染所引起的子宫颈癌、阴道癌、外阴癌;预防由上述病毒感染引起的生殖器癌前病变或混合性损伤,包括宫颈癌前病变一到三期(CIN1/2/3)、原位腺癌(AIS)、外阴上皮病变一期到三期(VIN1/2/3)、阴道上皮病变一期到三期(VaIN1/2/3);预防由HPV6、HPV11感染引起的生殖器疣。 |
进行中 招募完成 | HPV双价(16/18型)疫苗 | 用于预防HPV16型和18型病毒感染,从而预防由上述病毒感染导致的子宫颈上皮内瘤样病变(CIN),进而预防子宫颈癌。 |
进行中 招募完成 | 重组人乳头瘤病毒16/18型双价疫苗(大肠杆菌) | 人乳头瘤病毒HPV16和HPV18感染及因此引发的宫颈癌等疾病 |
进行中 招募完成 | HPV(16/18 型)疫苗 | 预防人乳头瘤病毒16 和/或18 型感染及相关病变,研究群体为18-30岁健康中国女性 |
进行中 招募完成 | 重组(大肠杆菌)人乳头瘤病毒6/11型双价疫苗 | 人乳头瘤病毒HPV6和HPV11感染及因此引发的尖锐湿疣等疾病 |
进行中 招募完成 | 四价重组人乳头瘤病毒疫苗(6,11,16,18型)(汉逊酵母) | 预防人乳头瘤病毒(HPV6,11,16,18型)感染及感染导致的相关病变 |
进行中 招募完成 | 四价重组人乳头瘤病毒疫苗(6,11,16,18型)(汉逊酵母) | 预防人乳头瘤病毒(HPV6,11,16,18型)感染及感染导致的相关病变 |
进行中 招募完成 | 四价重组人乳头瘤病毒疫苗(6,11,16,18型)(汉逊酵母) | 预防人乳头瘤病毒(HPV6,11,16,18型)感染及感染导致的相关病变 |
进行中 招募完成 | 四价重组人乳头瘤病毒疫苗(6,11,16,18型)(汉逊酵母) | 预防人乳头瘤病毒(HPV6,11,16,18型)感染及感染导致的相关病变 |
进行中 招募完成 | 双价人乳头瘤病毒吸附疫苗 | 预防因高危型人乳头瘤病毒(HPV)16、18型所致的下列疾病:宫颈癌,2级、3级宫颈上皮内瘤样病变(CIN2/3)和原位腺癌,1级宫颈上皮内瘤样病变(CIN1)。 |
进行中 招募完成 | 重组三价人乳头瘤病毒(16/18/58型)疫苗(大肠杆菌) | 用于预防人乳头瘤病毒16、18和58型感染及由此导致的宫颈癌 |
进行中 招募完成 | 四价人乳头瘤病毒疫苗(酿酒酵母) | 在中国女性中预防人乳头瘤病毒16和18型别相关的宫颈癌、宫颈上皮内瘤变(CIN)1/2/3、宫颈原位腺癌。 |
进行中 招募完成 | 重组人乳头瘤病毒九价病毒样颗粒疫苗(6、11、16、18、31、33、45、52、58型L1蛋白)(毕赤酵母) | 拟用于9-45岁女性人群,以期诱导体内产生HPV6、11、16、18、 31、33、45、52 和58 型的抗体,从而预防相关型别病毒感染以及感染可能导致的生殖器疣、宫颈癌、肛门癌、阴道癌和外阴癌等。 |
进行中 招募完成 | 重组人乳头瘤病毒6/11/16/18/31/33/45/52/58型九价疫苗(汉逊酵母) | 用于健康女性用于HPV-6/11/16/18/31/33/45/52/58型感染及相关病病的预防 |
进行中 招募完成 | 重组人乳头瘤病毒6/11/16/18/31/33/45/52/58型九价疫苗(大肠埃希菌) | 人乳头瘤病毒HPV6和HPV11感染及因此引发的尖锐湿疣等疾病和人乳头瘤病毒HPV16、HPV18、HPV31、HPV33、HPV45、HPV52、HPV58感染及因此引发的宫颈癌等疾病 |
进行中 招募完成 | 重组四价人乳头瘤病毒(16/18/52/58型)病毒样颗粒疫苗(毕赤酵母) | 接种本疫苗后,可刺激机体产生抗人乳头瘤病毒的免疫力。用于预防宫颈癌。 |
进行中 招募完成 | 重组四价人乳头瘤病毒(16/18/52/58型)病毒样颗粒疫苗(毕赤酵母) | 接种本疫苗后,可刺激机体产生抗人乳头瘤病毒的免疫力。用于预防因高危HPV16/18/52/58型所致下列疾病:(1)宫颈癌(2)2级、3级宫颈上皮内瘤样病变(CIN2/3)和原位腺癌(3)1级宫颈上皮内瘤样病变(CIN1) |
进行中 招募完成 | 九价人乳头瘤病毒疫苗(酿酒酵母) | 预防由人乳头瘤病毒(HPV)6、11、16、18、31、33、45、52和58型引起的宫颈癌、外阴癌、阴道癌和肛门癌及相关癌前病变、肛门生殖器病变、巴氏检查结果异常以及持续感染。 |
进行中 招募完成 | 九价人乳头瘤病毒疫苗(酿酒酵母) | 预防由人乳头瘤病毒(HPV)6、11、16、18、31、33、45、52和58引起的宫颈癌、外阴癌、阴道癌和肛门癌及相关癌前病变、肛门和生殖器病变、宫颈细胞学检查结果异常以及持续感染。 |
进行中 招募完成 | 重组九价人乳头瘤病毒(6/11/16/18/31/33/45/52/58型)疫苗(大肠埃希菌) | 用于预防6、11、16、18、31、33、45、52、58型人乳头瘤病毒感染及由此导致的宫颈癌等相关疾病 |
进行中 招募中 | 重组人乳头瘤病毒双价(16/18型)疫苗(酵母) | 预防人乳头瘤病毒16 和/或18 型感染及相关病变 |
进行中 招募中 | 人类乳头瘤病毒吸附疫苗 | 预防HPV-16/18所致宫颈癌及癌前病变 |
进行中 招募中 | 重组人乳头瘤病毒6/11/16/18/31/33/45/52/58型九价疫苗(大肠埃希菌) | 预防人乳头瘤病毒HPV6和HPV11感染及因此引发的尖锐湿疣等疾病和人乳头瘤病毒HPV16、HPV18、HPV31、HPV33、HPV45、HPV52、HPV58感染及因此引发的宫颈癌等疾病 |
进行中 招募中 | 11价重组人乳头瘤病毒疫苗 | 预防HPV 6,11,16,18,31,33,45,52,58,59和68型别相关的持续感染和生殖器疾病 |
已完成 | 重组人乳头瘤病毒16/18型双价疫苗(大肠杆菌) | 人乳头瘤病毒HPV16和HPV18感染及因此引发的宫颈癌等疾病 |
已完成 | 重组人乳头瘤病毒16/18型双价疫苗(大肠杆菌) | 人乳头瘤病毒HPV16和HPV18感染及因此引发的宫颈癌等疾病 |
已完成 | 高危HPV持续感染组 | 高危型HPV持续感染、宫颈上皮内瘤变 |
已完成 | 重组人乳头瘤病毒16/18型双价疫苗(大肠杆菌) | 人乳头瘤病毒HPV16和HPV18感染及因此引发的宫颈癌等疾病 |
已完成 | 四价重组人乳头瘤病毒(6/11/16/18型)疫苗(汉逊酵母) | 预防人乳头瘤病毒6/11/16/18型感染及相关病变 |
已完成 | 重组人乳头瘤病毒16/18型双价疫苗(大肠杆菌) | 人乳头瘤病毒HPV16和HPV18感染及因此引发的宫颈癌等疾病 |
已完成 | 双价人乳头瘤病毒吸附疫苗 | 中国已批准Cervarix适用于9-25岁女性预防高危16型和18型人乳头瘤病毒(HPV)所致的宫颈癌、宫颈上皮内瘤样病变2级、3级(CIN 2/3)、原位腺癌和宫颈上皮内瘤样病变1级(CIN 1)。 |
已完成 | 重组三价人乳头瘤病毒(16/18/58型)疫苗(大肠杆菌) | 用于预防人乳头瘤病毒16、18和58型感染及由此导致的宫颈癌 |
已完成 | 重组人乳头瘤病毒(6/11/16/18/31/33/45/52/58型)九价疫苗(汉逊酵母) | 预防 6、11、16、18、31、33、45、52和58型人乳头瘤病毒感染所引起的宫颈癌、阴道癌、外阴癌;预防由上述病毒感染引起的生殖器癌前病变或混合性损伤,包括1级、2级、3级宫颈上皮内瘤样病变(CIN 1/2/3)、宫颈原位癌(AIS)、浸润癌、外阴上皮内瘤样病变2级、3级(VIN1/2/3)、阴道上皮内瘤样病变2级、3级(VaIN1/2/3);预防由HPV6、11型病毒感染引起的生殖器疣。 |
资料来源:药物临床试验登记与信息公示平台
万泰拥有国内首个获批的2 价HPV 疫苗。主要优势包括:1)GSK 和默沙东的HPV 疫苗均为三针法接种,万泰只需两针法接种,接种程序更简单。2)由于万泰定价更低且接种次数减少,总费用仅658 元,仅为GSK 的2 价HPV 疫苗费用的38%,为默沙东4 价HPV 疫苗费用的27%和9 价HPV 疫苗费用的17%。
中国市场HPV 疫苗接种程序和价格比较
万泰 | GSK | 默沙东 | ||
2 价 | 2 价 | 4 价 | 9 价 | |
接种人群 | 9-45 岁女性 | 9-45 岁女性 | 20-45 岁女性 | 16-26 岁女性 |
接种剂量 | 2 | 3 | 3 | 3 |
中标价(元/支) | 329 | 580 | 798 | 1298 |
总费用(每人份) | 658 | 1740 | 2394 | 3894 |
资料来源:公司公告、智研咨询整理
2020年4月21日厦门万泰沧海生物技术有限公司首批93643瓶国产双价HPV疫苗“馨可宁”取得中检所批文。目前,HPV疫苗年需求日益增加,全球一年的需求量大约在1亿支。但全世界年供应能力仅3000万剂,大约是总需求量的三分之一。
厦门万泰沧海生物技术有限公司双价HPV疫苗批文一览
产品名称 | 规格 | 批号 | 签发量 | 有效期至 |
双价人乳头瘤病毒疫苗(大肠杆菌) | 每瓶0.5ml(西林瓶),含重组人乳头瘤病毒16型L1蛋白40μg,重组人乳头瘤病毒18型L1蛋白20μg。 | 20200102 | 40302瓶 | 2022年1月14日 |
双价人乳头瘤病毒疫苗(大肠杆菌) | 每瓶0.5ml(西林瓶),含重组人乳头瘤病毒16型L1蛋白40μg,重组人乳头瘤病毒18型L1蛋白20μg。 | 20200103 | 53341瓶 | 2022年1月17日 |
资料来源:中检所、智研咨询整理
目前中国需要接种HPV疫苗的人群约3.56亿,国内也反复出现一针难求、摇号打针的情况。按照各家产品接种剂量及中标价格测算:若全部接种万泰2价疫苗,我国HPV疫苗理论市场规模高达2342.48亿元;若全部接种葛兰素史克的2价疫苗,我国HPV疫苗理论市场规模高达6194.40亿元;若全部接种默沙东的9价HPV疫苗,我国HPV疫苗理论市场规模超万亿元。
我国HPV疫苗理论市场规模测算
- | 产品类型 | 需求人群:亿人 | 接种剂量:针 | 单针价格:元 | 理论容量:亿元 |
万泰 | 2 价 | 3.56 | 2 | 329 | 2342.48 |
GSK | 2 价 | 3.56 | 3 | 580 | 6194.40 |
默沙东 | 4 价 | 3.56 | 3 | 798 | 8522.64 |
默沙东 | 9 价 | 3.56 | 3 | 1298 | 13862.64 |
资料来源:公司公告、智研咨询整理
2016年之前,我国HPV疫苗属于空白区域。2016年7月,GSK公司的2价HPV疫苗在中国上市之后,迅速开启HPV疫苗接种热潮,多处出现供不应求的现象。面对HPV疫苗供需不平衡的局面,中国药品监督管理局加快审批流程,鼓励本土制药企业研发HPV疫苗来满足市场需求。2018年4月,默沙东公司的9价HPV疫苗在中国上市,该疫苗从提出申请到获批上市仅用了8天时间。同时,中国本土制药企业也抓住HPV疫苗接种热潮,加快对HPV疫苗的研发,厦门万泰沧海生物技术有限公司双价HPV疫苗上市将是HPV疫苗进口替代的完美开端。未来,在国家财政实力不断增强、消费者接种意愿高涨等因素的推动下,中国HPV疫苗市场将快速扩容,行业市场前景巨大。
 智研咨询 - 精品报告
智研咨询 - 精品报告

2026-2032年中国HPV疫苗行业市场供需态势及发展前景研判报告
《2026-2032年中国HPV疫苗行业市场供需态势及发展前景研判报告》共十章,包含2021-2025年HPV疫苗行业投资现状分析,2026-2032年HPV疫苗行业投资机会与风险防范,研究结论及投资建议等内容。

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询



















![2022年中国宫颈癌(HPV)疫苗行业运行现状及竞争格局分析,智飞生物九价HPV疫苗批签发量为9298758支[图]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)

