随着疫情防控科技攻关的深入,急需多渠道发现更多有价值的候选药物。在抗病毒产业链中化学药分支专利申请数量最多,为 980 项,其次中药 508 项,生物药 326 项,诊断和检测 301 项,疫苗 192 项。
各主要分支专利数量
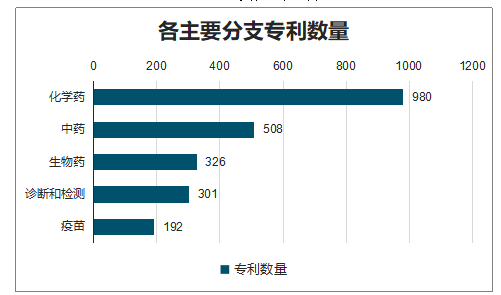
数据来源:公开资料整理
一、抗冠状病毒感染活性化合物专利申请情况
与当前疫情一样,2003 年暴发的 SARS 疫情、2012 年暴 发的 MERS 疫情,其“罪魁祸首”都是冠状病毒。抑制冠状病毒活性的化学药专利申请量与 2003 年 SARS,2009 年甲型 H1N1 流感疫情、2012 年中东暴发 MERS 疫情、2015 年韩国暴发 MERS 疫情呈正相关。同时,发现在 这类化学药专利申请中,涉及化合物结构改进研究的申请量占总量的 65.3%,开发已有化合物或其组合在抑制冠状病毒 方面用途占 26.7%,单一中药提取物或中药复方提取物占 8.0%。出于对突然暴发的疫情的紧急应对措施,将已知药物用于治疗冠状病毒感染,即“老药新用”这一创新思路贯穿 于整个技术发展过程中。
抗冠状病毒感染活性化合物申请类型与趋势
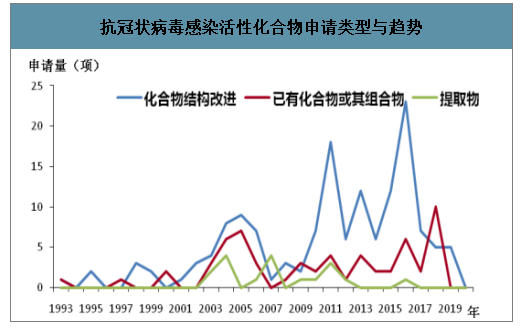
数据来源:公开资料整理
吉利德科学公司是该领域的重要申请人,重点研究领域包括人类免疫缺陷病毒(HIV)/艾滋病,肝脏疾病。代表产 品包括:替诺福韦(抗乙型肝炎病毒)、阿德福韦酯和富马 酸替诺福韦酯(抗 HIV 感染)、索非布韦(抗丙肝病毒)。在抗病毒研究方面具有较为丰富的经验。吉利德在抗 RNA 病毒领域,围绕核苷类 RNA 聚合酶抑制剂进行了专利布局,并特别注意到了对于冠状病毒感染的治疗作用。
二、冠状病毒疫苗专利申请总体情况
依据 2003 年至今国家药品监督管理局发布的获批冠状病毒疫苗的对象原理,将疫苗分为 5 类:核酸疫苗、亚单位 疫苗、灭活疫苗、减毒疫苗及病毒样颗粒。 亚单位疫苗数量最多,这与当前的病毒疫苗研究热点相匹配。 由于减毒疫苗对于病毒类型的要求比较高,并不是所有的病 毒都适宜于构建减毒疫苗,因此,从专利数量来看相对较少。
冠状病毒疫苗专利申请趋势
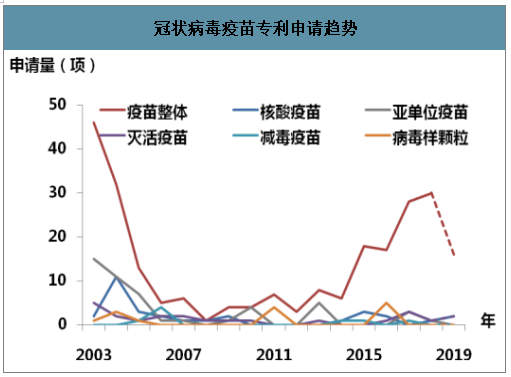
数据来源:公开资料整理
目前主要重点应当放在灭活疫苗和核酸 疫苗相对技术比较成熟的方向,而 mRNA 疫苗属于最新技术尚待发展。
三、诊断与检测专利申请
从 2003-2019 年冠状病毒检测和诊断相 关专利的整体申请趋势是先下降后升高。出现 SARS 疫情和中东呼吸综合征(MERS)时申请量明显增长,疫情结束后申 请量出现明显下落。从具体分支的申请量来看,核酸检测的 申请量比蛋白检测的申请量要高,主要是因为蛋白检测技术 难度高,而且研发的速度也相对较慢。本次抗击“新冠肺炎” 疫情的过程中,中国药监局审批通过的 7 个试剂盒均为核酸 检测试剂盒也反映出了研发速度的差距。
诊断与检测专利申请趋势

数据来源:公开资料整理
临床上针对冠 状病毒引发疾病的诊断以核酸检测为主,核酸检测方法包括 PCR、荧光 PCR、RPA、LAMP、基因芯片以及新技术等,其中 以 PCR 为主。
当前,我国抗击新型冠状病毒肺炎临床战线、疾病防控部门、药物研究机构都已针对国内外已公开且已进入临床应用、临床试验或临床前研究阶段的各种药物开展了广泛的筛选试验工作。
一级分支主要包括新冠肺炎治疗用药、 预防用药以及新冠病毒的检测诊断,二级分支分为化学药、 生物药、疫苗、检测方法和检测仪器。
技术分解表
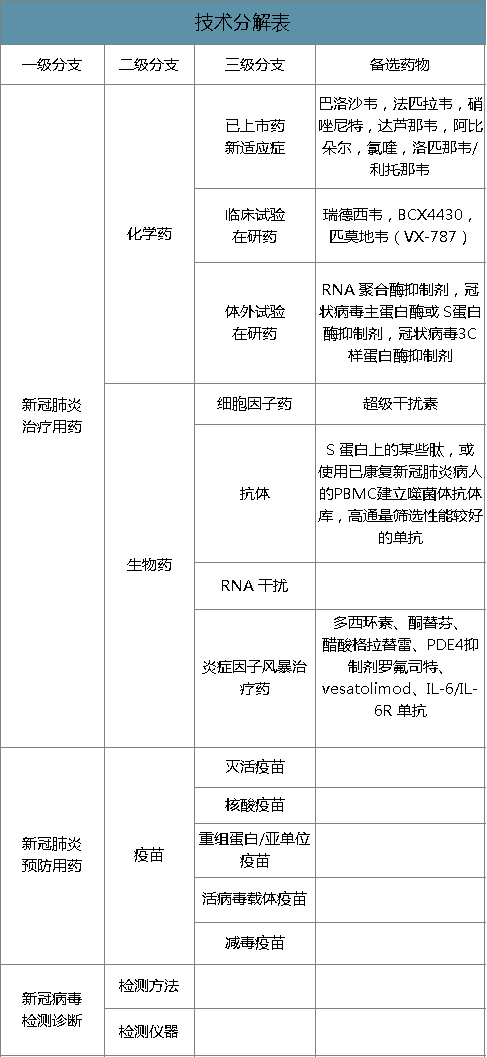
数据来源:公开资料整理
四、新冠肺炎治疗用化学药重点专利
智研咨询发布的《2020-2026年中国肺炎疫苗行业市场消费调研及投资价值预测报告》数据显示:新型冠状病毒(2019-nCoV)属于囊膜结构 RNA 病毒, 因此新型冠状病毒的化学药的筛选和研发目前主要从 RNA 阻断、囊膜阻断的机理两大方向开展,一是 RNA 聚 合酶抑制剂类药物。RNA 聚合酶抑制剂可能对所有 RNA 病毒 具有广谱的抗病毒作用,也已有许多成功的 RNA 聚合物抑制 剂药物(例如利巴韦林、法匹拉韦等)被广泛用于临床治疗, 这些药物也正被投入到抗 2019-nCoV 病毒的临床试验中。二 是冠状病毒的靶点囊膜阻断/抑制剂类药物。以冠状病毒主 蛋白酶或 3C 样蛋白酶(3C-like proteinase)、刺突蛋白酶 (S 蛋白)、血管紧张素转化酶 2(ACE2)为靶点的冠状病毒 抑制剂进行分析。三是近源性病毒囊膜阻断/抑制剂类药物。 针对与 2019-nCoV 病毒具有相同作用靶点 ACE2 受体的其它冠状病毒(SARS-CoV、HCoV-NL63),以及中东呼吸综合征病 毒(MERS-CoV)、埃博拉病毒(Ebola virus)、艾滋病病毒 (HIV)等近源性病毒通过囊膜阻断/抑制等药物作用方式进行分析。
国家卫生和健康委最新发布的《新型冠状病毒感染的肺 炎诊疗方案(试行第五版)》中提到的临床用药基本上均属于此类,包括阿比朵尔、法匹拉韦、氯喹等“老药”也进入了对抗 2019-nCoV 病毒的后备军。
与冠状病毒相关的上市药专利信息
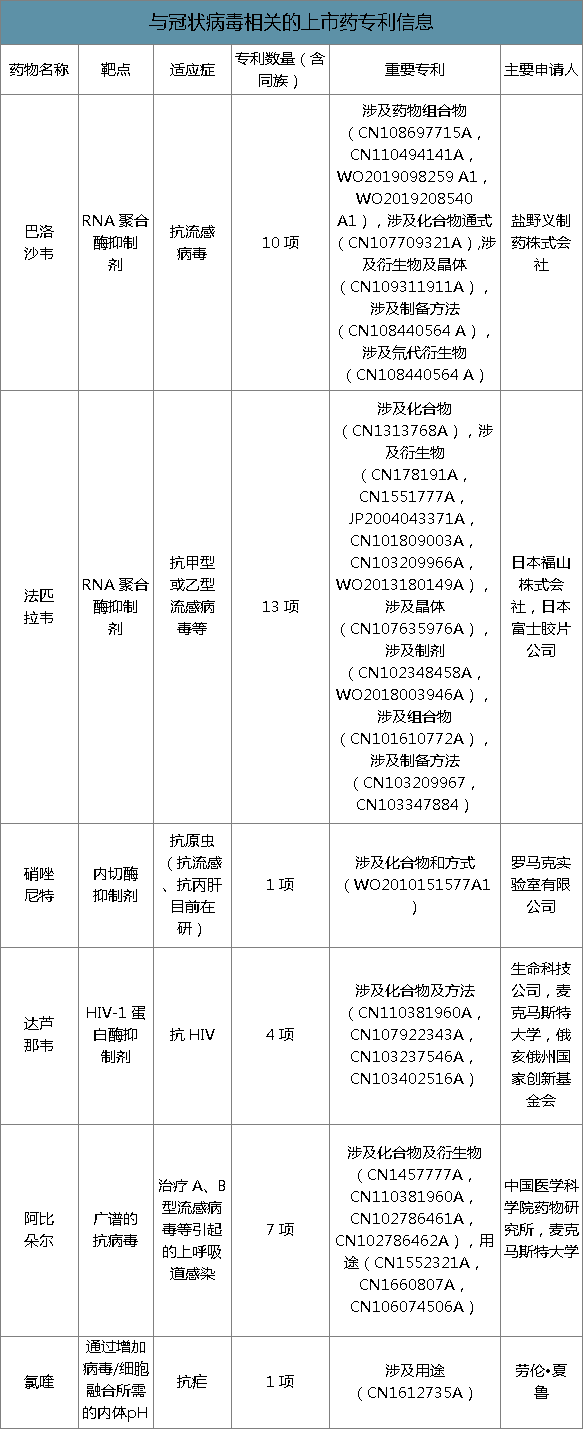
数据来源:公开资料整理
五、临床试验阶段在研化学药
抗病毒临床试验阶段的药物主要包括,瑞德西韦、 BCX4430 和匹莫地韦(VX-787)。除了瑞德西韦目前在武汉进 行针对新冠病毒的临床 III 期实验之外,其他药物分子的临 床实验均是针对其他病毒。
1.瑞德西韦
瑞德西韦(Remdesivir) 是吉利德公司在 研的一种核苷类似药物,能够抑制冠状病毒复制,原先是作 为抗埃博拉病毒药物,已经完成 II 期临床。在吉利德公司 之前的研究中,瑞德西韦被证实在体外和动物模型中,对 SARS 病毒和 MERS 病毒均有活性。2020 年 2 月 6 日,经国家 药监局、国家卫健委、科技部等多部门的批准,瑞德西韦 2019-nCoV 的相关临床试验启动。
在体外和动物模型中,瑞德西韦 证实了对非典型性肺炎(SARS)和中东呼吸综合征(MERS) 的病毒病原体均有活性。
实验数据显示 Remdesivir 及其非对映异 构体对埃博拉病毒具有较好活性,埃博拉病毒属于纤丝病毒 科,而 2019-nCoV 属于冠状病毒科。
2.BCX4430
BioCryst 医药公司开发的 BCX4430 ,是一种 广谱抗病毒药物,用于治疗出血热。属于 RNA 聚合酶抑制剂,治疗丝状病毒,包括埃博拉(Ebola)和马尔堡病毒 (Marburg)病毒,目前处于 I 期临床阶段。涉及 BCX4430 的专利申请数量共有 13 项,且大多为近年新申请。
BCX4430 相关专利申请

数据来源:公开资料整理
CN103429245B(WO2012051570A1):BCX4430 是一种 RNA 病毒聚合酶抑制剂,测量BCX4430 在多种病毒如麻疹病毒、腺病毒、登革热病毒、SARS-CoV 中的治疗活性,预防和治疗小鼠模型中对流感病毒、马尔堡病毒、埃博拉病毒感染的存活率百分比。对 SARS-CoV 的活性为视觉 CPE 测定 EC50为 14μM/ml,IC50>100,SI>7.1,中性红吸收 EC50为 16μM/ml,IC50>100,SI>6.3。
CN104379146B(WO2013158746A1): RNA 病毒聚合 酶抑制剂,广谱抗病毒活性,其中在 SARS-CoV 的活性为视 觉 CPE 测定 EC50 为 14μM/ml,IC50>100,SI>7.1,中性红 吸收 EC50 为 16μM/ml,IC50>100,SI>6.3。
3.匹莫地韦(VX-787)
VX-787 商品名为匹莫地韦是一种甲型流感病毒 RNA 聚合酶 PB2 亚基抑制剂,I 期研究证明 VX-787 具有良好的耐受性,对 Vertex 所选择的所有 A 型流感病毒株 具有强劲、快速的体外抗病毒作用,包括对奥司他韦产生耐药性的 A 型流感毒株。涉及 VX-787 的专利申请数量共有 17 项。
WO2010148197A1 公开了涉及抗 A 型流感病毒 ,基于细胞的抗病毒检测,检测了化合物对 细胞的存活的积极效应和病毒复制的抑制效应,但并未公开 治疗冠状病毒的内容。
WO2015073491A1 涉及 VX-787 的 HCl 盐·xH2O,在 细胞实验、小鼠体内实验和临床实验结果显示,病毒量减少和流感样症状减少。该专利涉及抗 A 型流感病毒,未公开治 疗冠状病毒的内容。
六、新冠肺炎治疗用生物药重点专利
对于冠状病毒治疗,生物防治药物例如细胞因子类药物同样发挥着重要作用,抗体药物与化学药物相比在抗病毒上 表现出更优异的疗效,小干扰 RNA 能特异性靶向病毒基因组以对抗病毒。
1、细胞因子药物
应用部分细胞因子的抗病毒活性刺激机体免疫细胞和 细胞因子网络从而治疗病毒性疾病,是临床研究的重点。 涉及治疗冠状病毒相关疾病的细胞因子药物的中国专利申请共计 93 项,用于冠状病毒相关疾病治疗的干扰素相 关药物专利申请共计 89 项,其他细胞因子,包括白介素、 集落刺激因子、肿瘤坏死因子和生长因子,用于治疗冠状病 毒的专利申请仅为 4 项。
细胞因子药物主要类型

数据来源:公开资料整理
通过改变IFN空间构象增强其抗病毒活性的干扰素6 项,其中 CN200910259339.2 公开的超级干扰素(sIFNα)在 体外试验中抗 SARS 的能力比普通干扰素高约 40 倍。
干扰素偶联物 6 项,对干扰素进行聚乙二醇化修饰 是较为常见的提高稳定性和延长半衰期的方法,对于干扰素 控释系统研究较少。
干扰素融合蛋白 4 项,以与白蛋白相融合为主,其中 CN201310141203.8 通过白蛋白和干扰素分子的作用区域, 使得利用白蛋白纳米粒负载干扰素成为可能,其肺部给药的 施用途径提高了药物的肺部沉积率和滞留浓度,在保持药物活性、减少副作用方面优势显著。
在针对冠状病毒的抗病毒治疗中,虽然细胞因子类药物 相关的专利申请数量和临床应用不及化合物类药物,但是由于其具备强大的免疫调节作用,对其进行的基础科学研究和 药物研发仍然十分活跃。细胞因子类药物的广谱抗病毒性质 也使其常常在临床上用于联合治疗。例如:国家卫建委发布 的最新版的治疗方案中将 α-干扰素雾化吸入作为推荐的抗 病毒治疗手段,目前已有 4 项使用细胞因子药物的临床试验 进行了注册,其使用的细胞因子药物包括重组细胞因子基因 衍生蛋白、干扰素 α1b 和干扰素 α2b。
2、抗体
对于 SARS-CoV,存在康复期血浆、动物血浆、卵黄抗体和单克隆抗体共四类方案,对于 MERS-CoV 仅有单克隆抗体一类方案,其中康复期血浆方案存在着血浆来 源有限而无法大规模应用问题,动物血浆方案由于动物抗体 在人体中的免疫原性以及成分复杂性而有潜在的安全性问 题,卵黄抗体方案的技术门槛较低,但针对冠状病毒感染的治疗活性仍待确认。单克隆抗体方案是当前治疗性抗体开发 的主流方案,具有作用机理明确、技术成熟和可以规模化生 产的优点。在单克隆抗体方案的国内专利申请人中,尚没有国内商业性抗体公司。
3、炎症因子风暴治疗药物
新型冠状病毒等感染后的重症肺炎,容易触发炎症因子风暴,对此类重症肺炎,临床缺乏特效的干预方法。涉及治 疗细胞因子风暴、炎症因子风暴或高细胞因子血症的中国专利申请共计 47 项,密切相关的重要专利申请 18 项,涉及化 学类药物 9 项,涉及生物药的有 8 项,涉及中药 1 项,筛选出了具有预防或治疗新型冠状病毒肺炎重症细胞因子风暴的可能性药物。
(1)、化学类药物
吉利德研发的 TLR7 激动剂抗病毒药 vesatolimod 对应的专利(CN201611005893.4)公开能有效的抑制 EV71 病毒 的复制,抑制自然杀伤细胞和巨噬细胞扩增,减少细胞因子 的分泌,减轻由于细胞因子风暴所导致的肌体损伤,全球范 围内有 7 项临床试验分别用于治疗艾滋病、乙肝和丙肝等病 毒感染。
CN201780068796.6 公开使用酮替芬治疗高细胞因子血 症,稳定肥大细胞膜,降低炎性递质和细胞因子释放,临床 上也用于抑制胰腺炎加重,可以尝试用于抑制新冠肺炎的加 重。
CN201711116524.7 公开使用醋酸格拉替雷治疗发生细 胞因子风暴,且免疫抑制剂治疗无效的小鼠自身免疫性肝炎, 该药目前临床上用于治疗多发性硬化症,促进抗炎性细胞因 子的产生。
CN201910092911.4 公开使用的多环西素则是一种半合 成的四环素类抗生素,其能下调 IL-6 和 TNF-α的含量。
CN201480072359.8 公开使用 PDE4 抑制剂罗氟司特治疗 病毒感染引起的细胞因子风暴,该药在临床上用于慢阻肺的 抗炎应用,包括抑制炎症介质释放和抑制免疫细胞激活在内 的广泛抗炎活性。
(2)、生物类药物
CN201811453328.3 和 CN201080061920.4 分别公开使用 了 IL-6 受体的抗体和 IL-6 抗体治疗细胞因子风暴。IL-6 是炎性因子的标志,目前国内上市的有罗氏开发的治疗类风湿 性关节炎的托珠单抗(IL-6R 单抗),该药在美国获批治疗细 胞因子释放综合症。嘉和生物和药明利康的 IL-6 单抗,海 正药业和百奥泰生物的 IL-6R 单抗等也在开展临床试验。
CN201080030275.X 和 CN200980153815.0 公开使用 TLR3 单抗治疗细胞因子风暴。口服 TLR3 单抗(TAO1)用于治疗 上呼吸道 RNA 病毒感染在比利时进行了 II 期临床试验,但 目前国内无可用上市药物。
CN201780086292.7 公开使用哺乳动物防御素(阳离子多 肽),CN201680063220.6 公开使用一些小分子肽的组合物, CN201680063220.6 使用镍纹蛋白样蛋白/IL-41 片段治疗细 胞因子风暴,可在药物研发时参考。
候选的生物药有 IL-6/IL-6R 单抗,例如罗氏的 托珠单抗、哺乳动物防御素和一些小分子肽组合物。另外, TLR3 单抗和镍纹蛋白样蛋白/IL-41 片段及其单抗等可考虑 作为药物研发方向。
4、RNA 干扰素
涉及冠状病毒感染治疗领域 RNA 干扰技术的中国专利申 请共 51 项,代表性专利见表 3-3。分析表明:国外申请人的 重点关注与 RNA 靶基因开发及 RNA 递送系统相关,而我国更 专注针对 SARS 病毒的不同靶标的 siRNA 的开发。
七、新冠病毒检测方法
与以往发现的冠状病毒不同,2019-nCoV 是以前从未在人体中发现的冠状病毒新毒株。随着疫情的发展,科研人员不断探索检测该病毒的方法,而且国家药品监督管理局已批准多个新型冠状病毒核酸检测试剂盒产品,并将其用于临床诊断。在常规的病毒检测方法中,免疫检测和核酸检测,以其高效的检测速度和准确性被普遍采用。通过对选取的 254 项专利或专利申请进行技术热点的分析,同样发现,快速检测病毒抗体或抗原的免疫学诊断方法仍然是病毒检测研究的重点,这与免疫学诊断方法相对于其他方法更为快捷方便有关;而核酸检测法由于其极高的准确度。各检测方法中的基本原理并没有太大变化,但在提高检测效率、精度以及扩展检测适用条件方面进行了不断改进。
1、免疫学检测法
CN1177224C 将 SARS 冠状病毒全病毒裂解液作为包被抗 原用于检测,CN1483737A 重组表达了 SARS 病毒特有蛋白质 和多肽片段,但后者通过具有特定氨基酸序列的蛋白质来测 定抗体,相对于 CN1177224C,其特异性和灵敏度有了进一步 提升。通过抗原表位筛选、蛋白重组表达等手段可以有效提 高血清免疫学检测的特异性和灵敏度。
CN102690336A 将蝙蝠 SARS 样冠状病毒的刺突蛋白(S 蛋白)切割成多段,免疫动物后,利用完整 S 蛋白的单克隆 抗体鉴定小鼠抗 S 单克隆抗体表位,并制备相应的检测用抗 体。CN100504391C 中利用基因工程重组抗原,获得了 SARS 冠状病毒 S、N、M、E 蛋白,并制备了偶联上述蛋白的抗体 的免疫微球。JP2017145246A 以 MERS 冠状病毒最为保守且明 显区别于其他冠状病毒的 NP 蛋白肽作为免疫原制备检测抗 体。WO2019066389A1 将 MERS 冠状病毒的 NP 蛋白的 N 端和 C 端构建融合蛋白,免疫小鼠并筛选单克隆抗体,用于 MERS 病毒感染的检测。上述对血清抗原的检测相对于血清抗体的 检测,能够在检测对象病毒感染初期即作出诊断,在病毒暴 发高峰阶段半定量地区分阳性或阴性样本。
US10421802B2 将健康人 PBMC 构建噬菌体抗体库,以 S 蛋白受体结构域(RBD)淘选富集单克隆抗体,但以康复病 人的 PBMC 构建抗体库,淘选效率会更高。 US2010075300A1 将接受病毒疫苗的人类患者的接种前和接种后的血清样品施加到包被有病毒样颗粒(VLP)的生 物传感器芯片上进行检测。该专利申请的研究重点在于:对待测病毒样颗粒进行构建,以提高检测的灵敏度同时降低生物风险;对检测平台本身的改进,同样在于提高检测灵敏度和检测速度。
2、核酸检测法
主要是改进 RT-PCR 的灵敏度和特异性,例如 US2018127836A1 鉴定了冠状病毒在感染细胞中存在的高拷贝数的高度保守的若干短 RNA 序列,例如非翻译区的前导序列,这些前导序列是 MERS 冠状病毒基因组中表达最丰富的 基因区域,可以引入锁核酸探针对其进行 RT-PCR LNA 扩增, 可以考虑增加前到序列作为检测靶标。US2019203280A1 公开了一种增加核酸扩增灵敏度和特异性的方法,包括添加失活 的 cas9 和结合于靶基因的引导 RNA(CRISPR 介导的生物敏 感器)。US2011027862A1 公开了在含有 SARS 等冠状病毒 RNA 的样本中加入盐酸胍和不超过 20mM 的金属离子,能够稳定 RNA,可考虑用于检测样本的运送过程中。US10301675B2 使 用苏拉明、Sso7d、AluI 甲基化酶和/或 poly(rA)(dT)n 等物 质减少 RT-PCR 中的逆转录抑制。WO2013049891A1 通过将不 同大小的珠粒子集标记不同的特异性核苷酸探针来实现呼 吸道病原体的检测,实现了菌体或病毒的高通量筛选,解决 了目前 PCR 缺乏有效地处理大量含多个靶的样品的高通量检 测能力的问题。该专利技术明确指出了包含珠粒的 PCR 系统 可能会成为 RT-PCR 的一个发展方向,也为大样本、高通量 检测提供了技术启示。
WO2019178188A1 提供了一种面向使用者的即时床旁诊 断系统,用专门设计的引物组和探针进行重组酶聚合酶测定 (RPA),可实现包括 SARS 在内的多种病毒的即时床旁检测。 该专利申请实际上也提出了一种设想,即将便携式的检测设备设置在隔离空间,利用物联网技术将其与诊断中心相连;在检测时,患者在隔离空间内自行提供样品(例如鼻拭子、 唾液或痰液),设备检测出数据后传送给诊断中心;再由诊断中心的医师给出结论。这样的设置可以极大地减轻医护人 员感染的风险,为实现快速、即时和远程检测提供了一种思 路。我国在 5G 技术方面具有世界领先的优势,实现该专利构想的技术基础已经存在,此项技术的实施无疑对提高现在的疫情防控能力以及今后的传染性疾病检测的生物安全性给出了很好的启示。
八、新冠病毒检测仪器
1、集成化小型 PCR 分析仪
集成化小型 PCR 分析仪的研发侧重于装置的全封闭、一体化,避免气溶胶的产生。集成化小型 PCR 分析仪的定位是 便于基层医院和中小型实验室的应用,因此,可以将分析仪设计成管式、卡式、盘式等,使得用户通过简单的按压、推 拉、拧动即可完成全程操作;简化信号读取装置,例如通过 线、点、变色、浊度等变化反映目标核酸的存在。
可以利用国内在制造业方面的优势,对集成化小型 PCR 分析仪的各个模块进行合理设计和布置,使得仪器的体积进 一步缩小,例如通过巧妙设置各模块的空间位置、合理优化流体管路等使得装置更加紧凑、小巧。
2、微流控 PCR 分析仪
微流控 PCR 分析仪方面的改进主要是实现整体微流控 PCR 分析仪的全封闭和紧凑化,适应 POCT(即时检测)的需 要;提高检测精度和检测通量;进一步降低生产成本。例如, 根据 CN104946510B 和 CN109072292A 所描述的,对微流控芯 片进行高度集成化和全封闭的设计,能够将病毒的提取、分 离、扩增以及在线检测集成在微尺度的芯片上,除了取样操 作外,操作人员只需要将采集好样本的微流控芯片插入配套 检测仪器中,利用卡扣结构等密封加样孔,之后所有的样品 处理和反应过程均由检测仪器自动完成,不需要人为干预, 就避免了人为操作带来的交叉污染以及气溶胶污染问题。
通过在芯片的微流体通道中设置不同温度区域, 实现温度调节,从而精确控制 PCR 分析仪的扩增环节;通过 改进流体驱动控制技术,包括微通道、微阀、微泵等的精细 加工,或采用离心力、挤压囊泡、电驱动等方式精确控制芯 片内的液体流动,从而定量控制核酸检测中的流体体积;可 以对芯片基底材料进行进一步的选择和处理,例如对基底材 料进行化学处理,使其既能适用于微流控的流体操控又能降 低生产成本。
3、自动化 PCR 检测系统
自动化 PCR 检测系统研发的重点主要是以移液平台为基础,通过集成、扩展的方式满足自动化核酸检测中的自动移 液需求;通过空气过滤、分隔空间、改进移液系统等方式防 止气溶胶污染;通过不同模块之间的传送系统、机械臂、计 算机处理系统等来实现自动化控制,使得各个模块集成化、 自动化以形成大型的工作站或者操作平台,最大限度地减少手工操作。

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询


















![趋势研判!2026年中国无人配送车行业政策、产业链、成本、市场规模、竞争格局及发展趋势:末端物流市场需求持续旺盛,派送场景不断开发,前景良好[图]](http://img.chyxx.com/images/2022/0408/54b870b64f647f1fc10474b02796382c9242dcfa.png?x-oss-process=style/w320)
![研判2026!中国海运行业货运量、运价、重点企业运力分析:中国海洋货运量稳健增长凸显核心引擎地位,港口能效升级护航贸易流通[图]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)
![研判2026!中国高压避雷器行业相关政策汇总、产业链、供需现状、竞争格局及未来发展趋势分析:供需两端均呈现高景气态势[图]](http://img.chyxx.com/images/2022/0330/4279f04d08c7260a105d321a303d34a91af3a3d5.png?x-oss-process=style/w320)
![研判2026!中国智慧城市轨道交通行业政策、产业链、市场规模、竞争格局及发展前景:智慧城市轨道交通市场规模达698.36亿元,技术融合驱动行业快速发展[图]](http://img.chyxx.com/images/2022/0330/920e1a3ff3bb6b7f469fbaa1e9ad45bc470a7578.png?x-oss-process=style/w320)
![趋势研判!2026年中国软件外包行业发展环境、产业链、市场规模、代表企业及未来趋势:受益于数字化转型需求增长,软件外包市场规模达6165.98亿元[图]](http://img.chyxx.com/images/2022/0330/83e55e0fd01cd7eb3b56b758f35281ec8d2514ab.png?x-oss-process=style/w320)
![2026年中国人工智能基础层行业产业链、发展现状、竞争格局、发展趋势研判:行业市场规模持续上涨,全栈自主可控进程持续深化[图]](http://img.chyxx.com/images/2022/0330/d1363a7ee3953fc25ed09e0b79158acce9dc7c22.png?x-oss-process=style/w320)
