一、PD-1/PD-L1抗体市场概况
(1)全球PD-1/PD-L1抗体市场规模
全球首个PD-1/PD-L1抗体Opdivo于2014年7月在日本上市,美国市场上,Keytruda于2014年9月首个上市。
根据智研咨询发布的《2020-2026年中国PD-1/PD-L1抗体行业市场现状调研及市场发展前景报告》数据显示:2018年全球PD-1/PD-L1单抗销售额162.6亿美元,同比增长66%,未来有望成为全球销售额最大的药品品类。
2014-2018年全球PD-1/PD-L1抗体市场规模走势图
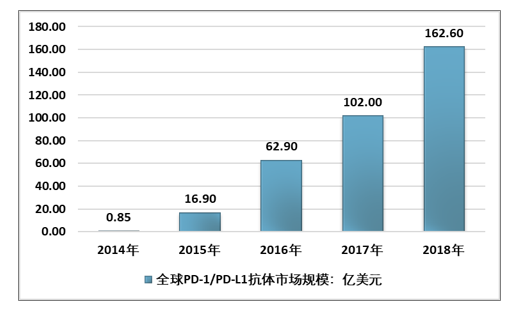
资料来源:智研咨询整理
2018年,Opdivo和Keytruda销售额分别达到75.7亿美元和71.7亿美元,同比增长32%和83%,都位居全球销售额前10大药品之列。2019年上半年,Keytruda实现收入49亿美元,已经超过Opdivo的40亿美元。
(2)PD-1/PD-L1抗体作用机制
1、促进APC激活T细胞
PD-1/PD-L1抗体通过激活人体自身的免疫系统杀伤肿瘤,能够促进APC激活T细胞抗原递呈细胞(APC)识别了肿瘤特异性抗原之后,会将肿瘤特异性抗原递呈给T细胞,激活T细胞发挥杀灭肿瘤细胞的作用。
在APC刺激T细胞活化的过程中,APC表面的PD-L1和T细胞表面的PD-1结合会抑制T细胞活化,PD-1/PD-L1抗体则能够避免两者的结合,促进APC激活T细胞。
2、帮助T细胞杀灭肿瘤
PD-1/PD-L1抗体通过激活人体自身的免疫系统杀伤肿瘤,能够促进防止肿瘤细胞免疫逃逸,帮助T细胞杀灭肿瘤。
正常细胞表面一般不表达PD-L1,但一些突变的肿瘤细胞表面会表达PD-L1,与T细胞表面的PD-1结合,抑制T细胞发挥杀灭肿瘤的作用,实现免疫逃逸。
PD-1/PD-L1抗体能够阻止肿瘤细胞表面的PD-L1与T细胞表面的PD-1结合,帮助T细胞杀灭肿瘤。
二、中国PD-1/PD-L1单抗发展现状
(1)PD-1/PD-L1单抗市场进入商业化阶段
国内PD-1/PD-L1单抗市场已经从药物研发阶段进入药物商业化阶段。2018年6月15日,纳武利尤单抗(Opdivo,BMS)获得NMPA批准上市,成为国内首个获批上市的PD-1单抗。在随后短短的1年时间内,NMPA先后批准上市了5款PD-1单抗,其中2款为进口(纳武利尤单抗(Opdivo,BMS)、帕博利珠单抗(Keytruda,默沙东)),3款为国产(特瑞普利单抗(拓益,君实生物)、信迪利单抗(达伯舒,信达生物)、卡瑞利珠单抗(艾立妥,恒瑞医药))。截止目前,另外3款PD-1/PD-L1单抗(替雷利珠单抗(百济神州)、度伐鲁单抗(Imfinzi,阿斯利康)、阿替利珠单抗(Tecentriq,罗氏))也已经向NMPA提交了上市申请。
国内PD-1/PD-L1单抗的新药申报情况
公司 | 通用名 | 靶点 | CDE受理号 | 状态 | 适应症 |
BMS | 纳武利尤单抗 | PD-1 | JXSS1700015/16 | 已批准 | 非EGFR/ALK突变的NSCLC(2线) |
BMS | 纳武利尤单抗 | PD-1 | JXSS900001/02 | 在审评审批 | |
默沙东 | 帕博利珠单抗 | PD-1 | JXSS1800002 | 已批准 | 黑色素瘤(2线) |
默沙东 | 帕博利珠单抗 | PD-1 | JXSS1800025 | 在审评审批 | 鳞状NSCLC(1线联合卡铂和紫杉醇) |
默沙东 | 帕博利珠单抗 | PD-1 | JXSS1800048 | 在审评审批 | PD-L1阳性的NSCLC(1线) |
默沙东 | 帕博利珠单抗 | PD-1 | JXSS1800018 | 已批准 | 非EGFR/ALK突变的非鳞状NSCLC(1线联合培美曲塞和顺铂/卡铂) |
君实生物 | 特瑞普利单抗 | PD-1 | CXSS1800006 | 已批准 | 黑色素瘤(2线) |
信达生物 | 信迪利单抗 | PD-1 | CXSS1800008 | 已批准 | 复发/难治性经典型霍奇金淋巴瘤(3线) |
恒瑞医药 | 卡瑞利珠单抗 | PD-1 | CXSS1800009 | 已批准 | 复发/难治性经典型霍奇金淋巴瘤(3线) |
恒瑞医药 | 卡瑞利珠单抗 | PD-1 | CXSS1900023 | 在审评审 | 批肝细胞癌(2线) |
百济神州 | 替雷利珠单抗 | PD-1 | CXSS1800019 | 在审评审批 | 复发/难治性经典型霍奇金淋巴瘤 |
百济神州 | 替雷利珠单抗 | PD-1 | CXSS1900025 | 在审评审批 | 尿路上皮癌(2线) |
阿斯利康 | 度伐鲁单抗 | PD-L1 | JXSS1800040/41 | 在审评审批 | Ⅲ期NSCLC |
罗氏 | 阿替利珠单抗 | PD-L1 | JXSS1900004 | 在审评审批 | NSCLC(2线) |
资料来源:智研咨询整理
随着PD-1/PD-L1单抗在国内的陆续上市,销售业绩是检验这类创新药物在国内市场前景的试金石。
根据纳武利尤单抗(Opdivo,BMS)和帕博利珠单抗(Keytruda,默沙东)在国内的总代理商上海医药发布的报告,截止2018年9月30日,Opdivo和Keytruda在国内市场的分销收入分别为1.9亿元(销售逾2个月)和1.5亿元(销售逾1个月);
2019年上半年特瑞普利单抗(拓益,君实生物)销售额约3.08亿元(销售逾4个月),远超预期(公司预期2019年特瑞普利单抗的销售额为4-4.5亿元);
信迪利单抗(达伯舒,信达生物)2019年上半年的销售额为3.316亿元(销售近4个月);
卡瑞利珠单抗(艾立妥,恒瑞医药)2019年三季度的销售额预计约为3亿元(销售逾2个月)。基于PD-1/PD-L1单抗在国内市场销售的良好开局,随着更多同类产品的上市和更多适应症的获批,PD-1/PD-L1单抗将成为国内创新药市场的标杆。
国内PD-1/PD-L1单抗上市后的销售情况
通用名 | 商品名 | 公司 | 批准时间 | 销售情况 |
纳武利尤单抗 | 欧狄沃(Opdivo) | BMS | 2018/6/15 | 1.9亿元(截止2018/9/30,销售逾2个月) |
帕博利珠单抗 | 可瑞达(Keytruda) | 默沙东 | 2018/7/20 | 1.5亿元(截止2018/9/30,销售逾1个月) |
特瑞普利单抗 | 拓益 | 君实生物 | 2018/12/17 | 约3.08亿元(截止2019/6/30,销售逾4个月) |
信迪利单抗达 | 伯舒 | 信达生物 | 2018/12/24 | 3.316亿元(截止2019/6/30,销售近4个月) |
卡瑞利珠单抗 | 艾立妥 | 恒瑞医药 | 2019/5/29 | 预计约3亿元(截止2019/9/30,销售逾2个月) |
资料来源:公司公告
(2)国内PD-1/PD-L1单抗形成“4+4”格局
国内已上市及正在进行中后期临床试验的PD-1/PD-L1单抗药物多达有20个,包括13个PD-1单抗和7个PD-L1单抗。BMS、默沙东、君实生物、信达生物和恒瑞医药的PD-1单抗从2018年6月开始已陆续获批上市,同时百济神州的PD-1单抗以及罗氏和阿斯利康的PD-L1单抗正在进行上市申请,预计2019年下半年能获批。
参照海外市场PD-1/PD-L1单抗的商业化进程,大概率是BMS、默沙东、罗氏和阿斯利康四家外企携手君实生物、信达生物、恒瑞医药和百济神州四家本土企业成为国内PD-1/PD-L1单抗市场的头部企业,形成“4+4”格局。头部企业将会利用先发优势分享未来国内PD-1/PD-L1单抗市场的大部分蛋糕,后入的企业只能在策略上进行差异化竞争。
国内PD-1/PD-L1单抗市场竞争格局
序号 | 药品 | 靶点 | 公司 | 国内研发进展 | 国内临床获批日期 |
1 | Opdivo | PD- | 1BMS | 2017/11/2上市申请 2018/6/15获批 | 2015/11/11(临床公示日期) |
2 | Keytruda | PD-1 | 默沙东 | 2018/2/11上市申请 2018/7/20获批 | 2016/6/6(临床公示日期 |
3 | JS001 | PD-1 | 君实生物 | 2018/3/9上市申请2018/12/17获批 | 2016/1/4 |
4 | IBI308 | PD-1 | 信达生物 | 2018/4/19上市申请 2018/12/24获批 | 2016/9/4 |
5 | SHR1210 | PD-1 | 恒瑞医药 | 2018/4/23上市申请 2019/5/29获批 | 2016/2/4 |
6 | BGB-A317 | PD-1 | 百济神州 | 2018/9/6上市申请 | 2016/9/3 |
7 | Imfinzi | PD-L1 | 阿斯利康 | 2018/12/26上市申请 | 2017/1/19(临床公示日期) |
8 | Tecentriq | PD-L1 | 罗氏 | 2019/2/25上市申请 | 2016/7/6(临床公示日期) |
9 | 杰诺单抗 | PD-1 | 嘉和生物 | Ⅱ期临床 | 2016/12/8 |
10 | KN035 | PD-L1 | 思路迪/康宁杰瑞 | Ⅱ期临床 | 2016/12/28 |
11 | GLS-010 | PD-1 | 药明康德/誉衡药业 | Ⅱ期临床 | 2017/3/15 |
12 | CS1001 | PD-L1 | 基石药业/拓石药业 | Ⅲ期临床 | 2017/7/17 |
13 | SHR-1316 | PD-L1 | 恒瑞医药 | Ⅲ期临床 | 2017/9/14 |
14 | BAT1306 | PD-1 | 百奥泰生物 | Ⅱ期临床 | 2017/9/14 |
15 | AK105 | PD-1 | 康方生物 | Ⅲ期临床 | 2017/9/14 |
16 | KL-A167 | PD-L1 | 科伦药业 | Ⅱ期临床 | 2017/9/27 |
17 | LZM009 | PD-1 | 丽珠医药 | Ⅰ期临床 | 2017/10/26 |
18 | TQB2450 | PD-L1 | 正大天晴 | Ⅱ期临床 | 2017/11/1 |
19 | HLX10 | PD-1 | 复宏汉霖 | Ⅱ期临床 | 2018/3/20 |
20 | SSI-361 | PD-1 | 安科生物 | Ⅰ期临床 | 2019/3/18 |
资料来源:智研咨询整理
(3)主要企业竞争集中在大适应症
根据国家癌症中心的数据,国内发病率最高的前五大癌症分别是肺癌、胃癌、结直肠癌、肝癌和乳腺癌。其中肺癌是我国发病率和病死率均排第一的癌症,占整体癌症发病人数的近20%。按照世界卫生组织(WHO)的病理学分类,肺癌可分为小细胞肺癌(SCLC)和非小细胞肺癌(NSCLC)。
其中SCLC约占肺癌的10-15%,NSCLC约占肺癌的85%,可细分为腺癌(40%-50%)、鳞癌(30-40%)和大细胞癌(<10%)。
中国常见新发癌症类型
- | 男性 | 女性 | ||
癌症 | 占比 | 癌症 | 占比 | |
1 | 肺癌 | 24.17% | 乳腺癌 | 17.1% |
2 | 胃癌 | 13.06% | 肺癌 | 15.02% |
3 | 肝癌 | 12.74% | 结肠癌 | 9.17% |
4 | 结直肠癌 | 10.46% | 甲状腺癌 | 8.49% |
5 | 食管癌 | 8.23% | 胃癌 | 6.86% |
6 | 前列腺癌 | 3.35% | 子宫颈癌 | 6.25% |
7 | 膀胱癌 | 2.88% | 肝癌 | 5.4% |
8 | 胰腺癌 | 2.51% | 食管癌 | 3.88% |
9 | 淋巴瘤 | 2.42% | 子宫体癌 | 3.88% |
10 | 脑瘤 | 2.32% | 脑瘤 | 3.21% |
资料来源:国家癌症中心、智研咨询整理
国内市场针对PD-1/PD-L1单抗的临床研发策略是效仿海外同类产品,先从疗效明确的小适应症(黑色素瘤/霍奇金淋巴瘤)入手,获得NMPA批准上市后再向大适应症推进,加快药物上市时间。国内头部企业针对五大适应症的癌症类型均有临床试验布局。
从临床试验布局上看,君实生物是肺癌、肝癌、乳腺癌;信达生物是肺癌、肝癌、胃癌;恒瑞医药是肝癌、肺癌、胃癌、结直肠癌;百济神州则覆盖了肺癌、肝癌、胃癌及微卫星不稳定型或错配修复缺陷型实体瘤(主要是结直肠癌)。外资药企在国内的适应症布局也是以肺癌、肝癌、胃癌为主。
肺癌适应症,是PD-1/PD-L1单抗商业化路程中继先发优势后的第二大里程碑,吸引了8家头部企业在临床试验上的多个布局;
肝癌适应症,7家头部企业均有布局,其中恒瑞医药的肝癌适应症已纳入优先审评,美国也进入了Ⅲ期临床,进度最快,其余6家也进入了临床Ⅱ/Ⅲ期;
胃癌适应症,BMS、默沙东、信达生物、恒瑞医药和百济神州的临床试验均已进入临床Ⅱ/Ⅲ期,结直肠癌有恒瑞医药和百济神州进展靠前,乳腺癌主要是默沙东、君实生物和罗氏。
综上所述,只有在肝癌方面恒瑞的进度较为领先,已进入优先审评,其它几大适应症仍处于激烈的角逐中。
(4)联合用成为临床试验的主要布局方向
从海外市场来看,罗氏等大药企利用旗下单抗药物优势,专注联合用药疗法的开发,斩获了4种肿瘤的一线治疗方案,使其PD-L1单抗的市场份额逐年增加。而在国内,头部企业凭借旗下产品线广的优势,获得更多的领先,比如恒瑞医药的PD-1单抗已经联合阿帕替尼进行了针对多种肿瘤的临床试验,临床疗效远高于单药治疗;由于卡瑞利珠单抗在肝癌临床Ⅱ期中的优异疗效,已被NMPA纳入优先审评,同时FDA也批准了卡瑞利珠单抗联合阿帕替尼治疗肝癌的Ⅲ期临床试验。
从国内PD-1/PD-L1单抗的头部企业主要中后期临床进展来看,联合用药的布局已经占据50%以上,已经成为各大药企研发的重中之重。由于PD-1/PD-L1单抗的联合用药临床疗效非常好,一方面可以增加临床试验的成功率,另一方面可以利用NMPA的有条件获批和优先审评政策,加快获批速度,抢占市场。而对于目前PD-1/PD-L1单抗研发落后的企业,联合靶向小分子药物和单抗药物凭借良好的疗效在尚未获批的适应症上获得有条件申请上市将是一个弯道超车的好机会。
国内头部企业PD-1/PD-L1单抗联合用药在主要后期临床试验中的占比

资料来源:CDE、智研咨询整理
三、发展国产PD-1/PD-L1抗体的关键
(1)专业的商业化队伍是关键
通过广泛聘用专业并拥有多年肿瘤药物销售经验的团队制定清晰的市场战略;通过市场声音(媒体及学术会分享临床数据和用药体验)和强大的学术研究数据产出提高市场的认可度;通过赠药援助和公益基金等创新支付方式确保患者的可及性,多管齐下不断扩大产品的影响力和覆盖面。外资药企凭借在国内的多年布局,具有稳定的销售团队和广泛的销售网络;4家本土头部企业中,恒瑞医药的销售团队逾1.2万人,其中肿瘤管线销售人员逾6000人,已覆盖数千家医院;而君实生物、信达生物和百济神州3家生物科技公司正处于市场开拓阶段,商业团队分别约300-600人,其中君实生物预计在2019年拓展约400家医院,信达生物的目标覆盖医院约1500家,百济神州则目标覆盖800-1000家医院。
(2)产能储备是先决条件
我国的生物制药起步较晚,大部分大分子生物药生产线仍处于较小规模。随着PD-1单抗的获批上市,面对巨大的市场需求,产能瓶颈也是制约产品商业化的一大因素。
(3)严控质量是重中之重
生物药物的分子量大,结构复杂,在生产制药过程中,细小的差异都可能导致生物制品的结构、含量等发生变化(如蛋白降解、细胞死亡等)。严格意义上讲,并不存在完全一样的生物制品,因为生物体系的复杂性,哪怕完全一样的原料和制备方法也不一定能生产出相同的生物制品。因此大分子药物的生产工艺要求比小分子药物要高很多。大分子药物的生产工艺是保障产品商业化进程的基础,在生产过程中通过开发高表达量细胞株,自主研发细胞培养基,缩短生产周期,提高生产效率可以大大降低大分子药物的生产成本;建立严格完善的产品质量标准和方法学验证体系则可以保证产品的质量
 智研咨询 - 精品报告
智研咨询 - 精品报告

2021-2027年中国PD-1/PD-L1抗体产业发展动态及投资前景分析报告
《2021-2027年中国PD-1/PD-L1抗体产业发展动态及投资前景分析报告》共十二章,包含2016-2020年PD-1/PD-L1抗体行业各区域市场概况,PD-1/PD-L1抗体行业主要优势企业分析,2021-2027年中国PD-1/PD-L1抗体行业发展前景预测等内容。

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询


















![2026年中国合成生物行业发展全景分析:下游应用从医药健康、化工材料向农业食品、能源环保全面渗透,行业已展现出巨大的应用潜力[图]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![2026年中国骨密度仪行业产业链图谱、采购总量、采购金额、获批企业、竞争格局及未来竞争趋势分析:外资品牌占据主导地位[图]](http://img.chyxx.com/images/2022/0330/e060dd24be7392f76ddd0a84489963879d953ac6.png?x-oss-process=style/w320)
![研判2026!中国物联网行业概念、市场规模、企业竞争格局分析:中国物联网产业领跑全球,AI融合驱动“泛在智联”新纪元[图]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![研判2026!中国汽车行业分类、产销量、重点企业销量分析:一季度中国汽车行业现“内冷外热”分化,出口同比激增成核心增量引擎[图]](http://img.chyxx.com/images/2022/0330/ff5315f651f3e124d0f5a156ac51655e46e5433f.png?x-oss-process=style/w320)
