相关报告:智研咨询发布的《2018-2024年中国疫苗行业设计趋势分析及市场竞争策略研究报告》
2018年6月SANOFI PASTEUR S.A.批签发1858122支,其中b型流感嗜血杆菌结合疫苗批签发1041143支,脊髓灰质炎灭活疫苗批签发816979支。
2018年6月SANOFI PASTEUR S.A.批签发产品情况
生产企业 | 产品名称 | 规格 | 批号 | 签发量 | 签发结论 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A151M | 40339 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A152M | 64405 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A531M | 90454 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A191M | 70285 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A351M | 93585 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A401M | 107760 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A201M | 17115 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A202M | 86449 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A311M | 51885 | 予以签发 |
SANOFI PASTEUR S.A. | 脊髓灰质炎灭活疫苗 | 0.5ml/。本品每1次人用剂量为0.5ml,含有脊髓灰质炎病毒1型40DU、脊髓灰质炎病毒2型8DU、脊髓灰质炎病毒3型32DU。 | P3K701M | 444373 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A161M | 108145 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A211M | 98390 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A411M | 107445 | 予以签发 |
SANOFI PASTEUR S.A. | b型流感嗜血杆菌结合疫苗 | 10μg/(含预充型注射器装稀释液0.5ml/) | P1A421M | 104886 | 予以签发 |
SANOFI PASTEUR S.A. | 脊髓灰质炎灭活疫苗 | 0.5ml/。本品每1次人用剂量为0.5ml,含有脊髓灰质炎病毒1型40DU、脊髓灰质炎病毒2型8DU、脊髓灰质炎病毒3型32DU。 | P3K101M | 372606 | 予以签发 |
数据来源:中国食品药品检定研究院,智研咨询整理
2018年6月SANOFI PASTEUR S.A.批签发企业占比图
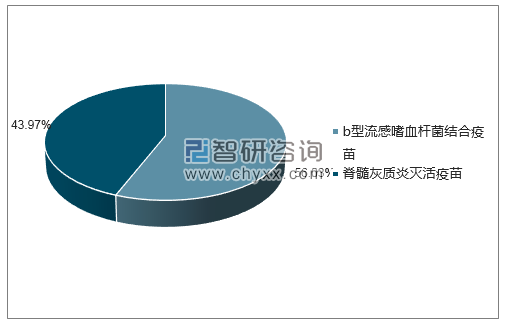
数据来源:中国食品药品检定研究院,智研咨询整理

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询
























