2018年,我国生物医药领域获得了突破性的发展,中国创新药产业开始爆发,2018年全年已有艾博卫泰、安罗替尼、硫培非格司亭、丹诺瑞韦、吡咯替尼、呋喹替尼、特瑞普利单抗和信迪利单抗8个国产新药获批上市。
2018年获批上市的国产新药
药物 | 靶点机制 | 适应症 | 公司 | 承办时间 | 批准生产 |
艾博卫泰 | 长效gp41抑制剂 | HIV | 前沿生物 | 2016/7/18 | 2018/5/23 |
丹诺瑞韦 | NS3/4A蛋白酶抑制剂 | 丙型肝炎 | 歌礼生物 | 2017/1/3 | 2018/6/11 |
安罗替尼 | VEGFR抑制剂 | 晚期肺癌 | 正大天晴 | 2017/3/16 | 2018/5/8 |
硫培非格司亭 | peg-G-CSF | 中性粒细胞减少症 | 恒瑞医药 | 2017/3/24 | 2018/5/8 |
呋喹替尼 | VEGFR抑制剂 | 转移性结直肠癌 | 和记黄埔 | 2017/6/30 | 2018/9/4 |
吡咯替尼 | HER1/HER2抑制剂 | 乳腺癌 | 恒瑞医药 | 2017/8/24 | 2018/8/14 |
特瑞普利单抗 | PD-1 | 黑色素瘤 | 君实生物 | 2018/3/20 | 2018/12/17 |
信迪利单抗 | PD-1 | cHL | 信达生物 | 2018/4/19 | 2018/12/27 |
资料来源:CDE、智研咨询整理
国产新药集中式的获批上市,一方面来自于,2017年10月中办、国办印发的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,缩短了新药临床试验审批流程。2018年7月,国家药监局又对药物临床试验审评审批做出调整:自申请受理并缴费之日起60日内,申请人未收到国家药监局药品审评中心否定或质疑意见的,可按照提交的方案开展试验。
另一方面,我国生物医药公司长期积累的技术经验有助于新药研发效率的提升,促使我国国产新药申请数量的增长。
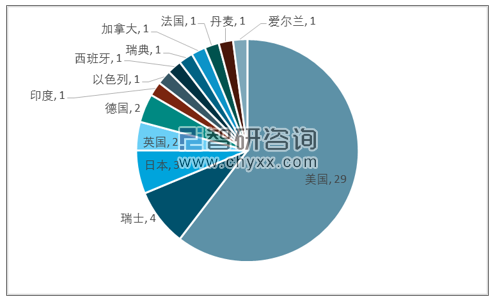
2017年FDA批准的新药以所属国家分布统计来看,美国占据了新药获批市场的绝对份额,以29个新药排名第一,第二名瑞士仅有4个。
2017年FDA批准新药国家分布
资料来源:智研咨询整理
从2017年的数据横向比较来看,中国在2018年获批8个新药上市,超过2017年瑞士一倍,同时也超越了日本、英国、德国等传统医药强国。
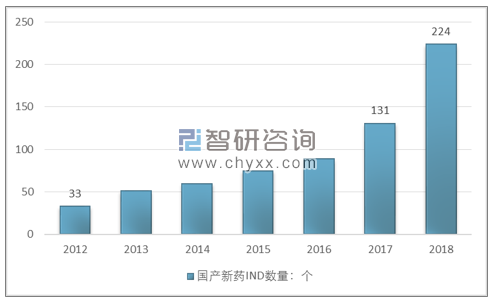
根据智研咨询发布的《2018-2024年中国高通量药物筛选与创新药物市场竞争现状及投资战略研究报告》数据显示:我国国产新药临床申请(IND)申报数量在2003-2012年的十年之间仅维持在每年30个左右,到2012年国产新药临床申请数量为33个。2012年之后我国国产新药IND申请数量开始呈现加速增长,到2017年国产新药临床申请数量增长至131个,相比2016年提升了46%,到2018年国产新药临床申请再度大幅攀升,达到224个,相比2017年提升了71%。短短三年时间,我国国产新药临床申请平均增幅逼近60%。
2012-2017年全国新药IND数量统计
资料来源:CDE、智研咨询整理
我国医药企业长期的新药研发投入在近几年逐步呈现出良好的成果表现,国产新药临床申请规模的加速提升也体现了我国新药研发实力的增强,在国内医药市场中,国产药市场以及进口替代市场有望获得可观的成长空间。
展望2019年,国产创新药的获批数量或将进一步增多。截至2019年1月2日,我国提交申请上市的国产新药数量达到了16个,包括2018年提交申请的苯烯莫德、奈诺沙星注射液、聚乙二醇洛塞那肽等15个新药申请。
有望2019年获批上市的国产新药
药物 | 靶点机制 | 适应症 | 公司 | 状态 | 承办时间 |
苯烯莫德 | 淋巴细胞激酶抑制剂 | 银屑病 | 天济药业 | NDA | 2016/12/9 |
奈诺沙星注射液 | 无氟喹诺酮抗菌素 | 社区获得性肺炎 | 浙江医药 | NDA | 2017/8/10 |
聚乙二醇洛塞那肽 | 长效GLP-1 | 2型糖尿病 | 豪森药业 | NDA | 2017/12/6 |
甲苯磺酸瑞马唑仑 | GABAa受体激动剂 | 麻醉 | 恒瑞医药 | NDA | 2018/3/21 |
优替德隆 | 抗微管蛋白聚合 | 乳腺癌 | 华昊中天 | NDA | 2018/3/28 |
卡瑞利珠单抗 | anti-PD-1Mab | cHL | 恒瑞医药 | NDA | 2018/4/23 |
KW-136 | NS5A蛋白酶抑制剂 | HCV | 凯因科技 | NDA | 2018/6/22 |
艾维替尼 | EGFR-T790M | 肺癌 | 艾森医药 | NDA | 2018/6/22 |
氟马替尼 | Bcr-Abl | CML | 豪森药业 | NDA | 2018/7/20 |
拉维达伟 | NS5A | HCV | 歌礼生物 | NDA | 2018/8/6 |
赞布替尼(双适应症) | BTK抑制剂 | CLL/MCL/WM | 百济神州 | NDA | 2018/8/29 |
替雷利珠单抗 | anti-PD-1Mab | cHL | 百济神州 | NDA | 2018/9/6 |
磷丙泊酚 | GABAa受体激动剂 | 麻醉 | 人福医药 | NDA | 2018/10/10 |
苯磺酸瑞马唑仑 | GABAa受体激动剂 | 麻醉 | 人福医药 | NDA | 2018/11/15 |
甘露寡糖二酸 | β-淀粉样蛋白等 | AD | 绿谷 | NDA | 2018/11/20 |
恩莎替尼 | ALK/ROS1抑制剂 | 肺癌 | 贝达药业 | NDA | 2019/1/2 |
资料来源:智研咨询整理
随着我国国产新药研发技术的提升,预计2019年获批的国产新药大概率超过10个,其中抗肿瘤药数量最多,有望达到7个。
2019年预计获批新药领域分布

资料来源:智研咨询整理
国产新药在全球临床试验方面,已经有多个国产创新药处于全球临床III期状态,其中万春布林的普那布林、和记黄埔的C-Met抑制剂沃利替尼、索元生物的Enzastaurin均可能成为first-in-class的品种,百济神州的BTK抑制剂赞布替尼有望成为me-better品种,贝达药业的ALK抑制剂恩莎替尼针对现有ALK抑制剂耐药的患者仍然有效。
预计2019年,普那布林、赞布替尼、恩莎替尼和贝格司亭均有望在美国提交上市申请或者完成临床试验,标志着国内创新药产业进入新阶段,创新从国内走向全球。
随着产业的繁荣发展,国内创新药正在呈现出“一超多强”的竞争态势。
从新药IND的数量来看,以恒瑞医药IND占比为例,2017年,恒瑞IND占国内的比例为10%,而2018年比例为4%。2017-2018年恒瑞医药进入研发加速期的同时,国内众多生物医药公司同样发展迅速。整体规模的加速发展也有助于我国生物医药领域在全球化的竞争中获取更有优势的竞争地位。
文章转载、引用说明:
智研咨询推崇信息资源共享,欢迎各大媒体和行研机构转载引用。但请遵守如下规则:
1.可全文转载,但不得恶意镜像。转载需注明来源(智研咨询)。
2.转载文章内容时不得进行删减或修改。图表和数据可以引用,但不能去除水印和数据来源。
如有违反以上规则,我们将保留追究法律责任的权力。
版权提示:
智研咨询倡导尊重与保护知识产权,对有明确来源的内容注明出处。如发现本站文章存在版权、稿酬或其它问题,烦请联系我们,我们将及时与您沟通处理。联系方式:gaojian@chyxx.com、010-60343812。


![研判2024!中国洗衣液行业产业链图谱、政策汇总、市场规模、重点企业及发展趋势分析:中国洗衣液市场规模持续扩大,生物科技赋能绿色洗衣[图]](http://img.chyxx.com/images/2022/0330/99d4e8a78387e45474dcca8da0b56041c69dec09.png?x-oss-process=style/w320)
![2024年中国广播电视和网络视听行业总收入、节目制作和播出时长、节目综合人口覆盖率、用户数量及行业从业人员数量统计分析:中国广电产业创收能力稳步提升,新兴业务成为拉动产业发展的重要增长极[图]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![研判2024!中国新材料行业发展历程、市场规模及细分领域现状分析:下游市场对新材料需求激增,新材料技术水平引领高新技术未来[图]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![2024年中国中央对地方转移支付及细分情况分析:中央对地方转移支付总额破10万亿 [图]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)
![2024年中国各级各类学校数量、在校生及专任教师数量分析:教育事业高质量发展持续推进,2023年在校生2.91亿人[图]](http://img.chyxx.com/images/2022/0330/ff5315f651f3e124d0f5a156ac51655e46e5433f.png?x-oss-process=style/w320)
![趋势研判!2024年中国单克隆抗体行业产业链、市场规模、竞争格局及重点企业分析:单克隆抗体市场规模超1200亿元,行业发展前景巨大[图]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)