一、肿瘤免疫治疗的分类
肿瘤免疫治疗是指应用免疫学原理和方法,通过激活体内的免疫细胞和增强机体抗肿瘤免疫应答,特异性地清除肿瘤微小残留病灶、抑制肿瘤生长,打破免疫耐受的治疗方法。肿瘤免疫治疗就是要克服肿瘤免疫逃逸的机制,从而重新唤醒免疫细胞来清除癌细胞。由于其副作用小、治疗效果明显,正逐渐成为未来肿瘤治疗的发展方向,被称为继手术、放疗和化疗之后的第四大肿瘤治疗技术。
癌症各类治疗技术优缺
治疗技术 | 优点 | 缺点 |
手术 | 适用于肉眼可见的肿瘤,治疗过程简单 | 对转移性患者治疗效果有限 |
放疗 | 能大面积杀伤肿瘤,治疗过程简单 | 对正常组织毒性大,特异性低 |
化疗 | 局部减轻肿瘤负荷,治疗过程简单 | 对正常组织毒性大,耐受性差 |
靶向药物 | 效果快,对正常组织毒性小 | 成本昂贵,耐药性问题 |
肿瘤免疫治疗 | 反应快,副作用小 | 过程复杂,价格昂贵 |
资料来源:公开资料整理
相关报告:智研咨询网发布的《2018-2024年中国肿瘤疫苗产业深度调研及未来发展趋势报告》
肿瘤免疫治疗可以广义地分为非特异性和肿瘤抗原特异性两大类。非特异性的手段包括非特异性免疫刺激和免疫检验点阻断;而肿瘤抗原特异性的方法主要是各种肿瘤疫苗和过继性免疫细胞治疗
肿瘤免疫治疗种类
种类 | 原理 | 特点 | 代表药物 |
非特异性免疫刺激 | 刺激T淋巴细胞或抗原呈递细胞来加强抗原呈递过程 | 治疗时间长、毒性和治疗肿瘤范围有限;常作为佐剂和其他疗法(如肿瘤疫苗、过继性T淋巴细胞疗法)合用 | IL-2, G-CSF |
免疫检查点阻断 | 解除肿瘤导致的免疫抑制,提高对肿瘤的杀伤作用 | 低毒,长效,但仅能解除已经位于肿瘤边缘的T淋巴细胞的束缚或加强呈递;与传统肿瘤靶向疗法和其他免疫疗法有非常好的联合用药前景 | Yervoy(CTLA4抑制剂)Opdivo(PD-1抑制剂) |
肿瘤疫苗 | 带有肿瘤特异性抗原或肿瘤相关抗原,激发特异性免疫功能来攻击肿瘤细胞 | 与免疫调节抗体有非常好的联合用药前景 | Sipuleucel-T |
过继性免疫细胞治疗 | 通过向肿瘤患者输注在体外培养扩增或激活后,具有抗肿瘤活性的免疫细胞,直接杀伤或激发机体免疫反应 | 能够特异性杀伤各类肿瘤细胞 | TIL,CAR-T,TCR-T |
资料来源:公开资料整理
非特异性免疫刺激: 包括淋巴因子激活的杀伤细胞(LAK)疗法和细胞因子介导的杀伤细胞(CIK)疗法。
LAK疗法是利用白细胞介素2(IL-2)刺激外周血淋巴细胞免疫活性细胞,这些细胞主要是由很多种淋巴细胞组成的混合体,包括NK细胞和T淋巴细胞,在体外对肿瘤具有人类白细胞抗原(HLA)非依赖型的杀伤作用,LAK细胞杀伤靶细胞的机制与NK细胞类似,可以通过细胞与细胞接触识别靶细胞表面结构,也可以通过分泌细胞因子参与杀伤肿瘤细胞。它对肾细胞癌、恶性黑色素瘤、鼻咽癌、非霍奇金淋巴瘤疗效较好,对控制微小残留灶及恶性胸腹水治疗效果比较显著。
CIK细胞由于来源于患者或健康人的外周血,培养扩增相对容易,目前已经进行肿瘤疫苗:肿瘤疫苗来源于自体或异体肿瘤细胞或其粗提取物,带有肿瘤特异性抗原(TSA)或肿瘤相关抗原(TAA),通过激发特异性免疫功能来攻击肿瘤细胞,客服肿瘤产物所引起的免疫抑制状态,增强TAA的免疫原性,提高自身免疫力来消灭肿瘤。根据肿瘤疫苗的来源,又可分为肿瘤细胞疫苗、基因疫苗、多肽疫苗、树突状细胞疫苗等。
过继性免疫细胞治疗:包括肿瘤浸润性淋巴细胞(TIL)治疗,T细胞受体嵌合型T细胞(TCR-T),嵌合抗原受体T细胞技术(CAR-T)。非特异性免疫刺激和免疫检查点单抗都是通过增强已有的免疫系统来发挥抗肿瘤作用,不能促使免疫细胞攻击肿瘤;肿瘤疫苗通过激发特异性免疫功能来攻击肿瘤细胞,但是治疗效果并不是特别好;过继性免疫效应细胞治疗,是指从肿瘤患者中分离免疫活性细胞,在体外进行扩增和功能鉴定,然后向患者转输,增强了杀伤肿瘤的免疫细胞数量,并且从而直接杀伤肿瘤或激发机体的免疫应答杀伤肿瘤细胞。治疗的特异性和靶向性是目前研究的重点和未来的发展方向,因此TCR-T和CAR-T因能够表达特异性受体靶向识别特异性的肿瘤细胞,受到广泛的关注和研究,从最开始的基础免疫研究转变为临床应用。
二、TCR-T和CAR-T的区别
T淋巴细胞是肿瘤细胞的天敌,在肿瘤免疫应答中起主要作用,对肿瘤细胞有极强的杀伤作用。但是,使用内源性T细胞进行肿瘤免疫治疗时,靶抗原需经过加工处理后才能和靶细胞表面的主要组织相容性复合物(main histocompatibility complex,MHC)作用,即“MHC限制性”。然而,肿瘤免疫编辑的过程会使MHC在肿瘤细胞表面表达下降,破坏抗原加工过程,降低肽段免疫原性。这样长期形成的免疫逃逸机制,能使肿瘤细胞成功躲避T淋巴细胞攻击,肿瘤快速增殖。此外,人体内肿瘤特异性T淋巴细胞数量较少,并且由于大多数肿瘤细胞不断表达自体抗原,使得靶向这些抗原的T淋巴细胞通过免疫耐受机制被中和或移除,数量进一步减少。因此,提高提高T淋巴细胞的识别能力的关键就在于改进“T淋巴细胞受体”,因而产生了这两种细胞免疫治疗技术:TCR-T和CAR-T。
TCR-T:TCR-T通过转导嵌合抗原受体(融合抗原结合域及T细胞信号结构域)或者TCR α/β异二聚体,来提高特异性识别肿瘤相关抗原(Tumor Associated Antigen, TAA)的TCR的亲和力和战斗力,使T淋巴细胞能够重新高效的识别靶细胞。通过输注能够识别特异靶标的基因修饰T淋巴细胞,赋予免疫系统以新的非自然免疫活性。这种方法除了能像细胞毒性化疗和靶向治疗快速杀灭肿瘤外,还避免了疫苗和T淋巴细胞检查点疗法的延迟效应。TCR基因治疗临床有效率相对较低,寻找有效的肿瘤靶抗原克隆高亲和性的TCR受体以及优化TCR的转化效率是目前的研究重点。
CAR-T:CAR-T细胞是通过基因工程获得携带识别肿瘤抗原特异性受体的T细胞,不需抗原处理和提呈,可直接识别肿瘤相关抗原,激活T细胞分泌多种细胞因子杀伤靶细胞。因此CAR-T细胞可以克服了主要组织相容性复合体限制性,同时通过 增加共刺激分子信号,增强了T细胞的抗肿瘤效应。此外,CAR-T细胞可以准确高效地定位到肿瘤靶点并长期表达,在持久抗肿瘤作用中比单克隆抗体更有效。
TCR-T和CAR-T这两种技术的一个共同点在于通过基因改造的手段提高T细胞受体对特异性癌症细胞抗原的识别能力和进攻能力。因此也都统称为“T细胞受体重新定向”技术(T cell receptor redirection)。但两者所使用的方法是不同的。TCR-T只是通过转入靶向识别基因来使T细胞获得抗癌效果,而CAR-T使TCR头部直接换成特异性的抗体,对T细胞的改动更大,这样就可以让T细胞就在抗体的指引下直接进攻癌细胞。
TCR-T和CAR-T比较
免疫治疗技术 | 原理 | 特点 |
TCR-T | 通过输注能够识别特异靶标的基因修饰T淋巴细胞,赋予免疫系统以新的非自然免疫活性 | 识别加工递呈的抗原,应用范围广泛,能够识别胞浆内部抗原 |
CAR-T | 通过基因工程获得携带识别肿瘤抗原特异性受体的T细胞,能够以非MHC限制性的方式识别和杀伤肿瘤细胞 | 不需要抗原递呈,靶向性克服免疫逃逸,存活时间较长 |
资料来源:公开资料整理
三、CAR-T疗法开启肿瘤治疗新时代
1、CAR-T细胞的发展历程
CAR-T技术的原理就是通过基因工程技术将能够识别和结合特异性肿瘤抗原的单链抗体与T淋巴细胞内的信号分子进行融合,通过病毒载体或转座子系统等转染T淋巴细胞,使T淋巴细胞表面表达嵌合抗原受体。转染后经过纯化和大规模扩增后的T淋巴细胞,即CAR-T细胞,可以特异性识别和结合肿瘤细胞表面的抗原并裂解肿瘤细胞,使效应T淋巴细胞的靶向性、杀伤活性和持久性较常规应用的免疫细胞大幅提高,并可克服肿瘤局部免疫抑制微环境,从而打破宿主免疫耐受状态,杀灭肿瘤细胞。
CAR-T细胞的组成包括抗原结合区、跨膜链接区和胞内信号区三个部分。胞外区主要是单克隆抗体的单链可变区序列(scFv),可识别肿瘤特异性抗原;胞内区主要是T细胞受体CD3的ζ链或者是免疫球蛋白Fc受体的γ链(FcRγ),向细胞内转导胞外识别的信号。
第一代CAR-T:1989年,Gross及其团队第一次提出了“嵌合受体”的概念,他们将T细胞受体(TCR)的可变区用单链抗体(scFv)替代,由此得到了具有抗原靶向性的T细胞,经改造后的T细胞不再具有MHC的限制性,上述嵌合受体的形式已经基本形成了第一代CAR-T细胞的雏形,该类T细胞基本解决了由于肿瘤细胞MHC I丢失而产生的免疫逃逸问题。随后,在上述“嵌合受体”的设计基础上,第一代CAR的结构基本确立——由能够特异性识别某个肿瘤相关抗原的scFv与T细胞内信号传递结构域CD3ζ或是FcRγ(Fc-gamma receptor)进行组合。
第二代CAR-T:为了增强T淋巴细胞在体内持续增殖的能力,第二代CAR-T将共刺激分子如CD28、CD137、CD134和ICOS等重组到CAR的胞内区,有效增强了识别肿瘤相关抗原的活性,促进T细胞活化增殖和白细胞介素2的分泌,从而杀伤肿瘤细胞。
第三代CAR-T:第三代CAR-T的CAR胞内区增加了两个共刺激分子,在体外实验中比第二代有更强的抗肿瘤效应。研究表明联合CD28-4-1BB 或者CD28-OX40 的CARs能够持续激活T 淋巴细胞。第三代CAR可增强PI3激酶信号转导通路的活性,并上调抗凋亡蛋白如Bcl-Xl的表达,使T细胞活化增殖能力增强。然而过强的共刺激分子可引起信号泄露和致死性的细胞因子风暴。此外,第三代CAR-T细胞可能会下调信号转导的阈值,导致T细胞未经抗原刺激便可激活,从而杀伤周围的正常组织细胞。
第四代CAR-T:近年来,为解决第二、三代CAR-T存在的脱靶等毒副作用,第四代CAR-T技术已经在开发。第四代CAR-T,也称为TRUCKs(T cells redirected for universal cytokine killing);这种被改造后的T细胞可以在CAR识别靶抗原后,通过激活下游转录因子NFAT(nuclear factor activated T cells)来诱导表达促炎性细胞因子白细胞介素-12(IL-12),从而招募环境中的其他免疫细胞(树突状细胞、吞噬细胞和自然杀伤细胞等)参与对不表达靶抗原的肿瘤细胞的清除。此外,被募集在肿瘤附近的免疫细胞还可以通过分泌某些细胞因子(如干扰素-γ、肿瘤坏死因子-α、IL-4和IL-5等)来调节肿瘤附近的微环境,解除其免疫抑制性,通过调动机体自身免疫力参与对肿瘤的杀伤。
2、CAR-T细胞的构建
合理筛选T细胞:CAR-T细胞可以是病毒特异性的,也可以是非病毒特异性的。研究表明,病毒特异性的CAR-T细胞不会增加治疗风险,并且体内存活时间和抗肿瘤活性均优于非病毒特异性的CAR-T细胞。初始T细胞经抗原刺激后可产生效应记忆T细胞或中枢记忆T细胞(TCM),TCM在体内可以建立长久免疫细胞记忆应答。因此,可以构建病毒特异性TCM进行CAR转导,形成双特异性CAR-T细胞,从而持久高效地杀伤肿瘤细胞。
安全高效的基因转导:逆转录病毒和慢病毒是常用的基因转导载体。相比逆转录病毒,慢病毒拥有接近100%的转导率,可感染增殖或未增殖的细胞,可引起持久稳定的基因表达,这些独特的优势使其得到广泛应用。然而病毒载体转导设备要求严格、费用高,并且可能因插入基因突变而导致细胞癌变,目前非病毒载体转导技术受到越来越多的关注。睡美人转座子系统可以将DNA质粒整合到人类初始T细胞中,使得CD19特异性CAR基因得到稳定高效表达,成为除病毒载体之外的另一理想选择。此外,将体外转录编码CAR的mRNA通过电穿孔整合入T细胞,可实现快速高效表达,并且没有改变T细胞的染色体结构,这种非整合的方式对T细胞基因修饰提供了一种比病毒载体更安全更经济的选择。
四、CAR-T疗法技术分析
1、CAR-T疗法优势
CAR-T疗法具有多种传统药物不具备的优点。相较于化疗药物和靶向药物,CAR-T的靶向性更强,并且可以通过技术修饰达到多靶向的目的。对于相同的靶点,CAR-T细胞均可进行特异性结合。由于CAR-T细胞中加入促进T细胞增殖与活化的基因序列,能保证T细胞进入体内后还可以增殖,可以长期在体内存活,使患者具有长期的免疫功能。
CAR-T疗法优势
优势 | 特点 |
靶向性强 | 由于CAR-T细胞是应用基因修饰病人自体的T细胞,利用抗原抗体结合的机制,能克服肿瘤细胞通过下调 MHC分子表达以及降低抗原递呈等免疫逃逸,让肿瘤细胞无所逃遁 |
多靶向 | CAR-T既可以利用肿瘤蛋白质抗原,又可利用糖脂类非蛋白质抗原,扩大了肿瘤抗原 靶点范围,并且CAR-T细胞作用过程不受MHC的限制 |
杀瘤范围广 | 鉴于很多肿瘤细胞表达相同的肿瘤抗原,针对某一种肿瘤抗原的 CAR 基因构建一旦 完成,便可以被广泛利用 |
效果持久 | 新一代 CAR-T 结构中加入了促进T细胞增殖与活化的基因序列,能保证T细胞进入 体内后还可以增殖,CAR-T 细胞具有免疫记忆功能,可以长期在体内存活 |
资料来源:公开资料整理
2、CAR-T疗法的临床应用
CAR-T疗法临床试验进展
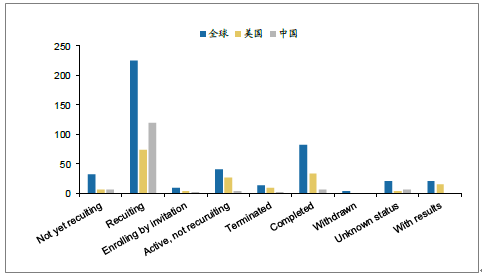
对于CAR-T细胞临床试验,截止2017年11月31日,全球目前注册的CAR-T临床研究项目一共有427个,美国以155项研究位列第一位,中国以145项位列第二。中美两国开展的CAR-T疗法临床试验占全部的70%以上。
在全球研究项目中,有226个项目都在临床招募中,超过项目总量的50%。已经完成的项目共有82个,其中21个项目拿到结果。美国的研究项目中,尽管招募中的项目占据多数,但可以看到,美国已经完成的研究项目有34项,其中15个项目拿到了结果。而中国已经完成的项目只有6个,并且目前尚未有项目拿到结果。中国的CAR-T研究正处于蓄势待发的状态。中国在招募中的临床研究项目占项目总数的83%,另外还有3个项目在积极准备中,或许一大批研究成果将在未来3-5年陆续出现。
CAR-T的临床申报分布情况(单位:项)
资料来源:公开资料整理
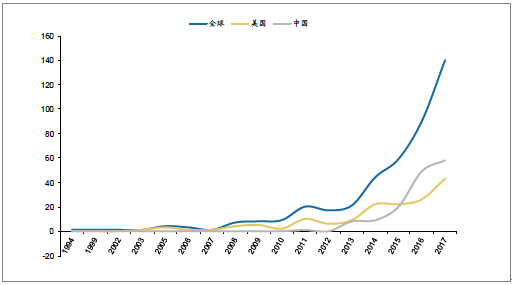
CAR-T的临床申报各年新增数量(单位:项)
资料来源:公开资料整理
最早登记的项目是丹麦国王医院与伦敦大学合作的关于HIV的前瞻性研究。该项目是一项长期的观察性试验,自1994年启动以来,已经先后有10组患者进入试验。该研究是目前欧洲最大的研究项目,在以色列、阿根廷等35个国家多2万多名患者进行了随访。这是一项持续性的研究项目,预计将在2030年12月完成。
全球的CAR-T研究从2008年、2009年开始正式起步,并且随后逐年上升,到2013 年正式爆发。其中,2013到2014年年增长数量为23项,2015到2016年年增长量为31项,2016到2017年年增长量为50项。美国CAR-T研究正式起步时间大约在2010、2011年。但从每年项目增长数量来看,美国的CAR-T研究一直处于一个相对平缓增长状态。除了2013到2014年出现翻倍增长以外,其他时间新增研究项目的浮动较小。
中国最早的CAR-T研究项目开始与2011年,由北京协和医院李太生教授主导。该研究是一项试验性研究,旨在评估雷公藤总苷在HIV治疗中对T细胞免疫激活和免疫激活的影响。该研究一共招收了23名患者,于2013年结束。从每年的新增研究数量来看,中国较全球来说起步时间晚,但变化趋势与全球趋势相似。中国的CAR-T 研究在2012、2013年起步,随着生物医药的全球化趋势,中国的CAR-T研究迅速猛增,其中2015到2016年就增长了29项,远超美国的同年增长数4项。美国市场已经出现了两极分化,涌现出了比如诺华,Kite,Juno这样的领先玩家,而中国市场正快马加鞭,涌现多家布局CAR-T的企业。
3、中国CAR-T临床试验进展
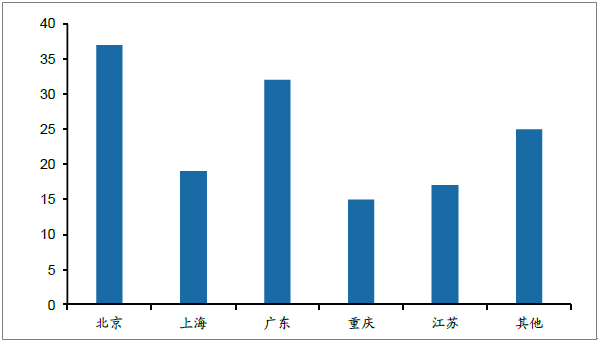
CAR-T试验正在中国各地医院开展,这些试验主要在北京、上海、广东、重庆和江苏等地的主流医院进行。国内开展临床最多的医疗机构主要有中国人民解放军总医院、第三军医大学西南医院、上海交通大学医学院附属仁济医院等,而南京传奇生物科技有限公司、上海斯丹赛生物技术有限公司等十多家企业也正在开展CAR-T产品开发,涉及的适应征包括急性淋巴白血病、骨髓瘤、淋巴瘤、乳腺癌、成神经细胞瘤、恶性胶质瘤等,有一些临床试验已取得了显著疗效。其中南京传奇生物科技有限公司今年6月在2017美国临床肿瘤学会年会上报告称,该公司开发的CAR-T产品LCAR-B38M对35名既往治疗后复发的多发性骨髓瘤患者进行临床试验,接受治疗后病情缓解率达到100%,有5位观察期已超过一年,骨髓中检测不到癌细胞,疗效显著优于美国的临床试验结果。
CAR-T试验在中国的分布(单位:项)
资料来源:公开资料整理
4、CAR-T疗法的临床研究方向
无论是全球市场、美国市场,还是中国市场,CAR-T研究中,关于组织学类型肿瘤和免疫系统疾病研究数量最多。组织学类型肿瘤和免疫系统疾病属于两个大类型的疾病,组织学类型肿瘤就包括上皮组织肿瘤、间叶组织肿瘤、结缔组织肿瘤等。这两个类型的研究数量说明了CAR-T研究的整体研究的方向。
就单一病种来看,淋巴瘤、非霍奇金淋巴瘤、白血病、HIV的相关研究数量最多。原因可能是就目前的医疗水平来说,这些病种相当棘手,保守性和平缓性的治疗方案作用不大,CAR-T疗法在对急性白血病和非霍奇金淋巴瘤的治疗,有着显著的疗效。因此,从患者刚需和可行性来说更强,市场也更可观。
CAR-T在研项目的研究方向种类与数目(单位:项)
研究类型 | 全球 | 美国 | 中国 |
组织学类型肿瘤 | 204 | 85 | 95 |
免疫系统疾病 | 186 | 73 | 67 |
淋巴组织增殖性疾病 | 140 | 56 | 64 |
免疫增生性疾病 | 140 | 56 | 64 |
淋巴瘤 | 128 | 45 | 64 |
非霍奇金淋巴瘤 | 128 | 45 | 64 |
白血病 | 111 | 40 | 56 |
HIV | 93 | 23 | 5 |
资料来源:公开资料整理
5、CAR-T临床试验抗原靶点
通过改变特定的抗原靶点元素,CAR-T细胞的特异性可以很容易地靶向特定类型的恶性肿瘤。这使得CAR-T细胞疗法被广泛的应用。许多抗原以这种方式成为靶点。越来越多的抗原被设计成CAR-T细胞,导致大量的CAR-T细胞被用于探索实体瘤和血液恶性肿瘤的治疗。
CAR-T临床靶点汇总
临床靶点 | 肿瘤类型 |
CD19 | 非霍奇金淋巴瘤、急性淋巴细胞白血病、慢性淋巴细胞白血病、霍奇金淋巴瘤 |
CD20 | B淋巴细胞慢性白血病、滤泡性淋巴瘤、套细胞淋巴瘤、成人弥漫性大细胞淋巴瘤 |
CD22 | 急性淋巴细胞白血病、非霍奇金淋巴瘤 |
CD30 | 霍奇金淋巴瘤、非霍奇金淋巴瘤 |
CD33 | 髓细胞性白血病 |
CD123 | 急性髓细胞白血病、成人急性巨核细胞白血病、成人急性单核细胞白血病、成人急性微分化型髓系白血病、成人急性粒单核细胞白血病 |
CD133 | 肝癌、胰腺癌、脑肿瘤、乳腺癌、卵巢癌、大肠癌、急性髓系和淋巴系白血病 |
CD138 | 多发骨髓瘤 |
CD19+meso | 转移性胰腺癌 |
CEA | 大肠癌、乳腺癌、胃癌、肺癌、卵巢癌、胰腺癌、肝癌 |
cMet | 转移性乳腺癌、三阴性乳腺癌 |
EGFR | 头颈部癌、晚期EGFR、阳性肿瘤、恶性脑胶质瘤 |
EGFR/CD171 | 神经母细胞瘤、神经节细胞瘤 |
EGFRVIII | 胶质母细胞瘤 |
EphA2 | 恶性脑胶质瘤 |
FAP | 恶性胸腔间皮瘤 |
GD2 | 神经母细胞瘤、肉瘤、非神经母细胞瘤 |
GPC3 | 肝细胞癌 |
HER-2 | 晚期骨肉瘤、多形性胶质母细胞瘤、HER-2阳性肿瘤 |
IL-13Rα2 | 恶性胶质瘤 |
LewisY | 多发性骨髓瘤、急性髓系白血病 |
Mesothelin | 转移性胰腺癌、上皮性卵巢癌、上皮性恶性胸膜间皮瘤、恶性间皮瘤、胰腺癌、卵巢肿瘤、三阴性乳腺癌、子宫内膜癌 |
MUC1 | 肝细胞癌、非小细胞肺癌、胰腺癌、三阴性乳腺癌 |
ROR1 | 慢性淋巴细胞白血病 |
SS1 | 胰腺癌 |
资料来源:公开资料整理
6、CAR-T细胞治疗血液系统肿瘤
很多血液肿瘤存在肿瘤特异性抗原,并且有研究清楚的单克隆抗体,这为构建CAR-T细胞提供了良好的靶点和单链可变区,临床试验表明, CAR-T细胞在治疗血液恶性肿瘤中有良好前景。
以B细胞表面标志物CD19为治疗靶点构建的CAR-T细胞,是迄今为止研究最广泛的CAR-T细胞。在中国CAR-T在研的145例试验中,有65例以CD19为靶点。最初选择CD19作为靶点是因为该分子在B系列淋巴细胞白血病的肿瘤细胞表面普遍高表达,但在造血干细胞及绝大多数正常组织中基本不表达,可以防止骨髓抑制等不良反应的发生。针对CD19的CAR有多种构建形式,临床试验涉及急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)、慢性淋巴细胞白血病(chronic lymphocytic leukemia,CLL)、非霍奇金淋巴瘤(non-Hodgkin’s lymphoma,HL)和小淋巴细胞淋巴瘤(small lymphocytic lymphoma,SLL)等多种血液肿瘤,且表现出优异的疗效。以r/r B-All为例,病人的完全应答率多为70~90%。2017年ASCO会议上,CAR-T用于r/r MM(多发性骨髓瘤)中也取得令人瞩目的效果,94%(33/35)患者在CAR-T细胞输注后2个月内获得了VGPR。CAR-T细胞治疗的出现,为晚期血液肿瘤患者带来新的希望。
除靶向CD19外,越来越多的新型靶点的CAR结构开始应用于临床治疗。美国国家癌症中心靶向CD22的CAR-T治疗已开展对滤泡性淋巴瘤(FL)、非霍奇金淋巴瘤(NHL)、弥漫性大B细胞淋巴瘤(DLBCL)、急性B淋巴细胞白血病(B-All)等多项血液肿瘤的临床试验。其他如CD20、ROR1、IgK、CD30、CD123、CD33、LeY、BCMA、CD138等靶点的细胞治疗均已在全球不同机构开展临床试验。目前,在中国针对非CD19抗原的临床试验有19个,包括CD20、CD22、CD30、CD33、CD38、CD123、CD138、BCMA、Lewis Y等血液恶性肿瘤抗原。
四、我国CAR-T研发进展迅速,中国企业有望弯道超车
1、国内外企业CAR-T临床结果对比
截止2017年12月收集到的临床数据显示,针对ALL适应症,诺华的CAR-T疗法治疗的患者数量为81名,客观反应率为53%,完全缓解率为40%,效果良好。国内博生吉安科的CD19-CART也是针对ALL患者,目前接受治疗的患者数量为19名,客观反应率为100%,完全缓解率为90%,如果样本扩大,等待时间的检验之后仍有这样的治疗效果,相比于诺华的CAR-T疗法将是ALL患者更好的选择。针对NHL适应症,Kite的CAR-T疗法治疗的患者数量为108名,客观反应率为82%,完全缓解率为58%;接受Juno治疗的患者数量为98名,客观反应率为76%,完全缓解率为55%,临床效果与Kite的差距不大,但还有待时间检验;接受博生吉安科治疗的患者数量为2名,完全缓解率为100%,但是样本太小,预计接受治疗的患者数量增加之后才可知道其真实的治疗效果。针对MM适应症,Bluebird的CAR-T疗法治疗的患者数量为18名,客观反应率为89%,完全缓解率为22%,除去最低剂量组的3名患者则客观反应率可达100%,完全缓解率可达26%;南京传奇的CAR-T疗法治疗的患者数量为35名,客观反应率为100%,完全缓解率为74%,临床效果非常显著。
部分国内外企业CAR-T临床结果
公司 | 产品 | 适应症 | 患者人数 | 客观反应率(6-12个月) | 完全缓解率(6-12个月) |
诺华 | CTL019 | ALL | 81 | 53% | 40% |
Kite | KTE-C19 | NHL | 108 | 82% | 58% |
Juno | JCAR017 | NHL | 98 | 76% | 55% |
博生吉(调研数据) | CD19-CART | ALL | 19 | 100% | 90% |
博生吉(调研数据) | CD19-CART | NHL | 2 | 100% | 100% |
Bluebird | bb2121 | MM | 18 | 89% | 22% |
南京传奇 | LCAR-B38M | MM | 35 | 100% | 40% |
资料来源:公开资料整理
五、CAR-T国内市场前景广阔,国家鼓励创新
血液肿瘤市场潜力达数百亿级
据国家癌症中心数据,中国2015年新发癌症病例429.2万,其中新增白血病患者人数为7.53万,新增骨髓瘤患者人数为2.8万,新增淋巴癌患者人数为8.82万。ALL患者占儿童白血病患者比例达70%以上,占成年人白血病患者比例为20%左右,因此ALL患者人数至少有1.5万。据世界卫生组织统计,NHL占淋巴癌患者比例高达89.1%,因此NHL患者人数为7.86万。目前CAR-T技术针对的癌症适应症MM、ALL、NHL目标人群数量至少有12.16万,现有疗法效果较差,而CAR-T疗法效果显著,假设渗透率达到60%,参考诺华CAR-T疗法的定价47.5万美元,Kite CAR-T疗法的定价37.2万美元,假设国内CAR-T疗法定价为50万元/疗程,则市场规模可达365亿元。如果CAR-T技术可以针对所有的癌症适应症,即目标人群扩展到每年的新发癌症病例429.2万,则潜在市场规模非常大,而且CAR-T还有其他领域的应用。
CAR-T疗法针对的适应症MM、ALL、NHL国内市场规模估算
目标人群 | 12.16万 | 12.16万 | 12.16万 |
渗透率 | 40% | 60% | 80% |
价格 | 50万 | 50万 | 50万 |
市场规模 | 243亿 | 365亿 | 486亿 |
资料来源:公开资料整理
文章转载、引用说明:
智研咨询推崇信息资源共享,欢迎各大媒体和行研机构转载引用。但请遵守如下规则:
1.可全文转载,但不得恶意镜像。转载需注明来源(智研咨询)。
2.转载文章内容时不得进行删减或修改。图表和数据可以引用,但不能去除水印和数据来源。
如有违反以上规则,我们将保留追究法律责任的权力。
版权提示:
智研咨询倡导尊重与保护知识产权,对有明确来源的内容注明出处。如发现本站文章存在版权、稿酬或其它问题,烦请联系我们,我们将及时与您沟通处理。联系方式:gaojian@chyxx.com、010-60343812。



![研判2024!中国洗衣液行业产业链图谱、政策汇总、市场规模、重点企业及发展趋势分析:中国洗衣液市场规模持续扩大,生物科技赋能绿色洗衣[图]](http://img.chyxx.com/images/2022/0330/99d4e8a78387e45474dcca8da0b56041c69dec09.png?x-oss-process=style/w320)
![2024年中国广播电视和网络视听行业总收入、节目制作和播出时长、节目综合人口覆盖率、用户数量及行业从业人员数量统计分析:中国广电产业创收能力稳步提升,新兴业务成为拉动产业发展的重要增长极[图]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![研判2024!中国新材料行业发展历程、市场规模及细分领域现状分析:下游市场对新材料需求激增,新材料技术水平引领高新技术未来[图]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![2024年中国中央对地方转移支付及细分情况分析:中央对地方转移支付总额破10万亿 [图]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)
![2024年中国各级各类学校数量、在校生及专任教师数量分析:教育事业高质量发展持续推进,2023年在校生2.91亿人[图]](http://img.chyxx.com/images/2022/0330/ff5315f651f3e124d0f5a156ac51655e46e5433f.png?x-oss-process=style/w320)
![趋势研判!2024年中国单克隆抗体行业产业链、市场规模、竞争格局及重点企业分析:单克隆抗体市场规模超1200亿元,行业发展前景巨大[图]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)