伴随国际临床多中心数据获得认证(更多早期临床项目有望进入中国),以及国内仿制药 一致性评价的推进,CRO 需求井喷。53 号征求意见稿中临床试验机构改为备案制(要求: PI 具备高级职称且参加过 3 个以上临床试验),可预见三甲医院及社会资本将积极参与, 缓解临床资源瓶颈(目前仅 500 家左右),推动 CRO 企业业绩持续快速增长。
药审中心接受化药 IND 申请(2016)
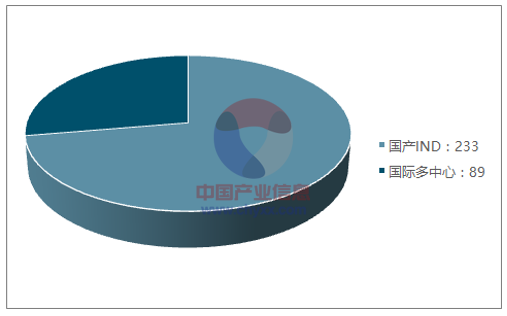
资料来源:公开资料,智研咨询整理
相关报告:智研咨询发布的《2017-2022年中国生物药品制造行业研究及发展前景预测报告》
国际多中心临床申请治疗领域分布(2016)

资料来源:公开资料,智研咨询整理
CDE 今年 3 月发布《2016 年度药品审评报告》,共批准 206 件药品上市注册申请(包含 中药 2 件、化学药品 188 件、生物制品 16 件),和 3666 件药物临床试验注册申请(中 药 84 件、化学药品 3311 件、生物制品 271 件)。全年完成审评的注册申请数量较 2015 年提高了 26%,其中化药注册申请为 10060 件,约占全部完成量的 83%。
2016 年各类药品注册申请完成审评数量
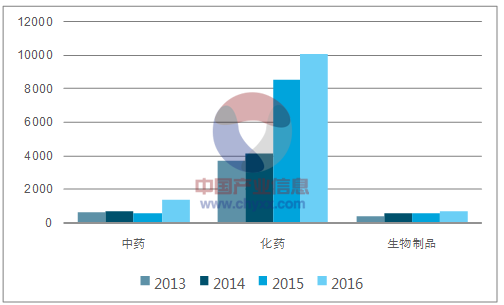
资料来源:公开资料,智研咨询整理
2016 年总局药审中心扩招一线技术审评人员至 近 300 人,相比 2014 年的 89 人增加了 3 倍多。2016 年待审注册申请由 2015 年高 峰时期的 21668 件下降至 8200 件,积压问题已基本解决。
CDE 评审人员增加至近 300 人
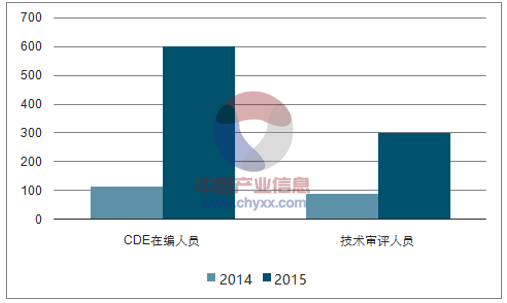
资料来源:公开资料,智研咨询整理
CDE 历年审批及积压批件的数量
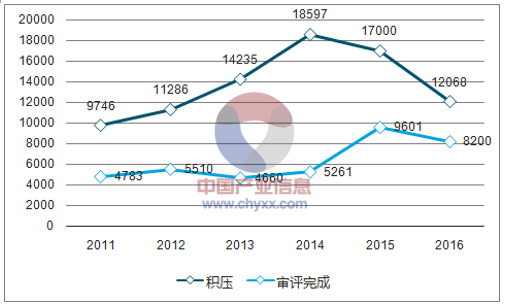
资料来源:公开资料,智研咨询整理
国务院 44 号文要求 CDE 严格规范审评技术要求, 客观上提高企业申报注册的门槛。2016 年 CDE 接收新注册申请 3779 件,较 2015 年下降了 54%,其中化药接收量下降幅度最大,降幅达 57%。与此同时,ANDA 的 通过量也出现了大幅下滑(2015 年化药 ANDA 批准量 2215 件下滑 29%至 2016 年 批准量 1564 件),药品审评逐渐呈现速度和质量兼具的趋势。
2016 年注册申请接收情况与前三年对比

资料来源:公开资料,智研咨询整理
2015-2016 完成审评的化药各类注册申请数量
(件数) | 批准 | 不批准 | 撤回等 | 合计 | ||||
注册申请类型 | 2015 | 2016 | 2015 | 2016 | 2015 | 2016 | 2015 | 2016 |
IND | 332 | 455 | 26 | 51 | 28 | 22 | 386 | 528 |
验证性临床 | 2050 | 2856 | 632 | 375 | 43 | 44 | 2725 | 3275 |
NDA | 83 | 23 | 22 | 28 | 187 | 478 | 292 | 529 |
ANDA | 2215 | 1564 | 998 | 1012 | 372 | 397 | 3585 | 2973 |
补充申请 | 917 | 1634 | 291 | 448 | 141 | 173 | 1349 | 2255 |
进口再注册 | 141 | 173 | 7 | 76 | 24 | 8 | 172 | 257 |
复审 | 2 | 1 | 2 | 5 | 243 | - | - | - |
合计 | 5740 | 6705 | 1977 | 1990 | 797 | 1122 | 8514 | 10060 |
资料来源:公开资料,智研咨询整理
截至 2017 年 6 月 6 日,CDE 共出台十七批(将 2016 年 7 月 21 日出台的合并为一批)优先审评拟纳入名单,包含 269 个批件(除去第 8、 第 9 批中重复计算的 “治疗用乙型肝炎腺病毒注射液”),166 个品种。其中创新药品 108 个,首仿 41 个(CDE 将仅有一个进口原研在国内上市的 6 类药品也算作首仿),出口制 剂 15 个,充分体现鼓励创新、强调临床价值的核心思想。可预见未来国产新药及疗效确 定、安全有效的高水平仿制药有望持续获益。
截至 2017 年 6 月 6 日拟纳入优先审评的品种分类(按批次)

资料来源:公开资料整理
截至 2017 年 6 月 6 日拟纳入优先审评的品种分类(按总量)
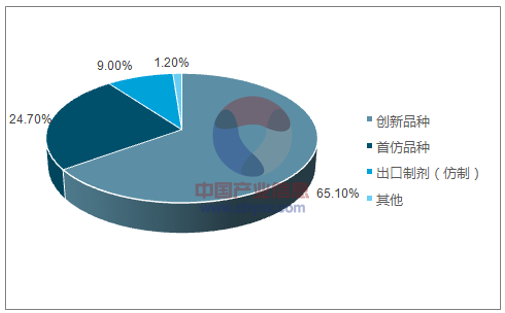
资料来源:公开资料,智研咨询整理
在入围的 108 个创新药中,国产品种有 34 个(第九批 拟纳入 11 个国产新药)。同时还有 41 个首仿入围,可以看出优先审评政策将更大程度地 鼓励本土企业优质药品的加速上市。
创新品种中,国产 vs 国外(2017 年 6 月 6 日)
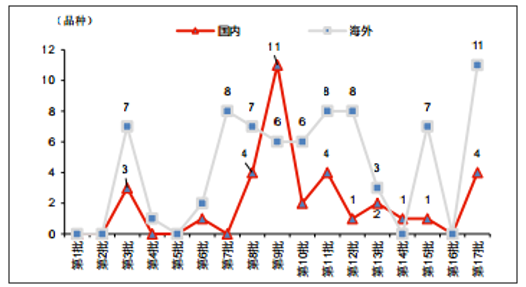
资料来源:公开资料整理
仿制品种中,国产 vs 国外 (2017 年 6 月 6 日)
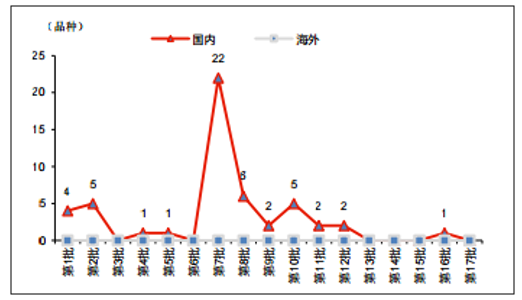
资料来源:公开资料整理
拟纳入优先审评的国内制药企业(截至 2017 年 6 月 6 日)
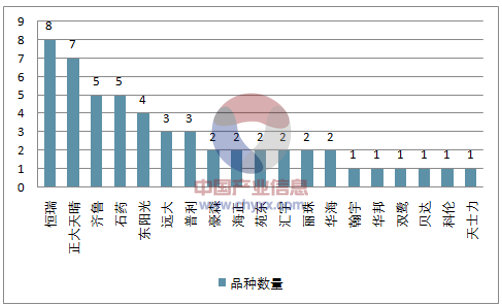
资料来源:公开资料,智研咨询整理
优先审评中获益的国外原研企业(截至 2017 年 6 月 6 日)
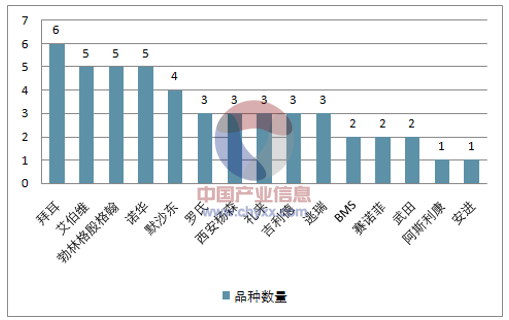
资料来源:公开资料,智研咨询整理
肿瘤与儿童药受益最大。目前纳入优先审评的产品以化药为主,截至 2017 年 6 月 6 日丙 型肝炎(批量入围)、抗肿瘤药、儿童药在优先审评中入围数目最多(合计近 60%),免疫 系统疾病、眼底药、糖尿病等热点领域也均有重磅产品入围。可以预见未来技术难度大、 临床效果好的高水平制剂将会受到政策红利拉动而脱颖而出。
截至 2017 年 6 月 6 日入围优先审评的品种(按适应症)
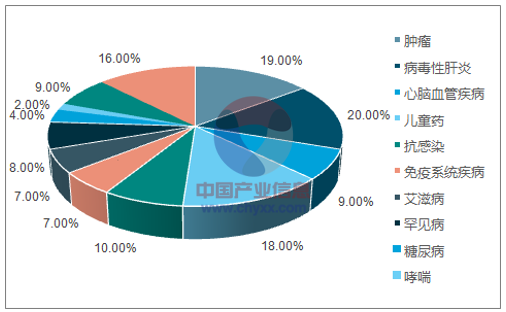
资料来源:公开资料,智研咨询整理
我国医药工业转型在即,低水平仿制药品将被 淘汰(一致性评价、飞检),高水平优效药品多重受益(优先审评、新医保),制剂水平接 轨国际的制药龙头有望脱颖而出
国内创新研发管线(1.1 类化药+1 类生物制品)领先的制药企业(2010-6M2017)
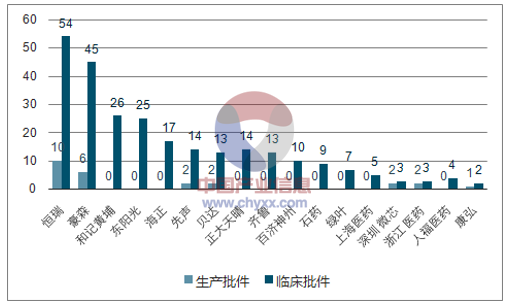
资料来源:公开资料,智研咨询整理
国内 3.1 类仿制药品管线领先的企业(2010-6M2017)

资料来源:公开资料整理
 智研咨询 - 精品报告
智研咨询 - 精品报告

2024-2030年中国硫酸氢氯吡格雷行业市场全景评估及发展前景研判报告
《2024-2030年中国硫酸氢氯吡格雷行业市场全景评估及发展前景研判报告》共十一章,包含硫酸氢氯吡格雷地区运行分析,硫酸氢氯吡格雷重点企业竞争力分析,2024-2030年中国硫酸氢氯吡格雷行业发展前景预测等内容。
文章转载、引用说明:
智研咨询推崇信息资源共享,欢迎各大媒体和行研机构转载引用。但请遵守如下规则:
1.可全文转载,但不得恶意镜像。转载需注明来源(智研咨询)。
2.转载文章内容时不得进行删减或修改。图表和数据可以引用,但不能去除水印和数据来源。
如有违反以上规则,我们将保留追究法律责任的权力。
版权提示:
智研咨询倡导尊重与保护知识产权,对有明确来源的内容注明出处。如发现本站文章存在版权、稿酬或其它问题,烦请联系我们,我们将及时与您沟通处理。联系方式:gaojian@chyxx.com、010-60343812。







