1、新冠病毒传播力强,多国强力隔离防控
截至2020年4日7日,全球累计新冠确诊病例超140万例,4月7日单日新增超8万例。由于新冠病毒感染者中约80%为轻症患者或无症状感染者,若不采取强力社会隔离措施,极难控制其传播。在巨大的防疫压力下,多国出台了强力居家隔离和边境管制措施。意大利、西班牙、法国等欧盟国家相继实施了全国封锁;英国要求全民居家隔离;美国宣布入境禁令,多州发布“居家令”;日本包括东京在内的7个都府县亦于4月7日进入紧急状态,要求居民尽量避免外出。我国虽前期国内防疫措施取得阶段性成果,但现依然存在“防输入”压力,当前处于“外国公民入境暂停、本国公民入境隔离”的强力边境管控之中。
全球新冠累计确诊和新增确诊病例数
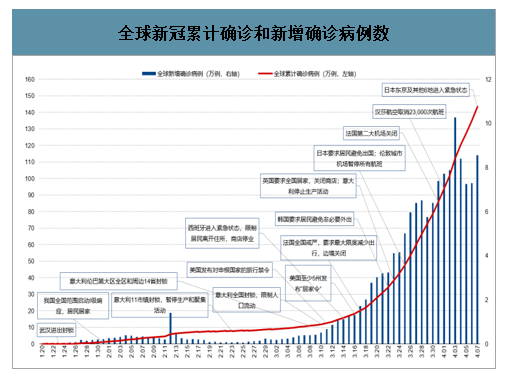
数据来源:公开资料整理
2、新型冠状病毒检测方法
新型冠状病毒的检测方法主要包含核酸检测、抗体检测、抗原检测几种方法。由于抗原检测检出率较低,目前新冠检测主要集中在抗体和核酸检测。核酸检测目前是新型冠状病毒检测的“金标准”,具有早期诊断、灵敏度和特异性高等特点;但抗体检测操作便捷、检测迅速,可作为核酸诊断的补充手段。
3、新冠检测试剂盒国内外上市情况
1)国内外审评要求
2020年3月以来,新冠肺炎全球爆发,为应对紧张的疫情,国家药品监督管理局(NMPA)、美国食品药品监督管理局(FDA)、世界卫生组织(WHO)开放了应急审批通道,加快了新型冠状病毒检测试剂盒的审批。
监管机构对新冠病毒核酸检测试剂发布审评标准时间表
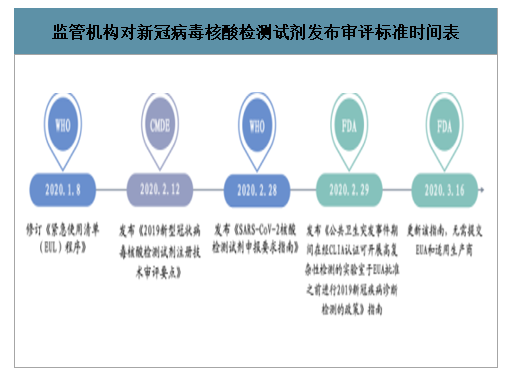
数据来源:公开资料整理
智研咨询发布的《2020-2026年中国新冠检测试剂盒产业运营现状及发展前景分析报告》数据显示:2020年2月28日,美国微生物学会(theAmericanSocietyofMicrobiology,ASM)致函FDA,对在新冠肺炎爆发期间,通过紧急使用授权(emergencyuseauthorizationEUA)流程可能对供临床实验室用的诊断检测的影响表示担忧。一天后,FDA发布即时生效的指南,允许某些实验室在获得EUA授权之前使用实验室开发的检测(laboratorydevelopedtest,LDT)。
FDA在3月16日更新后的指南中表示,商业制造商可以开发新冠病毒检测,在提交EUA请求之前的15个工作日内,一旦通过验证,就可以开始使用相关的检测。制造商可以提供检测的使用说明,并在其网站公布检测性能信息。FDA同时通过没有紧急使用授权的情况下,准许使用血清学检测,但要求在检测中包括警告声明,注明“FDA指出,该测试尚未得到FDA审评,抗体检测的结果不应作为诊断或排除新冠病毒感染,或告知感染状况的唯一依据。”
通过对比中国CMDE、美国FDA以及WHO对于新冠检测试剂盒的注册审评要求,总体来说,中国的审评要求更加严格,对于细节的要求比较充分和明确。同时,明确的具体要求也有利于申请人在产品确认过程中一步到位,但国际监管机构也有部分先进的经验值得我国学习。
CMDE、WHO及FDA新型冠状病毒核酸检测试剂审评要求对比
CMDE、WHO及FDA新型冠状病毒核酸检测试剂审评要求对比 | |||
项目 | 中国 | WHO | FDA |
文件适用范围 | 中国IVD生产企业;产品在境内上市 | 全球企业;全球采购 | 经CLIA认证的实验室;商业生产商 |
质量管理体系 | 与WHO类似 | EUR程序(质量管理体系审查+上市后监管) | 未提及 |
应急审评产品证据 | 认可有限性证据 | 产品描述信息以及安全有效性证据 | 有效性证据水平为“可能有效” |
产品质量控制要求 | 明确主要原材料的验证过程和质量控制标准;要求试剂盒中具备质控体系 | 简单描述申报产品的原材料/成分信息;未对试剂盒中的质控体系进行要求 | 未对试剂盒中的质控体系进行要求 |
性能要求(核酸提取/纯化性能;病毒样本包容性验证;精密度;计量学溯源性;适用机型…) | 明确要求研究配套提取试剂的性能;要求对包容性相关序列分析和试验验证;要求精密度验证的充分性;进行量值研究;要求提供产品说明书-适用机型项中列出所有型号仪器性能评估资料 | 未要求研究配套提取试剂的性能;未要求对包容性相关序列分析和试验验证;概括性描述精密度影响因素和样本浓度水平;进行量值研究;未考虑机型因素 | 未要求研究配套提取试剂的性能;要求对包容性相关序列分析,但未要求试验验证;未提及精密度要求;未提及量值研究;可能考虑适用仪器一般是密闭系统,但未提及 |
临床试验要求(试验机构;样本要求;入组人群;试验结果统计分析…) | 三家以上机构进行临床试验;确诊病例不少于200例,排除病例不少于300例;适用人群为新冠肺炎疑似病例;结果挖掘更充分 | 未对试验机构进行要求;50个前瞻性阳性样本;入组人群为各类人群;临床结果仅计算一致性百分比 | 未对试验机构进行要求;30个反应性人工样本和30个非反应性样本;未规定入组人群;临床结果仅计算一致性百分比 |
数据来源:公开资料整理
2)国内外获批试剂盒
截至2020年4月26日,国家药品监督管理局已应急审批30个新型冠状病毒检测试剂。其中核酸检测试剂18个,抗体检测试剂11个。
国内已批准新型冠状病毒检测试剂
国内已批准新型冠状病毒检测试剂 | |||||
检测方法 | 序号 | 注册证号 | 产品名称 | 注册人 | |
核酸检测 | 荧光PCR法 | 1 | 国械注准20203400057 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 上海之江生物科技股份有限公司 |
2 | 国械注准20203400058 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 上海捷诺生物科技有限公司 | ||
3 | 国械注准20203400060 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 华大生物科技(武汉)有限公司 | ||
4 | 国械注准20203400063 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 中山大学达安基因股份有限公司 | ||
5 | 国械注准20203400064 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 圣湘生物科技股份有限公司 | ||
6 | 国械注准20203400065 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 上海伯杰医疗科技有限公司 | ||
7 | 国械注准20203400179 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 北京卓诚惠生生物科技股份有限公司 | ||
8 | 国械注准20203400184 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 迈克生物股份有限公司 | ||
9 | 国械注准20203400212 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 武汉明德生物科技股份有限公司 | ||
10 | 国械注准20203400299 | 新型冠状病毒(2019-nCoV)核酸检测试剂盒(荧光PCR法) | 上海复星长征医学科学有限公司 | ||
11 | 国械注准20203400322 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 北京金豪制药股份有限公司 | ||
12 | 国械注准20203400384 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) | 江苏硕世生物科技股份有限公司 | ||
恒温扩增-实时荧光法 | 13 | 国械注准20203400241 | 新型冠状病毒2019-nCoV核酸检测试剂盒(恒温扩增-实时荧光法) | 杭州优思达生物技术有限公司 | |
杂交捕获免疫荧光法 | 14 | 国械注准20203400298 | 新型冠状病毒2019-nCoV核酸检测试剂盒(杂交捕获免疫荧光法) | 安邦(厦门)生物科技有限公司 | |
联合探针锚定聚合测序法 | 15 | 国械注准20203400059 | 新型冠状病毒2019-nCoV核酸检测试剂盒(联合探针锚定聚合测序法) | 华大生物科技(武汉)有限公司 | |
恒温扩增芯片法 | 16 | 国械注准20203400178 | 六项呼吸道病毒核酸检测试剂盒(恒温扩增芯片法) | 成都博奥晶芯生物科技有限公司 | |
RNA捕获探针法 | 17 | 国械注准20203400300 | 新型冠状病毒2019-nCoV核酸检测试剂盒(RNA捕获探针法) | 上海仁度生物科技有限公司 | |
RNA恒温扩增-金探针层析法 | 18 | 国械注准20203400301 | 新型冠状病毒2019-nCoV核酸检测试剂盒(RNA恒温扩增-金探针层析法) | 武汉中帜生物科技股份有限公司 | |
双扩增法 | 19 | 国械注准20203400302 | 新型冠状病毒2019-nCoV核酸检测试剂盒(双扩增法) | 武汉中帜生物科技股份有限公司 | |
抗体检测胶体金法 | 20 | 国械注准20203400176 | 新型冠状病毒(2019-nCoV)抗体检测试剂盒(胶体金法) | 广州万孚生物技术股份有限公司 | |
21 | 国械注准20203400177 | 新型冠状病毒(2019-nCoV)IgM/IgG抗体检测试剂盒(胶体金法) | 英诺特(唐山)生物技术有限公司 | ||
22 | 国械注准20203400199 | 新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(胶体金法) | 广东和信健康科技有限公司 | ||
23 | 国械注准20203400239 | 新型冠状病毒(2019-nCoV)IgM/IgG抗体检测试剂盒(胶体金法) | 南京诺唯赞医疗科技有限公司 | ||
24 | 国械注准20203400240 | 新型冠状病毒(2019-nCoV)IgM/IgG抗体检测试剂盒(胶体金法) | 珠海丽珠试剂股份有限公司 | ||
25 | 国械注准20203400367 | 新型冠状病毒(2019-nCoV)抗体检测试剂盒(胶体金法) | 上海芯超生物科技有限公司 | ||
磁微粒化学发光法 | 26 | 国械注准20203400182 | 新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(磁微粒化学发光法) | 博奥赛斯(重庆)生物科技有限公司 | |
27 | 国械注准20203400183 | 新型冠状病毒(2019-nCoV)IgG抗体检测试剂盒(磁微粒化学发光法) | 博奥赛斯(重庆)生物科技有限公司 | ||
28 | 国械注准20203400198 | 新型冠状病毒(2019-nCoV)抗体检测试剂盒(磁微粒化学发光法) | 厦门万泰凯瑞生物技术有限公司 | ||
29 | 国械注准20203400365 | 新型冠状病毒(2019-nCoV)IgG抗体检测试剂盒(磁微粒化学发光法) | 丹娜(天津)生物科技有限公司 | ||
30 | 国械注准20203400366 | 新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(磁微粒化学发光法) | 丹娜(天津)生物科技有限公司 | ||
数据来源:公开资料整理
国外疫情日趋严峻,各国陷入试剂盒短缺的困境。国产试剂盒具有先发临床和成本优势,多家国内企业开始向世界各国出口试剂盒。3月开始,欧洲严峻疫情态势产生新冠检测的巨大需求,多家中国企业瞄准了欧洲庞大的新冠检测市场,并积极推动自主研发的新冠检测产品进入欧洲市场。截至4月22日,国内从事新冠检测相关产品研发生产的企业近千家,其中产品已获得CE认证的企业超过160家。
获得欧盟CE认证的厂家和产品(不完全统计)
获得欧盟CE认证的厂家和产品(不完全统计) | |
达安基因 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
丹大生物 | 新型冠状病毒IgM/IgG快速检测试剂盒 |
汉唐生物 | 新型冠状病毒抗体检测试剂盒(免疫层析法) |
华大基因 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
华迈兴微 | 微流控化学发光新冠病毒检测试剂盒 |
凯普生物 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
迈克生物 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
2019新型冠状病毒IgM/IgG抗体检测试剂盒(胶体金法) | |
美康生物 | 新型冠状病毒COVID-19抗体(IgG/IgM)联合检测试剂盒(乳胶法) |
圣湘生物 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
泰熙生物 | 新型冠状病毒IgM/IgG检测试剂盒 |
万孚生物 | 2019-nCoV新型冠状病毒抗体检测试剂(免疫层析法) |
2019-nCoV新型冠状病毒IgM抗体检测试剂(荧光免疫层析法) | |
2019-nCoV新型冠状病毒抗体检测试剂(荧光免疫层析法) | |
新产业生物 | 全自动化学发光新型冠状病毒2019-nCoVIgM、IgG抗体检测试剂盒 |
亚辉龙 | 化学发光法新冠病毒抗体检测试剂盒 |
一瑞生物 | 新型冠状病毒COVID-19抗体检测试剂盒(胶体金法) |
之江生物 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
卓诚惠生 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
硕世生物 | 新型冠状病毒(2019)核酸检测试剂盒(荧光PCR法) |
新型冠状病毒IgM/IgG抗体联合检测试剂盒(胶体金法) | |
安图生物 | 新型冠状病毒(2019-nCoV)IgG抗体检测试剂盒(磁微粒化学发光法) |
新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(磁微粒化学发光法) | |
新型冠状病毒(2019-nCoV)IgM/IgG双抗体检测试剂盒(胶体金法) | |
新型冠状病毒2019-nCoV核酸检测试剂盒(PCR-荧光探针法) | |
科华生物 | 新型冠状病毒(2019-nCoV)ORF1ab/N/E基因核酸检测试剂测试剂盒(荧光PCR法) |
新型冠状病毒(SARS-CoV-2)IgM/IgG抗体检测试剂盒(胶体金法) | |
新型冠状病毒(SARS-CoV-2)IgM抗体检测试剂盒(ELISA法) | |
新型冠状病毒(SARS-CoV-2)IgG抗体检测试剂盒(ELISA法) | |
凯创生物 | 新型冠状病毒(2019-nCoV)IgM/IgG总抗体快速检测试剂盒(胶体金法) |
新型冠状病毒(2019-nCoV)IgM抗体快速检测试剂盒(胶体金法) | |
中元汇吉 | 新型冠状病毒(2019-nCoV)核酸检测试剂盒(PCR-荧光探针法) |
核酸提取试剂盒(磁珠法) | |
银科医学 | 新型冠状病毒IgG/IgM抗体检测试剂盒(胶体金法) |
明德生物 | 新型冠状病毒(2019-nCoV)核酸检测试剂盒 |
新型冠状病毒IgM/IgG抗体检测试剂盒(胶体金法) | |
康华生物 | 新型冠状病毒IgM抗体检测试剂盒(免疫层析法) |
基蛋生物 | 新型冠状病毒(2019-nCOV)核酸检测试剂盒(荧光PCR法) |
新型冠状病毒(2019-nCOV)IgM抗体检测试剂盒(胶体金法) | |
新型冠状病毒(2019-nCOV)IgG抗体检测试剂盒(胶体金法) | |
新型冠状病毒(2019-nCOV)IgM/IgG抗体检测试剂盒(胶体金法) | |
国赛生物 | 新型冠状病毒IgG/IgM抗体检测试剂盒(时间分辨荧光免疫法) |
诺唯赞 | 新型冠状病毒(2019-nCoV)IgM/IgG抗体检测试剂盒(胶体金法) |
微米生物 | 新型冠状病毒(COVID-19)IgM/lgG抗体检测试剂 |
博奥赛斯 | 新型冠状病毒(COVID-19)抗体检测试剂盒(胶体金免疫层析法) |
新型冠状病毒(COVID-19)IgG抗体检测试剂盒(胶体金免疫层析法) | |
新型冠状病毒(COVID-19)IgM抗体检测试剂盒(胶体金免疫层析法) | |
新型冠状病毒(COVID-19)IgG抗体检测试剂盒(化学发光法法) | |
新型冠状病毒(COVID-19)IgM抗体检测试剂盒(化学发光法法) | |
新型冠状病毒(COVID-19)IgG抗体检测试剂盒(酶联免疫法) | |
新型冠状病毒(COVID-19)IgM抗体检测试剂盒(酶联免疫法) | |
美联泰科生物 | 新型冠状病毒IgG抗体检测试剂盒(磁微粒化学发光法) |
新型冠状病毒IgM抗体检测试剂盒(磁微粒化学发光法) | |
新型冠状病毒S1蛋白检测试剂盒(磁微粒化学发光法) | |
伊仕生物 | 新冠状病毒(2019-NCOV)IgG/IgM抗体联合检测试剂盒(胶体金法) |
宝太生物 | 新型冠状病毒IgG/IgM抗体检测试剂盒(胶体金法) |
万泰生物 | 新型冠状病毒(2019-nCoV)抗体检测试剂盒(胶体金法) |
新型冠状病毒(2019-nCoV)抗体检测试剂盒(酶联免疫法) | |
新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(酶联免疫法) | |
新型冠状病毒(2019-nCoV)核酸检测试剂盒(PCR-荧光探针法) | |
英盛生物 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
康录 | 新型冠状病毒(COVID-19)核酸检测试剂盒(荧光PCR法) |
三诺生物 | 新型冠状病毒抗体检测试剂盒(胶体金法) |
艾克韦 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
安必奇生物 | 新型冠状病毒(COVID-19)IgM/IgG抗体检测试剂盒(胶体金免疫层析法) |
比格飞序生物 | 新型冠状病毒核酸扩增检测试剂盒 |
波生生物 | 新型冠状病毒IgM/IgG抗体检测试剂盒(胶体金法) |
博日科技 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
丹娜生物 | 新型冠状病毒(2019-nCoV)IgG抗体检测试剂盒(胶体金法) |
新型冠状病毒(2019-nCoV)核酸检测试剂盒(RT-PCR多重荧光探针法) | |
达伯药业 | 新型冠状病毒(SASA-CoV-2)IgG抗体诊断试剂盒(胶体金法) |
新型冠状病毒(SASA-CoV-2)IgM抗体诊断试剂盒(胶体金法) | |
新型冠状病毒(SASA-CoV-2)IgG/IgM抗体诊断试剂盒(胶体金法) | |
新型冠状病毒(SASA-CoV-2)核酸检测试剂盒(荧光RT-PCR法) | |
迪安生物 | 新型冠状病毒核酸检测试剂盒(荧光PCR法) |
禾柏生物 | 新型冠状病毒IgG/IgM抗体检测试剂盒(胶体金法、免疫比浊法) |
华益美生物 | 新型冠状病毒(2019-nCoV)核酸检测试剂盒(PCR-荧光法) |
简码基因 | 新型冠状病毒核酸检测试剂盒(快速PCR荧光法) |
莱和生物 | 新型冠状病毒(2019-nCoV)IgG抗体检测试剂(胶体金法) |
新型冠状病毒(2019-nCoV)IgM抗体检测试剂(胶体金法) | |
新型冠状病毒(2019-nCoV)IgM/lgG抗体联合检测试剂(胶体金法) | |
乐普医疗 | 新型冠状病毒抗体检测试剂盒(胶体金免疫层析法) |
黎明生物 | 新型冠状病毒(SARS-COV-2)多重RT-PCR试剂盒(荧光探针法) |
新型冠状病毒IgM及IgG抗体二联检测试剂盒(乳胶免疫层析层析法) | |
新型冠状病毒总抗体检测试剂盒(乳胶免疫层析层析法) | |
新型冠状病毒抗原检测试剂盒(乳胶免疫层析层析法) | |
隆基生物 | 新型冠状病毒检测试剂盒(COIVD-19) |
默乐生物 | 新型冠状病毒(2019-nCoV)ORF1ab、E和N基因检测试剂盒(荧光PCR法) |
新型冠状病毒IgG/IgM抗体检测试剂盒(免疫层析法) | |
纳奥生物 | 新型冠状病毒(COVID-19)多重核酸快速PCR检测试剂盒 |
普瑞康 | 新型冠状病毒试剂盒 |
深蓝医疗 | 新型冠状病毒(COVID-19)IgM/IgG抗体检测试剂盒(胶体金免疫层析法) |
新型冠状病毒(COVID-19)IgM抗体检测试剂盒(胶体金免疫层析法) | |
新型冠状病毒(COVID-19)lgG抗体检测试剂盒(胶体金免疫层析法) | |
思路迪 | 新型冠状病毒2019-nCoV核酸检测试剂盒(光PCR法) |
新型冠状病毒2019-nCoV和流感AB核酸联合检测试剂盒(四色光PCR法) | |
泰格科信 | 新型冠状病毒(2019-nCoV)IgG/IgM抗体检测试剂盒(胶体金法) |
天深医疗 | 新型冠状病毒IgM抗体检测试剂盒(化学发光法) |
新型冠状病毒IgG抗体检测试剂盒(化学发光法) | |
新产业 | 全自动化学发光新型冠状病毒2019-nCoVIgM、IgG抗体检测试剂盒 |
新健康成 | 新型冠状病毒(SARS-Cov-2)IgG/M检测试剂盒(免疫荧光层析法) |
英科新创 | 新型冠状病毒IgM/IgG抗体联合检测试剂盒(胶体金法) |
新型冠状病毒IgM/IgG抗体联合检测试剂盒(胶体金法)-带配件 | |
新型冠状病毒抗体检测试剂盒(胶体金法) | |
新型冠状病毒抗体检测试剂盒(胶体金法)-带配件 | |
致善生物 | 新型冠状病毒SARS-CoV-2核酸检测试剂盒(荧光PCR法) |
喜诺生物 | 新型冠状病毒IgG抗体检测试剂盒(胶体金法) |
新型冠状病毒IgM抗体检测试剂盒(胶体金法) | |
岚煜生物 | 新型冠状病毒(2019-nCoV)IgM/IgG检测试剂盒 |
扬新生物 | (SARS-CoV-2)IgM抗体检测试剂盒(胶体金法) |
(SARS-Cov-2)IgM/IgG抗体检测试剂盒(胶体金法) | |
(SARS-CoV-2)IgM抗体检测试剂盒(荧光法) | |
(SARS-CoV-2)IgM/IgG抗体检测试剂盒(荧光法) | |
2019-nCoV核酸检测试剂盒 | |
良润生物 | 新型冠状病毒IgM/IgG抗体检测试剂盒(胶体金免疫层析法) |
华银医药 | 新型冠状病毒2019-nCOV核酸检测试剂盒(荧光PCR法) |
丽拓生物 | 新型冠状病毒(COVID-19)IgG/IgM检测试剂盒(免疫层析法) |
泰乐德医疗 | 新型冠状病毒(SARS-CoV-2)核酸检测试剂盒(PCR-荧光探针法) |
新型冠状病毒(SARS-CoV-2)IgM/IgG抗体检测试剂盒(胶体金法) | |
新型冠状病毒(2019-nCoV)核酸检测试剂盒(双重荧光PCR法) | |
宇诺生物 | 新型冠状病毒(SARS-CoV-2)IgG/IgM抗体联合检测试剂盒(胶体金法) |
亿立方 | 新型冠状病毒2019-nCoV核酸检测试剂盒(PCR-荧光探针法) |
新型冠状病毒COVID-19IgG、IgM抗体检测试剂盒(胶体金法) | |
新赛亚 | 新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(胶体金免疫层析法) |
新型冠状病毒(2019-nCoV)lgG抗体检测试剂盒(胶体金免疫层析法) | |
新型冠状病毒(2019-nCoV)lgM抗体检测试剂盒(量子点免疫荧光法) | |
新型冠状病毒(2019-nCoV)lgG抗体检测试剂盒(量子点免疫荧光法) | |
沃文特生物 | 2019-nCoVIgG/IgM抗体检测试剂盒 |
优利特 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
金磁纳米 | 新型冠状病毒(2019-nCoV)核酸检测试剂盒 |
(2019-nCoV)IgG/IgM抗体检测试剂盒 | |
康永生物 | 新型冠状病毒抗体IgG/IgM联合检测试剂盒(胶体金法) |
北京库尔科技 | 新冠病毒(2019-nCoV)IgM/IgG抗体检测试剂盒(胶体金层析法) |
宝瑞源生物 | 新型冠状病毒(SAR-CoV-2)核酸检测试剂盒(多重荧光PCR法) |
安科生物 | 新型冠状病毒(COVID-19)IgG/IgM抗体检测试剂盒(胶体金法) |
东方基因 | 新型冠状病毒(COVID-19)IgG/IgM抗体快速检测试纸(全血/血清/血浆) |
新型冠状病毒SARS-COV-2核酸检测试剂盒(荧光PCR法) | |
杭州优思达 | 新型冠状病毒2019-nCoV核酸检测试剂盒(恒温扩增-实时荧光法) |
海尔施基因科技 | SARS-CoV-2VirusDetectionDiagnosticKit(RT-qPCRMethod) |
方欣生物 | 新型冠状病毒(COVID-2019)抗体检测试剂盒 |
新型冠状病毒(COVID-2019)IgG抗体检测试剂盒 | |
新型冠状病毒(COVID-2019)IgM抗体检测试剂盒 | |
中检安泰 | 新型冠状病毒(COVID-19)IgA/IgM/IgG抗体联合检测试剂会(胶体金法) |
融智生物 | 七项呼吸道病毒核酸联检试剂盒(微流控RT-PCR法) |
英诺特生物 | 新型冠状病毒IgM/lgG抗体胶体金检测试剂 |
申瑞生物 | 新型冠状病毒2019-nCoV及流感病毒核酸检测试剂盒(荧光PCR法) |
丽珠试剂 | 新型冠状病毒(2019-nCoV)IgM/IgG抗体检测试剂盒(胶体金法) |
芯超生物 | 新型冠状病毒(2019-nCoV)抗体检测试剂盒(胶体金法) |
光景生物 | 新型冠状病毒(SARS-CoV-2)IgG/IgM抗体检测试剂盒(时间分辨荧光免疫层析法) |
中生捷诺 | 新型冠状病毒(2019-nCoV)核酸检测试剂盒(荧光PCR法) |
德诺生物 | 新型冠状病毒(2019-nCoV)IgG抗体检测试剂盒(胶体金免疫层析法) |
新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(胶体金免疫层析法) | |
新型冠状病毒(2019-nCoV)抗原检测试剂盒(荧光免疫层析法) | |
威斯腾生物 | 新型冠状病毒(COVID-19)核酸检测试剂盒(PCR荧光探针法) |
万类生物 | 新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法) |
拜澳泰克 | 2019新型冠状病毒核酸检测试剂盒(荧光RT-PCR法) |
2019新型冠状病毒核酸检测试剂盒(恒温显色法) | |
博奥生物 | 六项呼吸道病毒核酸检测芯片试剂盒(恒温扩增芯片法) |
迅敏康 | 新型冠状病毒(2019-nCoV)核酸检测试剂盒(PCR-荧光探针法) |
检康生物 | 冠状病毒IgM和IgG双抗体快速检测试剂盒 |
金匙医学 | 新型冠状病毒核酸检测试剂盒(多重荧光RT-PCR法) |
博晖创新 | 新型冠状病毒IgM/IgG抗体检测试剂盒 |
新型冠状病毒2019-nCoV核酸检测试剂盒 | |
微远基因 | 宏基因组(mNGS)新型冠状病毒核酸检测试剂盒 |
阳普医疗 | 新型冠状病毒(SARS-CoV-2)核酸检测试剂盒(PCR-荧光探针法) |
迪瑞医疗 | 新型冠状病毒IgM抗体检测试剂盒(化学发光免疫分析法) |
新型冠状病毒IgG抗体检测试剂盒(化学发光免疫分析法) | |
优尼德生物 | SARS-CoV-2核壳蛋白(IgG抗体+IgM抗体+总抗体)ELISA试剂盒 |
数据来源:公开资料整理
相比欧盟CE认证而言,美国市场的准入门槛更高。截止2020年4月27日,核酸检测产品已获得美国EUA的40余家企业中,多为业内知名的跨国巨头企业,其中有四家中国企业:华大基因、南京科维思、迈克生物、复星医药;而核酸检测产品已同时取得国内NMPA注册证书、欧盟CE认证和美国FDAEUA的国内企业只有华大基因、迈克生物、复星医药三家公司。
获得FDAEUA认证的国内核酸检测产品
获得FDAEUA认证的国内核酸检测产品 | ||
获批企业 | 获批时间 | 产品 |
华大基因 | 2020年3月27日 | 新型冠状病毒SARS-nCoV-2核酸检测试剂盒(荧光PCR法) |
南京科维思 | 2020年4月6日 | 新冠病毒(COVID-19)检测试剂盒(数字PCR法) |
迈克生物 | 2020年4月15日 | 新冠病毒核酸检测试剂盒(荧光PCR法) |
复星医药 | 2020年4月17日 | 新型冠状病毒2019-nCov核酸检测试剂盒(荧光PCR法) |
数据来源:公开资料整理
在
抗体检测产品中,乐普医疗的新型冠状病毒(SARS-CoV-2)抗体检测试剂盒(胶体金免疫层析法)于3月27日取得FDAEUA准入,安图生物的新型冠状病毒抗体检测试剂盒(胶体金法,英文名称:Anti-SARS-CoV-2RapidTest)于2020年4月24日获得FDAEUA认证。此外,国内企业万孚生物、三诺生物等的抗体检测试剂盒也已按照FDA发布的《PolicyforDiagnosticTestsforCoronavirusDisease-2019duringthePublicHealthEmergency》完成Notification程序,并且完成了公司注册和产品列名,标志着公司该产品具备了在美国上市销售的资格。2020年4月25日,我国商务部发布公告,“自4月26日起,取得国外标准认证或注册的新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的出口企业,报关时须提交书面声明,承诺产品符合进口国(地区)质量标准和安全要求,海关凭商务部提供的取得国外标准认证或注册的生产企业清单验放”。这也就意味着新冠检测产品的出口只需要取得国外标准认证或注册,无需拥有国内注册证。但同时很重要的一点是出口企业必须进入中国医药保健品进出口商会企业清单才能被验放。目前,符合规定的企业都在积极申请加入,截至4月28日,已有51家企业进入清单。而在此前2020年3月31日,国家商务部会同海关总署、国家药监局发布《关于有序开展医疗物资出口的公告》(2020年第5号),要求自4月1日起,同时获得NMPA注册证书和国外特定区域准入资格的企业可实现国内及获授权的国外地区新冠检测产品的销售。此次“双证”限制的放开,进一步促进国内IVD企业的新冠检测产品出口。
4、国内外新冠检测试剂盒需求测算
1)国内新冠检测试剂盒需求测算
截至2020年3月底,国内新冠检测数量(含核酸及抗体检测)在1500万人份以上,包含确诊患者、高危人群以及疑似病例的排除等,其中国内确诊患者从确诊到出院全流程至少需要检测5次。核酸检测收费国内基本上在150元-270元(各地区及检测机构有所差异,主要分为医院和第三方检测机构,第三方检测机构价格高于医院),抗体检测收费在100元左右,绝大多数医保承担,部分自费隔离患者自己承担。
4月24日,湖北省在全国范围内率先开始新冠病毒检测试剂集中采购。4月26日,湖北省药械集中采购服务平台发布《湖北省新型冠状病毒相关检测试剂集中采购拟中选企业公示》,本次湖北新冠病毒检测试剂集采共有19家企业申报竞价,其中14家申报核酸检测试剂组,5家申报抗体检测试剂组。结果共有4家企业中标核酸检测试剂盒(迈克生物、达安基因、武汉明德生物、华大生物),2家企业中标检测试剂盒(珠海丽珠、南京诺唯赞),采购执行周期原则上为1年。我们以中标公司报价的平均值作为检测试剂的平均出厂价,计算得出核酸检测产品平均出厂价为21.417元,抗体检测产品平均出厂价13.393元。我们预计后续其他省份也将陆续开展集采工作,新冠检测收费价格也将对应下降。
湖北省新型冠状病毒相关检测试剂集中采购拟中选企业名单及报价
湖北省新型冠状病毒相关检测试剂集中采购拟中选企业名单及报价 | ||
类别 | 注册人名称 | 报价价格(元) |
核酸检测试剂 | 迈克生物股份有限公司 | 16780 |
中山大学达安基因股份有限公司 | 19998 | |
武汉明德生物科技股份有限公司 | 23900 | |
华大生物科技(武汉)有限公司 | 24990 | |
抗体检测试剂 | 珠海丽珠试剂股份有限公司 | 12900 |
南京诺唯赞医疗科技有限公司 | 13885 | |
数据来源:公开资料整理
对于2020年国内新冠检测的需求测算,我们分为以下四个假设:1)医院现存确诊患者以及住院、陪护等检测:根据国家发布的《新冠肺炎诊疗方案第七版》中的相关规定,保守估计现存确诊患者每人治愈出院前进行两次核酸检测,共需2280次检测。我们还要关注医院住院病人以及陪护人员的情况,全国多地都出台了对住院患者及陪护人员进行新冠肺炎检测的政策,例如黑龙江省政府规定4月16日起二级及以上医疗机构对所有入院患者和陪护人员开展核酸和血清抗体检测,浙江大学医学院附属第二医院对3000多位住院病人开展新型冠状病毒核酸检测和新型冠状病毒血清抗体检测,做到应检尽检。对这部分人群的测算,首先根据2016-2018年每年医院入院人数保守估计2020年将达到20216万人次,假设一个患者有一名人员陪同,他们都将进行一次检测,推测得到检测需求量为40432万次。与此同时,假设每位医护人员进行2次检测,那么推算共需要2400万次。
2)境外输入检测:当前国内疫情防控积极向好的态势来之不易,对于境外输入环节的防控坚决不能放松。北京、上海等多个入境点城市都发布了对所有入境人员全面落实集中医学观察和核酸检测的规定。根据北京市疾控中心介绍,4月1日至4月13日期间,入境人员累计3122人,据此我们保守估计一个月全国入境人员为2万人。由于全球疫情原因,各个国家对出入境都进行了严格把关,入境人员短期内并不会出现大的增幅。按照2020年剩下8个月计算,假设今年累计入境16万人次,每人进行一次核酸检测,故需要16万次检测。
3)复工、复学检测:许多企业都会组织复工复产的员工进行核酸检测,进一步确保安全性。截至4月14日,全国规模以上工业企业平均开工率已达99%,其它行业也基本复工,还未复工的仅为少数。我们假设还有100万的跨省市复工人员,每人进行一次检测,推算检测需求量为100万次。同时,教师群体以及学生群体也是重点目标人群,不少省市地区在近日宣布将会在开学之后对返校师生进行“核酸检测”,广州已经对20.8万名首批复学的高三、初三师生员工,全覆盖开展核酸检测。根据教育部披露的2018年在校师生的数据,以此为基础进行测算。假设每位师生进行一次核酸检测,预计检测需求量也将达到2.93亿次。
4)常态化检测:当前疫情防控已经进入常态化。4月22日,中共中央政治局常委、国务院总理、中央应对新冠肺炎疫情工作领导小组组长李克强主持召开领导小组会议,会议指出做好常态化防控要提升检测能力,大规模开展核酸和抗体检测。日前,上海率先发布了单位或个人可自愿自费预约进行核酸检测的通知,截至4月24日,已经有北京、上海、广州、山西、天津等地公布了新冠检测机构。我们对于自愿检测的人群数量进行了预估,假设东部发达地区的检测比率是5%,中西部地区的检测比率是3%,推算自愿检测需求达到5390万次。综上,根据我们的推算,国内从目前到今年年底检测需求量共计为77641.42万次,我们假设其中70%为核酸检测,30%为抗体检测。以湖北省中标公司报价的平均值作为出厂价,最终推算得到国内新冠检测的市场规模约为147.59亿元。
国内从目前到2020年年底新冠检测新增需求测算
国内从目前到2020年年底新冠检测新增需求测算 | |||||
住院患者及医护人员检测 | |||||
- | 人数(万) | 人均检测次数(次) | 检测需求量(万) | ||
全国现有确诊人数 | 0.114 | 2 | 0.2 | ||
预计2020年医院入院情况 | 20216 | 1 | 20216 | ||
入院患者陪护情况 | 20216 | 1 | 20216 | ||
医护人员 | 1200 | 2 | 2400 | ||
境外输入检测 | |||||
- | 人数(万) | 人均检测次数(次) | 检测需求量(万) | ||
预计全国每月入境(万) | 总人数(万) | ||||
入境情况 | 2 | 16 | 1 | 16 | |
复工、复学检测 | |||||
- | 人数(万) | 人均检测次数(次) | 检测需求量(万) | ||
复工人群省际流动 | 100 | 1 | 100 | ||
教师 | 1700 | 1 | 1700 | ||
学生 | 27600 | 1 | 27600 | ||
自愿检测 | |||||
- | 人数(万) | 人均检测次数(次) | 检测需求量(万) | ||
总人数(万) | 假设检测比例 | 检测人数(万) | |||
东部发达地区 | 56538.51 | 5% | 2826.93 | 1 | 2826.93 |
中西部地区 | 85443.28 | 3% | 2563.3 | 1 | 2563.3 |
国内检测市场测算 | |||||
- | 核酸检测 | 抗体检测 | 总体 | ||
检测需求(万次) | 54346.9 | 23291.53 | 77638.42 | ||
检测市场(亿元) | 116.4 | 31.19 | 147.59 | ||
数据来源:公开资料整理
2)国外新冠检测试剂盒需求测算
2020年3月以来,国外疫情爆发,先是在欧美等发达国家迅速传播,近期第三世界国家如南美、非洲等地疫情日渐严重,同时暴露出新冠检测试剂盒供应不足的问题,我们选择一些典型的发达国家以及发展中国家对于未来几个月全球(除中国)新冠试剂盒的需求进行测算。根据现有各国新型冠状病毒确诊情况以及检测情况的数据,我们选取了目前确诊人数大于5000的国家,推算了整个疫情期间各国的检测试剂需求量。首先计算出“现已检测总次数/总确诊数”,对疫情发展做出“情景1”、“情景2”、“情景3”三种假设情况下的预测。在情景1下,我们假设发达国家未来新增患者数是现在确诊人数的2倍,发展中国家未来新增患者数是现在确诊人数的4倍;情景2按照发达国家3倍、发展中国家5倍;情景3按照发达国家4倍、发展中国家6倍进行假设,以此为基础推算出未来预计需要检测的次数。同时,对于未来疫情好转之后的常态化检测也进行预估,假设发达国家总人口的检测比率为5%,发展中国家相对低一些为3%。
由于发展中国家医疗服务能力较低,医疗物资非常匮乏,通常检测标准较低。假设:1)发达国家确诊患者治愈出院需要经过两次检测,而在发展中国家只需进行一次检测。2)发达国家核酸试剂盒平均出厂价32.2元,抗体试剂盒平均出厂价20.1元(按照比国内价格高50%计算)。所有检测试剂盒中70%为核酸试剂盒,30%为抗体试剂盒。3)发展中国家的试剂盒平均出厂价要低于发达国家,假设核酸试剂盒平均出厂价27.9元,抗体试剂盒平均出厂价17.5元(按照比国内价格高30%计算)。使用的所有检测试剂盒中30%为核酸试剂盒,70%为抗体试剂盒。
最终预测得到,在情景1假设下,全球(除中国)新增市场规模将合计超过10.78亿美元;在情景2假设下,全球(除中国)新增市场规模将合计超过11.84亿美元;在情景3假设下,全球(除中国)新增市场规模将合计超过12.90亿美元。表11以情景2为例,测算疫情发展期间现存患者、预计新增患者需要检测的次数,以及疫情达到平稳状态后常态化检测的需求:
疫情期间国外新型冠状病毒试剂盒市场规模测算(不含常态化检测)
疫情期间国外新型冠状病毒试剂盒市场规模测算(不含常态化检测) | |||||
疫情发展情况 | 发达国家 | 发展中国家 | 全球市场(亿美元) | ||
预计新增患者数/现总确诊数 | 检测试剂市场(亿美元) | 预计新增患者数/现总确诊数 | 检测试剂市场(亿美元) | ||
情景1 | 2 | 1.73 | 4 | 1.05 | 2.78 |
情景2 | 3 | 2.54 | 5 | 1.3 | 3.84 |
情景3 | 4 | 3.34 | 6 | 1.56 | 4.91 |
数据来源:公开资料整理
国外新型冠状病毒试剂盒市场规模测算(情景2、含常态化检测)
国外新型冠状病毒试剂盒市场规模测算(情景2、含常态化检测) | |||||
发达国家 | 发展中国家 | ||||
- | 检测次数(次) | 市场规模(元) | - | 检测次数(次) | 市场规模(元) |
核酸检测 | 80,459,107 | 2,590,783,258 | 核酸检测 | 74,229,391 | 2,070,999,998 |
抗体检测 | 34,482,475 | 693,097,739 | 抗体检测 | 173,201,911 | 3,031,033,450 |
总体 | 114,941,582 | 3,283,880,998 | 总体 | 247,431,302 | 5,102,033,447 |
假设检测中核酸检测占比70%,抗体检测占比30%假设核酸检测出厂价32.2元,抗体检测出厂价20.1元(按照比国内价格高50%计算) | 假设检测中核酸检测占比30%,抗体检测占比70%假设核酸检测出厂价27.9元,抗体检测出厂价17.5元(按照比国内价格高30%计算) | ||||
国外检测试剂市场规模>83.86亿人民币(11.84亿美元) | |||||
数据来源:公开资料整理
文章转载、引用说明:
智研咨询推崇信息资源共享,欢迎各大媒体和行研机构转载引用。但请遵守如下规则:
1.可全文转载,但不得恶意镜像。转载需注明来源(智研咨询)。
2.转载文章内容时不得进行删减或修改。图表和数据可以引用,但不能去除水印和数据来源。
如有违反以上规则,我们将保留追究法律责任的权力。
版权提示:
智研咨询倡导尊重与保护知识产权,对有明确来源的内容注明出处。如发现本站文章存在版权、稿酬或其它问题,烦请联系我们,我们将及时与您沟通处理。联系方式:gaojian@chyxx.com、010-60343812。



![2024年中国电饭煲行业全景速览:美的、苏泊尔、九阳龙头优势明显[图]](http://img.chyxx.com/images/2022/0330/6b296592ed87ae76d174b4fbc262ff18a3c189b8.png?x-oss-process=style/w320)
![2024年中国激光直接成像(LDI)设备行业发展全景浅析:市场规模持续稳定增长,行业将迎来更多的发展机遇[图]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![2024年中国碳监测行业发展现状分析:碳监测市场正逐渐打开,多家企业布局 [图]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)
![2023年中国聚苯胺行业现状分析:行业规模稳步增长,新技术的研发推动行业进一步发展[图]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![2023中国布鞋行业全景速览:定制化、跨界合作将是行业未来重要发展趋势[图]](http://img.chyxx.com/images/2022/0330/d1363a7ee3953fc25ed09e0b79158acce9dc7c22.png?x-oss-process=style/w320)
![2024年中国高强度聚焦超声(HIFU)行业全景洞察:随着技术不断改进和产业链不断完善,行业市场前景广阔[图]](http://img.chyxx.com/images/2022/0330/dd2a6e2dd1963d26c8672c625ba6166e69bd4120.png?x-oss-process=style/w320)